Фармкомпания из России создает лекарство, которое "затормозит" старение. Теломеры и старение клеток лекарство
Теломеры и продолжительность жизни человека — Остановить старение человека
Ограничение деления клеток (Лимит Хейфлика). Когда теломеры в клетке себя исчерпывают, то клетка больше не способна делиться – организм стареет и умирает. Теломеры грубо ограничивают максимальную продолжительность жизни человека на отметке в 110-120 лет.
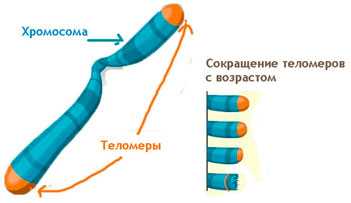
Теломеры и продолжительность жизни человека
Каждая клетка в организме имеет теломеры, длина которых уменьшается с каждым новым делением клеток. Но длина теломер способна восстанавливаться под воздействием фермента теломеразы. В отличие от половых, стволовых, некоторых других тканей организма и раковых клеток в обычных клетках фермент теломераза (который восстанавливает длину теломер) отсутствует, поэтому они не могут делиться бесконечно и ткани изнашиваются, ограничивая продолжительность жизни человека. Весьма положительно влияют на длину теломеров витамин B12, Витамин В6+магний, витамин В9, витамин D3, цинк и умеренная физическая нагрузка, хорошее настроение. Отрицательно– сильный хронический (на протяжении многих лет) стресс, депрессия, хронические инфекции, малоподвижный образ жизни (особенно сидячий образ жизни — лучше лежать или стоять), чрезмерные физические нагрузки, канцерогены в питании, курение, соль в продуктах питания.
В конце 2013 года учёным удалось точечными воздействиями восстановить длину теломеров в опытах на старых крысах без ущерба для их здоровья. В результате шёрстка животных стала гладкой, и исчезли другие признаки старения. Продолжительность жизни крыс выросла на 70%. Следующий этап – эксперименты на обезьянах, а в дальнейшем на людях. Остаётся ждать.
- 1985 — открытие теломеразы (C. Greider, E. Blackburn)
- 1998 — введение гена теломеразы в фибробласты человека увеличивает продолжительность их жизни in vitro без признаков малигнизации (Bodnar et al.)
- 2009 – Нобелевская премия по физиологии или медицине: E.Blackburn, C. Greider, J. Szostak
Источники информации: Von Zglinicki T. (2002). «Oxidative stress shortens telomeres» (английский). Trends in biochemical sciences 27: 339–344.
Каждую неделю публикуются новые научные открытия, и появляются новые средства, с помощью которых возможно продление жизни. Наука развивается очень быстро. Рекомендуем Вам стать подписчиком на новые статьи блога, чтобы быть в курсе.
Уважаемый читатель. Если Вы находите материал данного блога полезным и имеете желание, чтобы данная информация была доступна всем, то можете помочь в раскрутке блога, уделив этому всего пару минут Вашего времени. Для этого пройдите по ссылке.
Рекомендуем также прочитать:
- Аспирин кардио предупреждает рак, инсульт, инфаркт, стимулирует продление жизни на 8%.
- Метформин — самое изученное и надёжное лекарство для продления жизни.
- Сегодня мы живём 70 лет, а раньше люди жили мало — всего 25 лет.
- Старость человека — единое заболевание, а рак и инсульт – это симптомы старости.
- Жизнь в аскетических условиях, трудности, вредные воздействия стимулируют продление жизни человека.
- Никотинамид рибозид — продление жизни нематод на 240%
- Некоторые витамины группы Б и витамид Д продлевают жизнь на 5-18%
- Бег трусцой стимулирует продление жизни до 10%
- Мёд ускоряет старение человека сильнее сахара — доказанный факт
- Миф о том, что красное вино полезно
- Миф о том, что кофе вреден: кофе предупреждает многие болезни и стимулирует продление жизни.
- Как остановить старение человека http://nestarenie.ru/
nestarenie.ru
Биолог Билл Эндрюс о теломерах и лекарстве от старости
Интервью с биологом Биллом Эндрюсом, автором исследования, которое может сделать нас бессмертными

Известный американский ученый Билл Эндрюс вплотную подошел к созданию препарата, замедляющего старение клеток. Лекарство действует за счет теломеразы — фермента, который Билл обнаружил вместе со своей исследовательской группой. Ученый также занимается бегом и в свои 62 одолел сложнейший ультрамарафон в Гималаях, — а это 222 километра без остановки в разреженном горном воздухе. T&P поговорил с ним о здоровье, спорте и старости, наступление которой можно отсрочить и без таблеток.
— Ваши разработки основаны на исследовании теломер и теломеразы. Что это такое и как это работает?
— Теломеры — это кончики наших хромосом. В живой природе в хромосомах содержатся молекулы ДНК с генетической информацией, определяющей цвет волос, глаз и все остальное. Каждая такая молекула — как длинная цепочка записей, или «оснований». В каждой хромосоме их сотни миллионов. На самом деле молекула ДНК похожа на шнурок для ботинок, а теломеры — на пистончики у него на концах. За последние 30 лет мы узнали, что с возрастом эти пистончики уменьшаются, и доказали, что короткие теломеры связаны почти со всеми мыслимыми болезнями, которыми с возрастом может заболеть человек. Сейчас мы пытаемся восстановить длину теломер в живой клетке или, по крайней мере, замедлить процесс их сокращения. Мы выпустили сотни публикаций в научных журналах, рассказывая о том, как они связаны с состоянием здоровья человека. Мы не знаем точно, что здесь причина, а что — следствие, но большая часть исследований доказывает, что уменьшение теломер вызывает заболевания, а не наоборот.
Я возглавлял исследовательскую группу, которой удалось открыть фермент под названием теломераза, ответственный за поддержание длины этих участков хромосом. Теломераза производится только в наших гаметах: дети рождаются с длинными теломерами, а потом, с возрастом, начинается процесс их сокращения. Мы взяли теломеразу, ввели ее в другие человеческие клетки в чашке Петри и увидели, что клетки стали моложе, а теломеры в них выросли. Вторая группа ученых в той же компании позже поместили эти клетки на спинки лабораторных мышей и заметила, что кожа в этих местах вновь стала молодой. Это говорит о том, что механизмы старения можно повернуть вспять.
После этих открытий третьей группе специалистов в Гарварде, возглавляемой доктором Рональдом де Пино, с помощью техник генной терапии удалось удлинить короткие теломеры старых мышей. Когда они сделали это, то увидели, что за несколько недель мыши опять стали молодыми. Это избавило их от множества заболеваний, связанных с возрастом. Мы не знаем на 100%, может ли восстановление теломер лечить болезни, но я, опираясь на множество научные публикации, на 99% уверен, что может. И все же мы хотим узнать это точно, прежде чем создадим таблетки для людей. К тому же техники, которые применялись в случае с мышами, не подходят человеку: не из-за теломеразы, а из-за побочных эффектов самой генной терапии.
Моя компания тестирует химические вещества и добавляет их к человеческим клеткам в чашках Петри в поисках того, что запустит процесс производства теломеразы. Среди сотен тысяч «претендентов» мы нашли природные вещества, которые сегодня использует для производства своих продуктов фирма Isagenix. Кроме того, в Южной Корее, Новой Зеландии, Австралии и Китае существует косметика для кожи, эффект которой основан на действии теломеразы, — хотя здесь для производства используются синтетические вещества. Мы провели клинические исследования этого крема и обнаружили, что это самое эффективное средство против морщин и для восстановления эластичности кожи, которое мы когда-либо рассматривали. К сожалению, мы не изучали влияние этого крема на ранки, хотя пользователи говорят, что он их заживляет.
— Вообще, есть гипотеза, что весь процесс старения существовал не всегда. Это так?
— Я уверен, что старение — это недавнее изобретение эволюции. На нашей планете до сих пор есть существа, у которых отсутствует этот механизм, — или, во всяком случае, мы его не замечаем. Это омары, черепахи, двустворчатые моллюски, некоторые киты, рыбы и птицы. У всех этих животных в клетках постоянно производится теломераза, а теломеры не укорачиваются.
Все это было открыто недавно, поскольку на самом деле людей никогда не интересовало, как долго живут животные. По большинству животных нельзя определить их возраст, у них нет «колец роста» или морщин. Можно только найти новорожденное животное, поместить на него какое-нибудь устройство и наблюдать. В некоторых случаях даже спустя много лет животное не выказывает никаких признаков старения.
У Чарльза Дарвина, например, была черепаха по кличке Гариетта, которая внезапно умерла в возрасте порядка 180 лет, — но это было не из-за старости. Есть черепахи, которые появились на свет больше двухсот лет назад и до сих пор живы. Недавно рыбаки выловили гренландского кита, на шкуре которого нашли гарпун, сделанный 130 лет назад. А у двустворчатых моллюсков на панцире есть полосы, каждая из которых вырастает за год, — и сейчас люди находят моллюсков старше пятиста лет. Все это происходит потому, что их теломеры не становятся короче, а теломераза вырабатывается во всех клетках организма. У таких животных также редко возникают тяжелые болезни, в том числе рак.
Возникает вопрос — почему в природе появился процесс старения? Думаю, для этого есть отличное теоретическое объяснение. Цель эволюции — помочь нам адаптироваться к изменениям среды. За последние две тысячи лет мы смогли в этом преуспеть и стали достаточно разумными. Нам позволила сделать это наша способность тасовать гены: ведь если двое людей или животных производят потомство, они создают вариант, который никогда прежде не существовал на планете. Так мы безостановочно улучшаем свою способность приспосабливаться к переменам и улучшаем шансы на выживание вида в будущем — за счет новых детей и новых поколений.
Однако если старики не стареют, а остаются здоровыми и умудренными опытом, молодежь не может с ними соревноваться — ни за еду, ни за невест и все остальное. В результате гены тасуются реже. То есть вид выживает лучше, если старых существ убивают. У долгой жизни нет преимуществ после того, как вы вырастили детей: когда они становятся взрослыми, вы превращаетесь в их конкурента.
Тем не менее с точки зрения механизма старение в природе бывает разным: мыши, например, становятся дряхлыми из-за окислительного стресса и сердечнососудистых заболеваний. Существует двадцать разных теорий о том, почему мы стареем. Я не могу поверить ни в одну из них, но вижу, что все они рассматривают умирание как процесс сгорания клеток. Вопрос заключается в том, когда и как этот процесс запускается. Я предполагаю, что сегодня эволюция «отрабатывает» разные его варианты. Возможно, сотни тысяч лет назад старения не существовало, поскольку волноваться о конкуренции с потомками было не нужно: все могли найти себе место и так.
Ученые обнаружили, что из-за укорачивания теломер стареют только люди и другие приматы, а также собаки, кошки, лошади, овцы, медведи и свиньи. У остальных живых существ этот процесс устроен иначе, — или его просто нет. Любопытно, что большая часть животных, которых я перечислил выше, была одомашнена. Это заставляет меня задумываться над тем, могло ли приручение, когда охотиться и защищать себя стало не нужно, заставить их создать новый механизм старения в процессе генетической эволюции вида. При этом кроликов или мышей мы тоже приручили, — и все же они стареют не от укорачивания теломер.
— Люди все равно хотят жить долго — с потомством или без него. Есть ученые, которые говорят, что человеческий организм рассчитан на 100 или даже 120 лет. Так ли это?
— Три независимых исследования, проведенных в последние годы, подтвердили, что продолжительность человеческой жизни растет. И во всех случаях максимальный возраст, по расчетам, составлял 125 лет. Сегодня мы уже не живем до 20 лет, как древние римляне, и не живем до 45, как люди Средневековья: наш средний возраст на момент смерти составляет порядка 80 лет. Однако при этом максимальная продолжительность жизни с древних времен совсем не увеличилась.
Укорачивание теломер прекрасно это объясняет. Если поместить человеческие клетки в чашку Петри, мы увидим, что их длина сокращается примерно на 5200 оснований за один год. В момент рождения длина теломер составляет 10 тысяч оснований, а через 125 лет после этого — 5 тысяч. И это при условии, что мы ведем идеально здоровый образ жизни. Однако мы этого не делаем: мы курим, набираем лишний вес, пренебрегаем спортом, переживаем стресс.
Как только мы найдем способ замедлить процесс сокращения длины теломер, остановить его совсем или даже вновь удлинить короткие теломеры, это позволит людям жить дольше, чем до 125 лет. Возраст самого старого человека на планете в данный момент составляет 116 лет, так что в лучшем случае пройдет еще как минимум восемь лет, прежде чем мы сможем проверить теорию. И у нас пока нет лекарства от старости. Есть только вещи вроде продукции Isagenix, хотя мы ожидаем, что люди, которые пользуются ею, смогут прожить больше 125 лет.
«Я хочу доказать, что я или кто-то другой может прожить больше 125 лет. Нет смысла жить долго, если ты не живешь полноценно»
Я воспринимаю старость как болезнь, от которой мы все страдаем, и ищу от нее лекарство. Многим людям, особенно в Управлении по надзору за качеством продуктов питания и лекарственных средств Правительства США (FDA), не нравится то, что я так это называю. Но когда я буду пробегать одну милю (1,6 км) за семь минут в возрасте 100 лет, они тоже начнут так говорить о старости. Я хочу доказать, что я или кто-то другой может прожить больше 125 лет. Нет смысла жить долго, если ты не живешь полноценно. Я хочу быть способным показать, что можно быть молодым и здоровым в 130 лет. Когда я или кто-нибудь еще выполнит эту задачу, я скажу: теперь все обязаны согласиться, что старость — это болезнь, и ее можно вылечить.
— Вы говорили, что ваш биологический возраст сейчас почти на 20 лет отстает от фактического.
— Да, в 60 лет я прошел тесты компании Life Length, где врачи измерили длину моих теломер. Они установили, что мой биологический возраст — 42 года. Через неделю после этого этого лаборатория Терри Гроссмана прислала результаты других, не связанных с теломерами тестов. Они тоже определили мой возраст как 42. Честно говоря, в детстве я представлял 60-летних людей совсем иначе, и это потрясающее чувство.
Я учитываю все теории старения, которые существуют сегодня, и делаю все, что могу: веду здоровый образ жизни, включаю в рацион антиоксиданты, витамин D, жирные кислоты омега-3, занимаюсь спортом, стараюсь сократить стресс и количество всякого мусора в жизни и быть оптимистом. Главное, что стоит знать, — смерть чаще всего наступает, только когда теломеры становятся короче: хромосомы, по сути, просто начинают расщепляться на концах. Этот процесс, вероятно, может вызвать множество заболеваний: рак, сердечнососудистые патологии, болезнь Альцгеймера, остеопороз и дистрофию мышц.
— Вы много бегаете. Что нужно, чтобы начать заниматься бегом?
— Чтобы начать бегать, нужно ходить. Ходьба так же хороша, как бег, — она просто занимает больше времени. «Встань и иди», — так говорят в моей любимой группе тренеров по бегу Desert Sky Adventures. Большинство людей, которые начинают много ходить хотя бы шесть дней в неделю, через месяц или два уже не могут удержать себя на месте и не побежать. Тело становится энергичнее, суставы работают лучше. Я, кстати, впервые столкнулся с болями в них, когда сделал перерыв в беге. Но каждый раз, когда я возвращаюсь к этому занятию, боли проходят, и через две-три недели остается только удовольствие.
— Какие у бега есть преимущества?
— Это удивительно, но если вы будете каждый день сажать мышь на беговую дорожку и тренировать ее выносливость, это сократит ее жизнь. При беге в организме возникает множество свободных радикалов, которые очень вредят мышиному организму. У мышей есть ужасная проблема со свободными радикалами — проблема окислительного стресса, от которого они стареют и погибают. Однако у людей все иначе. И у людей, и у мышей имеются антиоксиданты, которые убирают свободные радикалы. Однако у мышей их уровень очень низок: в 10 раз ниже, чем у человека. Когда люди подвергают себя стрессу во время упражнений на выносливость, они, как и мыши, производят множество свободных радикалов внутри своих тел, — но при этом у них подскакивает уровень антиоксидантов, и в результате уровень окислительного стресса оказывается ниже, чем если упражнения не делать.
Есть научные публикации, которые рассказывают о том, что чем больше ты тренируешь выносливость, тем длиннее твои теломеры. Я относился к этому с подозрением 25 лет назад, но сейчас удивлен тем, сколько 80-летних людей хотят пробежать 100 миль, забыв, что они старые. Они активны, как подростки, и они очень хорошо бегают. Когда я бежал свои первые 100 миль, одна 75-летняя женщина сказала мне, что будет бежать рядом, чтобы показать, как вести себя на ультрамарафонах. Когда мы прошли 85 миль, она заметила: «Похоже, у тебя все в порядке. Я поддам газу, увидимся позже». Она рванула вперед и опередила меня на полчаса. Я никак не мог с ней тягаться. Сейчас ей 90, и она еще бегает. Мой биологический возраст сейчас по-прежнему составляет 42 года, а бегать ультрамарафоны я начал 26 лет назад, когда мне было 38 или 39.
— Какой из ваших ультрамарафонов был самым трудным?
— La Ultra The High в Гималаях, в Северной Индии. В мире есть и другие сложные ультрамарафоны: например, летний Badwater длиной в 135 миль, в Долине Смерти, при температуре 54 градуса Цельсия. Я пробежал его дважды, но это не было и в половину так же тяжело, как La Ultra. Самые высокие точки ее маршрута находятся на высоте 5,5 км над уровнем моря, самые низкие — на высоте 3,3 км. Когда я участвовал в этом ультрамарафоне, длина маршрута составляла 222 км. Нон-стопом.
Я был одним из трех бегунов, которые участвовали в гонке в первый год ее существования. Тогда правительство было уверено, что преодолеть эту дистанцию в таких условиях невозможно, ни один человек не сможет справиться с этим. Организаторы разослали приглашения 25 бегунам, которые уже испробовали свои силы на маршрутах вроде Badwater, и 22 из них отказались. В назначенный день на старте стояли всего трое — и двое, включая меня и мою жену Молли Шеридан, в результате оказались в больнице. Только один парень из Великобритании пришел на финиш, едва успев вовремя. Моя жена вернулась к La Ultra The High через год, чтобы все-таки пройти ее с начала до конца, а я вернулся спустя два года. Молли стала первой американкой и вторым человеком из списка старейших бегунов, которым удалось это сделать, а самым старым оказался я.
В первый год у меня случился приступ желчекаменной болезни на 50-й миле. Я думал, что умру. У меня не было высотной болезни, но на второй год существования ультрамарафона множеству спортсменов пришлось сойти из-за нее с дистанции. Я очень жду еще одной возможности принять участие в La Ultra The High. Теперь дистанция составляет 333 км, и я хочу пробежать их. Пока лишь одному человеку удалось пройти это расстояние до конца.
— Вы боец.
— Нет, я думаю, это просто весело, это приключение. Я жить не могу без приключений, а лучший способ в них ввязаться — это быть в движении. Скоро в прокат выйдет документальный фильм «The High», в котором снималась моя жена. В этой картине хорошо видно, что такие соревнованя — это прежде всего общение.
— Ваша работа в медицине похожа на марафон?
— Когда я основал компанию, я сказал себе: «Это мой новый ультрамарафон». Я тратил 100% времени на нее, несколько лет почти не бегал и в результате набрал 45 кг. У меня появились все проблемы, которые обычно бывают связаны с лишним весом, и мой врач сказал: «Вернись к своим ультрамарафонам или умрешь». Я стал бегать снова, и теперь не собираюсь останавливаться. Я расставил приоритеты и стараюсь оставаться в хорошей форме. Это никуда не годится: вылечить человечество от старости и умереть из-за проблем со здоровьем, чтобы потом все, кроме меня самого, наслаждались плодами моей работы. Я уверен, что появится средство, которое увеличит срок нашей жизни, удлинив теломеры и повернув старение вспять. Думаю, это лекарство будет у нас через три года.
— Почему именно через три?
— Потому что мы вышли за пределы своих прошлых достижений и делаем новые открытия. Сначала мы нашли вещество, которое позволяло произвести в клетках 1% монотеломеразы, необходимой для того, чтобы остановить процесс сокращения длины теломер. Потом мы открыли другие вещества и добрались до 5%. Затем начали работать в области медицинской химии и поднялись до 60%. Недавно мы оценили свою динамику продвижения и увидели, что через год будет 100%, — если мы найдем источник неограниченного финансирования. Однако его у нас пока нет. Так что мы думаем, с учетом средств, которые мы, как я надеюсь, скоро получим, нам потребуется три года.
Чтобы сделать это лекарство в США, нам придется проводить испытания на животных. Мне бы очень хотелось этого избежать, но, к сожалению, по нормам FDA они необходимы. Возможно, мы разработаем средство, которое можно будет продавать в других странах, и тогда таких испытаний не потребуется. Откровенно говоря, я не думаю, что они нужны: все животные, на которых, по закону, нужно тестировать препараты, стареют не из-за уменьшения длины теломер. Главное животное в этой области — мышь, и в ее случае мы ничего не сможем увидеть. Есть, конечно, те мыши из Гарварда, и, может быть, нам удастся провести испытания на них. Но проблема в том, что даже у этих мышей механизм производства теломеразы сильно отличается от человеческого. Его создали искусственно, и есть вероятность, что лекарство не подействует. Так что, когда все будет готово, мы, вероятно, попытаемся выйти на рынок за пределами США. Я много работаю с Южной Кореей, Новой Зеландией, Австралией и Китаем и знаю, что там сделать это проще. Конечно, тут некрасиво думать о коммерции, но, чтобы люди смогли использовать средство, к нему должен быть доступ. Полагаю, в первое время будет множество людей, которым такое лекарство окажется жизненно необходимо.
Каждый раз, когда кто-то умирает, я думаю, что это наш провал. Я хочу, чтобы это закончилось как можно скорее. Не знаю, какие законы регулируют выпуск лекарств в России, но думаю, было бы здорово, если бы этот препарат появился и у вас.
— Российский биохимик Владимир Скулачев также разрабатывает препараты против старения. Я говорила с ним пять лет назад, но тогда он не упоминал теломеры.
— Теломеры — это достаточно свежая идея. Мы никому не рассказывали о своих исследованиях до 2008 года, а потом из-за трудностей с финансированием решили представить их публике. Тогда начался экономический кризис, и все мои инвесторы потеряли возможность вкладывать средства в проект. Мы были первыми, кто начал работать в этой сфере и добился успеха, так что наши разработки получили широкий отклик. Но даже сегодня 99% людей ничего не знает о теломерах. И все же я думаю, что они связаны с одним из крупнейших прорывов в области медицины. О лекарстве от старости и вечной молодости люди говорили тысячи лет, и сегодня никто не обращает внимания на эту тему, но это скоро изменится. Как только произойдут большие открытия, люди начнут отходить от старых представлений и увидят, что теперь это настоящая наука.
— Почему вам так хочется победить старость и смерть?
— Я люблю жить. Я хочу делать это так долго, как только смогу. Мой отец в старости ужасно изменился из-за болезни Альцгеймера, а мать стала инвалидом. Отцу нужна помощь сиделок, мама к этому близка. Я не хочу пройти через это и не хочу видеть, как кто-то другой через это проходит. Дело не просто в старости — дело в болезнях. Они — основная причина, по которой люди не хотят долго жить. Ученые уже так много сделали для того, чтобы увеличить продолжительность человеческой жизни, — но не пока смогли заметно увеличить продолжительность ее здорового периода. В результате множеству людей приходится пройти через операции на сердце, коронарное шунтирование, химиотерапию и другие процедуры, которые помогают выжить. Через 20 лет порядка 40% населения планеты будет старше 65 лет. В мире будет очень много стариков, — особенно в Китае, Южной Корее и США. Россия тоже столкнется с этой проблемой. Во всех этих странах появится колоссальная потребность в медицинской помощи. Так что когда студенты спрашивают меня, какую специальность лучше выбрать, я говорю: уход за пожилыми пациентами. Это профессия будущего номер один, которая будет самой востребованной и высокооплачиваемой в мире.
И все же нам не нужно, чтобы старики лежали в больницах, нуждаясь в чужой заботе. Я хочу, чтобы люди старше 60 танцевали, играли в теннис и тратили свободное время в свое удовольствие. Они должны быть здоровыми. Вот почему о продолжительности здорового периода жизни нужно думать больше, чем о ее сроке в целом. Когда его границы станут шире, срок жизни увеличится и так.
Я хочу, чтобы люди жили очень долго, возможно, несколько сотен лет, не выказывая признаков увядания. И все же мы не называем клетки без укороченных теломер бессмертными. Теломераза не избавит человечество от смерти. Люди все равно будут погибать в автокатастрофах или на железнодорожных путях, и в мире все равно останутся болезни — ведь не все они, даже не все онкологические заболевания, возникают из-за укорачивания теломер. Однако в среднем все изменится очень сильно. Мы увидим множество людей, старых де-факто и при этом очень молодых биологически.
— За что же вы так любите жизнь?
— Я обожаю приключения. Я люблю природу, меня захватывают открытия. Не могу дождаться момента, когда люди откроют жизнь на других планетах. Я хочу быть здесь, когда это случится, и участвовать в исследованиях, когда мы попытаемся узнать, что это за живые существа. Нам предстоит так много открытий, и мне хочется быть их частью. Меня приводит в восторг изучение океана на Земле и ДНК существ, которые в нем живут.
В детстве мои братья и сестры увлекались наукой и медициной так же сильно, как я. Когда мне было 10, я мечтал о телескопе, чтобы можно было рассматривать звезды. В тот год на Рождество мне подарили игрушечный телескоп, и это так меня расстроило, что я разрыдался. Родителей так шокировало то, как серьезно я относился ко всему этому, что они купили мне зеркальный телескоп, который я хотел. Он был 2,5 метра в длину, 200 мм в диаметре. Немыслимый подарок для 10-летнего ребенка. Я каждую ночь торчал во дворе, рассматривал Юпитер и его луны, Сатурн и его кольца, и постоянно бегал в дом, звал родителей, братьев и сестер, чтобы они тоже на них посмотрели. Там, возле телескопа, отец однажды сказал мне: «Ты так увлечен наукой и медициной. Ты должен стать врачом, когда вырастешь, и найти лекарство от старости». Вот уже 53 года я одержим этим. Каждый раз я думаю: «Боже, какая великолепная идея!».
Я люблю жизнь из-за того, что можно узнать что угодно. В этом весь смысл приключений. Что будет за следующим поворотом, что случится через несколько лет? Вот почему мне легко бегать марафоны длиной в 100 миль. Я всегда хочу пройти дальше и увидеть, что там. Я так сосредоточен на том, что впереди, что теряю счет времени. Иногда кажется, что пробежать 100 миль так просто, и это занимает так мало времени. Знаете, маршрут марафона иногда бывает круговым, а иногда — линейным, когда точка финиша оказывается совсем не там, где точка старта. В последний раз было так; на финиш я прибежал, а обратно к старту мы поехали на машине, и меня потрясло, как далеко они оказались друг от друга. На бегу я этого совсем не чувствовал.
Ты получаешь настолько больше приключений, когда встаешь с места и двигаешься вперед. Можно оказаться там, куда никто не может попасть, увидеть нетронутый ландшафт. На некоторых ультрамарафонах еду и воду можно получить, только если вертолет привезет их. Я жить не могу без таких соревнований.
И мне нравится общаться с людьми. Каждый раз, когда я с кем-то знакомлюсь, это новое приключение. Думаю, если я когда-нибудь и устану жить, то только если потеряю здоровье, и кому-то придется заботиться обо мне. Такого со мной еще не бывало, и я делаю все, чтобы этого не произошло. Удивительно, но подобная забота о ком-то тоже вызывает укорачивание теломер. Сейчас проходят исследования с участием людей, которые профессионально занимаются этим, и организаторам удалось выяснить, что болезнь или старость, по сути, плохо отражается не только на пациенте, но и на его помощниках.
— Вас, кстати, кажется, критикуют христиане — в основном за попытки изменить продолжительность человеческой жизни.
— Нет, на самом деле, забавно, но мы обнаружили, что это не так. Один из наших самых увлеченных потенциальных инвесторов сейчас — это католическая больница. А другие представители католической церкви даже написали целую главу для моей книги «Curing Aging». Они объяснили, почему это может быть частью плана творения. Согласно Библии, Бог изгнал людей из Эдема, и одним из качеств, которые мы потеряли после этого, было бессмертие. Мы начали стареть после падения, и Бог хочет, чтобы мы однажды от этого избавились, вернув себе свою вечную жизнь.
— Вам пришлось пережить много трудных моментов в поисках инвестиций и признания в научном мире. Что заставляет вас продолжать?
— Самое трудное в такой работе — это финансирование. Я столько раз терял его: не было денег даже на зарплаты сотрудников. Но каждый раз мне удавалось как-то спастись, вынув кролика из шляпы в последний момент. Меня заставляет двигаться вперед моя вера в то, что мы делаем. Она очень сильна. Когда я думаю о том, что мы можем потерпеть поражение из-за денег, то понимаю, что никто не станет дальше делать нашу работу вместо нас. Я просто боюсь, что, если мы проиграем, через 300–400 лет кто-нибудь поймет, что мы были правы, и я окажусь в учебнике истории, где будет написано: «Билл Эндрюс сделал это 400 лет назад, но не смог закончить работу из-за проблем с деньгами». Это так меня угнетает! Единственная цель моей жизни — провести исследования и доказать, что увеличение длины теломер значительно увеличивает срок жизни и продолжительность ее здорового периода. Возможно, у старения есть другие причины. Но наши открытия должны дать мне еще 20–30 лет жизни, чтобы я смог выяснить это. Если мы соберем вместе все исследования, которые сейчас проводятся, то увидим, что сможем скоро достичь бессмертия. Есть надежда, что это произойдет, пока наше поколение еще будет в живых, — особенно если мы сможем увеличить срок своего пребывания здесь благодаря теломеразе.
econet.ru
Популярно о сложном: теломеры и молодость организма
Теломеры — последовательности ДНК, повторяющиеся и локализуюються на концах хромосом. При каждом делении клетки теломеры укорачиваются, что в конечном итоге приводит к потере способности клетки к делению, физиологического старения и гибели. Накопление подобных клеток в организме повышает риск патологий. Еще в 1962 году Леонард Хейфлик (Leonard Hayflick) разработал революционную теорию в биологии, известную как теория разделения Хейфлика. Согласно этой теории, максимальная продолжительность жизни человека может составлять 120 лет. По теоретическим подсчетам именно к этому возрасту в организме накапливаются клетки не способны делиться и поддерживать жизнедеятельность. Через 50 лет генетика открыла человеку перспективы оптимизации собственного генетического потенциала и путь к продолжению молодости.
 Теломеры и молодость организма
Теломеры и молодость организмаРазличные стрессовые факторы способствуют преждевременному укорочению теломер, что ускоряет биологическое старение клеток. Уже доказано взаимосвязь между сокращением теломеров и заболеваниями сердца, ожирением, сахарным диабетом, дегенерацией хрящовоих ткани, ограничением овариального резерва. Укорочение теломер снижает эффективность функционирования генов, что приводит к триаде проблем — воспаления, окислительного стресса и снижения активности иммунных клеток.
После 3-летнего наблюдения за 110 000 добровольцами специалисты предоставили следующие данные — в группе пациентов, у которых теломеры были на 10% короче, уровень смертности был на 23% выше.
При исследовании 787 добровольцев в течение 10 лет оказалось, что у тех, кто имел критически короткие теломеры, в 3 раза больше рискуют заболеть онкопатологии и в 11 раз больше умереть по сравнению с теми, у кого длина теломер была максимальной.
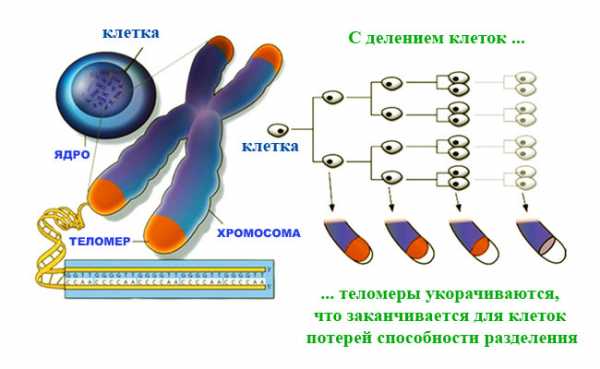 Теломер
ТеломерЕще одним важным аспектом является качество теломеров. Например, пациенты с заболеванием Альцгеймера не всегда короткие теломеры. В то же время их теломеры всегда демонстрируют выраженные признаки функциональных нарушений, коррекции которых способствует витамин Е. В определенном смысле теломеры являются «Ахилесовою пятой» ДНК. Они легко поражаются и нуждаются в восстановлении, однако не обладают мощными репарационному механизмами, как в других участках ДНК. Это приводит к накоплению частично пораженных и плохо функционирующих теломеров, низкое качество которых не зависит от их длины.
Торможения процесса старения возможно при применении стратегий, притормаживают процесс укорочение теломер, одновременно защищая их и устраняя повреждения, которые возникают. В последнее время специалисты одержають все больше данных о правильно подобранный рацион питания и употребление витаминов в
znaxar.info
Теломеры и теломераза в процессе старения
Он несколько напоминает поезд: движется по рельсам в виде двойной спирали ДНК и "буква за буквой" воспроизводит ее нуклеотидную последовательность, изготовляя идентичную молекулу, которая остается рядом с оригиналом.
Однако у ДНК-полимеразы есть существенный недостаток. По причинам, углубляться в которые нет необходимости, вся молекула ДНК этим ферментом никогда не копируется.
Иными словами, при каждом клеточном делении небольшой ее участок теряется, и скопированная цепочка оказывается короче исходной. Конец хромосомы постепенно "обгрызается".
Вторая возникающая с хромосомами проблема - их тенденция часто рваться из-за действия радиации и других неблагоприятных факторов. Клетке приходится сшивать возникающие обрывки. При этом, разумеется, она ни в коем случае не должна путать их с концами интактных хромосом, и, следовательно, ей надо каким-то образом различать эти два типа участков ДНК.
Частично такая проблема решается природой с помощью теломер. Эти концевые участки хромосом не содержат генетической информации, представляя собой монотонные повторы короткой последовательности нуклеотидов. Их укорочение при многократных копированиях ДНК и клеточных деления никакого вреда организму не приносит - пока теломеры остаются достаточно длинными. однако ее полного исчезновения бояться не стоит, поскольку существует фермент теломераза, который удлиняет эту бессмысленную концевую последовательность ДНК.
Точнее говоря, он решает сразу две проблемы. С одной стороны, экспрессирующие теломеразу клетки восстанавливают свои укорачивающиеся при каждом делении теломеры и могут делиться неограниченно долго. С другой стороны, сохранение теломер не позволяет механизму, устраняющему разрывы ДНК, сшивать разные хромосомы: бессмысленные концевые повторы распознаются соответствующими ферментами и оставляются в покое.
Люди и некоторые другие виды остроумно используют эту теломернотеломеразную систему для защиты от рака. Злокачественные клетки убивают организм только после многократного деления. Без теломеразы это невозможно: если теломеры не будут восстанавливаться, они постепенно исчезнут, концы хромосом, перестав отличаться от внутрихромосомных разрывов, в конце концов, соединятся, а в результате раковые клетки как минимум не смогут больше делиться. Поэтому кодирующие теломеразу гены в них по мере возможности отключаются.
Для восстановления активности этого фермента и, соответственно, способности раковых клеток к делению потребовалось бы много очень "удачных" мутаций. Хотя этот вопрос изучен меньше, у пожилых носителей цитомегаловируса (ЦМВ) наблюдается также избыток дефектных СD4-лимфоцитов, называемых Т-хелперами, которые помогают другим компонентам иммунной системы организовать контрнаступление на проникшие в организм патогены. Иными словами, у этих внешне здоровых людей происходит такая же клональная экспансия нацеленных на ЦМВ, но лишенных рецептора CD28 СD4-клеток, как и в их СD8-популяции. Результат - аналогичное перенасыщение специализированными лимфоцитами, не реагирующими на активацию антиген-презентирующими клетками.
Не активируясь ими, эти дефектные Т-хелперы не выполняют своей функции, т.е. не обеспечивают мобилизацию на борьбу с врагом СD8-лимфоцитов и других иммунных клеток. Такая ситуация - вместе с упоминавшейся выше неспособностью Т-киллеров эффективно атаковать свои мишени - дает цитомегаловирус беспрепятственно размножаться. Это ведет к дополнительным клональным экспансиям и дальнейшему усугублению иммунной дисфункции.
Клонально размножившиеся ЦМВ-специфичные СD8-клетки анергичны (неэффективны) и с других точек зрения. При первом заражении мышиным вариантом этого вируса молодые мыши вырабатывают очень активные Т-киллеры, распознающие не менее 24 его антигенов. Однако, когда инфекция становится хронической, их нацеленные на ЦМВ спецподразделения сокращаются до клонов, реагирующих в среднем лишь на пять таких белков. Кроме того, у пожилых людей с цитомегаловирусом анергические СD8-клетки реагируют на вирус слабее, чем у молодых его носителей, вырабатывая значительно меньше гамма-интерферона, одного из важнейших химических усилителей иммунологического ответа.
Плохие полководцы хороших армий
Вероятно, неспособность анергических Т-лимфоцитов бороться с ЦМВ-инфекцией ведет ко многим другим типичным для пожилых людей иммунологическим дисфункциям, которые нельзя объяснить никаким непосредственным эффектом старения этих клеток. Некоторые из таких эффектов можно было бы ожидать в связи с изменением выработки ими цитокинов, влияющих на активность прочих бойцов врожденной и адаптивной частей иммунной системы, однако другие вызывают гораздо более стойкие последствия, чем просто проблемы с химической сигнализацией.Например, согласно широко распространенному сейчас мнению, старение Т-клеток объясняет возрастное снижение эффективности В-лимфоцитов, синтезирующих антитела к чужим антигенам и метящих таким образом патогены как мишени для разрушения другими клетками. Для созревания и выработки антител В-клеткам необходимы сигналы от Т-хелперов, поэтому доказательство того, что старость Т-клеток вызывает снижение эффективности В-лимфоцитарной системы, независимое от ее собственного старения, было лишь вопросом времени.
К сожалению, никто пока не выяснял, обусловлен ли такой эффект индуцированной цитомегаловирусом клональной экспансией Т-лимфоцитов, играющей важнейшую роль в развитии прочих аспектов старения всей их популяции. В результате мы не знаем, насколько сильно влияет на В-клетки такой специфический феномен, как анергизация Т-клеток.
Даже если отвлечься от механистических объяснений и молекулярно-биологических механизмов, реальное влияние ползучего подтачивания всей иммунной системы анергическими СD8-клонами на человеческое здоровье становится очевидным при изучении конкретных результатов этого процесса. Опыты на животных показывают, что возрастная клональная экспансия отдельных СD8-субпопуляций снижает разнообразие присутствующих в организме Т-клеток, а в итоге и их способность обеспечивать эффективную иммунную защиту. Примеры аналогичных этому эффектов у нашего с вами вида - ухудшение СD8-ответа на прививки от гриппа и происходящее несколько позже ослабление Т-клеточного иммунитета против вируса Эпштейна-Барр у людей с клональной экспансией ЦМВ-специфичных клеток памяти.
Подсчет потерь
Даже если бы влияние на организм клонов анергических Т-лимфоцитов ограничивалось повышением заболеваемости и смертности от инфекционных болезней, у нас было достаточно причин желать избавления от этих клеток. Однако есть достаточно веская причина полагать, что они способствуют также возрастному ослаблению организма, которые не находит очевидного иммунологического объяснения.Прежде всего, у пожилых людей, пострадавших от гриппа или спровоцированной им пневмонии, наблюдаются удивительно долгие их последствия, существенно ускоряющие прочие патологические процессы и движение человека в сторону старческой беспомощности, а в конечном итоге и на кладбище. По многим данным, перенесенный в солидном возрасте грипп повышает риск смерти от неожиданных причин типа инфаркта миокарда и инсульта, а также от как будто не связанных с этой инфекцией респираторных заболеваний; кроме того, обостряется течение застойной сердечной недостаточности.
Далее, такое долгое выздоровление биологически старых людей от гриппа, накладываясь на их общую слабость, обусловленную другими аспектами старения, вероятно, способствует серьезной, зачастую пожизненной функциональной деградации и инвалидизации. Грипп нередко укладывает пожилого человека в больницу, порой на целых три недели, а исследования показывают, что каждый день постельного режима означает для него потерю до 5% мышечной силы и 1% аэробической выносливости. Однако, видя, как женщина в возрасте с трудом открывает дверь или, поскользнувшись на льду, ломает себе шейку бедра, никто не думает о перенесенной ею простуде или иммунологическом старении.
Можно вспомнить и о других старческих недугах, в развитии которых, по-видимому, существенную роль играют клоны анергических Т-клеток, но свидетельства этого не настолько очевидны. Одна из таких патологий - остеопороз. У пожилых женщин с остеопорозными переломами обнаружены более высокие уровни анергических СD8-клеток, чем у их сверстниц со здоровыми костями. При этом некоторые молекулярные механизмы наводят на мысль, что обилие таких дефектных лимфоцитов являются именно причиной, а не следствием снижение плотности и прочности костной ткани.
Кроме того, несмотря на сравнительную спекулятивность данного предположения, ползучая "клонализация" Т-клеточной популяции могла бы влиять даже на ход атеросклероза. Она ведет к хроническому воспалительному процессу, который, как известно, портит артерии, способствуя возникновению инфаркта миокарда. В пользу этой гипотезы говорит более высокий, чем у здоровых людей, уровень анергических СD8-клеток у пациентов с ишемической болезнью сердца - как при ЦМВ-инфекции, так и в ее отсутствие. Таким образом, ослабление иммунной системы является, по-видимому, как облегчающим фактором, так и результатом инфекционного поражения артерий, которое в свою очередь благоприятствует развитию атеросклероза со всеми его потенциальными последствиями.
Как уже говорилось, точные доказательства связи анергических клонов Т-клеток с этими отдаленными эффектами пока отсутствуют. Однако пара интересных исследований в рамках осуществляемого сейчас Европейским союзом проекта Т-КИС (Т-клеточный иммунитет и старение), уже приблизил нас к более четкой оценке летальной роли этой причины возрастного иммунодефицита - что бы в конечном итоге ни было написано в свидетельстве о смерти.
Эти исследования касались двух когорт "самых старых" жителей Швеции, т.е. тех, кому за 80 и за 90, причем охватывали только людей, практически здоровых по сравнению с большинством своих хронологических сверстников: с отсутствием в анамнезе серьезных заболеваний сердца, головного мозга, печени и почек, без рака, диабета, признаков активных инфекций или химических маркеров воспаления и не принимающих никаких лекарств, заметно действующих на иммунную систему, включая недавние вакцинации.
Европейские ученые обнаружили даже среди этих относительно здоровых стариков несколько человек с комплексом скрытых иммунологических дефектов ("фенотипом иммунного риска"), например различными формами возрастного поражения, которые можно объяснить цитомегаловирус-инфекцией, а значит, в не меньшей степени и клональной экспансией анергических ЦМВ-специфичных CD8-клеток.
Тот факт, что некоторые представители изученной здоровой, несмотря на большую хронологическую старость (по современным стандартам) выборки были свободны от клонов анергических Т-клеток, позволил проследить их "чистый" эффект в подгруппе, где присутствие таких лимфоцитов могло действительно способствовать развивающимся в следующие два года болезням, а не являться их результатом.
Никого не удивил результат наблюдений: фенотип иммунного риска, как и предполагалось, повышал вероятность скорой кончины, однако масштабы такого влияния шокировали. Оно было особенно выражено в группе людей старше 90, где этот дефицит позволял объяснить 57% смертности. Напоминаем: речь идет о возрастном ослаблении иммунной системы, вызываемом вирусом, активность которого многими из нас вообще не замечается, а в прочих случаях обычно ощущается лишь как легкое недомогание с повышением температуры.
Важно правильно понять все значение этого открытия. Фенотип иммунного риска способствовал всем причинам смертности, а не только повышал риск умереть от инфекционной болезни. Хотя внешние патогены, действительно, убивают многих биологически старых людей, микробные атаки объясняют полученные результаты далеко не полностью.
Война против клонов
По мере накопления данных, говорящих о роли клонов ЦМВ-специфичных CD8-клеток в возрастном ослаблении иммунитета, стала приоткрываться и светлая сторона этого феномена. Если иммунологическое старение в такой значительной степени объясняется экспансией Т-лимфоцитов, значит, ее предупреждение, а тем более обращение вспять должно (соответственно) защищать или восстанавливать молодое состояние иммунной системы независимо от нашего хронологического возраста. А значит, вакцины будут действовать на стариков так же эффективно, как и на юношей. И пожилые люди сбросят неподъемный груз инфекций, от которых молодежь избавляется, всего лишь пару ней не походив в школу или на работу.Один из вариантов профилактики, поддерживаемый многими иммунологами, - вакцинация против цитомегаловируса. Еще до того, как выяснилась центральная роль ЦМВ-инфекции в возрастном ослаблении иммунной системы, опубликованный в 1999 доклад Медицинского института Национальной академии наук США, отмечая неудовлетворительные темпы разработки новых вакцин, поставил на первое место в списке неотложных задач создание эффективной анти-ЦМВ-вакцины. Подчеркнем, что авторы доклада исходили только из накопленной к тому времени информации о человеческих и финансовых потерях, вызываемых этим вирусом.
Позднее Национальное агентство США по программе вакцинации, придя к такому же выводу, запросило у правительства дополнительные средства на исследования в области вакцины против цитомегаловируса. Сейчас, когда получены четкие доказательства важной роли ЦМВ-инфекции в старении иммунной системы, многие специалисты высказываются за дальнейшее увеличение этих ассигнований.
Хотя польза такого подхода и выглядит бесспорной, стоит напомнить, что речь идет главным образом о профилактической стратегии. Она снизит риск заражения ЦМВ и, возможно, усилит иммунный ответ на него уже инфицированных людей, но не избавит их от вируса полностью и, естественно, не устранит накопленного за долгие годы его присутствия иммунологического ущерба.
Следовательно, такая вакцина спасет относительно небольшой процент младенцев от тяжелых врожденных дефектов и предотвратит безвременную кончину многих больных СПИДом и пациентов с пересаженными органами, однако почти не улучшит состояния сотен миллионов людей, уже страдающих от хронических инфекций и повышенной чувствительностью к патогенам из-за ослабления иммунной системы клональной экспансией анергических СD8-клеток.
Другие предложения, хотя бы потенциально устраняющие некоторые аспекты иммунологического старения, связаны с попыткой лечения дефектов уже существующих анергических Т-клеток методами генной терапии. Идея в том, что снабжение этих лимфоцитов генами, кодирующими их утраченные или недостаточно активные белки (например, СD28-рецептор или теломеразу), позволило бы восстановить эффективность выполнения ими своих специфических задач и предупредить угнетение прочих Т-клеточных популяций. Хотя подобный подход и выглядит логичным, польза его представляется слишком ограниченной, а путь клинической разработки - чересчур туманным.
Что же касается конкретно теломеразы, последствия ее активизации в любой клетке вызывают еще много вопросов и требуют более серьезного рассмотрения. Эти сомнения связаны с еще одной возрастной патологией - раком. Поскольку необходима хотя бы крошечная теломера для продолжения делений, каждое из которых ее укорачивает, клеткам с потенциально канцерогенными мутациями для превращения в злокачественную опухоль требуется механизм восстановления теломеры.
Почти все раковые клетки запускают его, срывая собственные тормоза с теломеразных генов. Стоит ли снабжать этими генами дефектные клетки, тем более учитывая риск случайного "заражения" геннотерапевтическими векторами "посторонних" клеток, в которых ни в коем случае нельзя включать теломеразу?
Более правомерным решением выглядит не реабилитация бездействующих лимфоцитов, а их уничтожение. Пожилым носителям цитомегаловируса, по-видимому, не хватает функциональных Т-киллеров, нацеленных на зараженные этим вирусом клетки. Причина такого дефицита - перенасыщение организма огромными субпопуляциями анергических лимфоцитов. Даже если нам удастся вернуть всем им полную иммунологическую компетентность, они будут создавать проблему, все еще ограничивая ресурсы, необходимые для сохранения наивных лимфоцитов и клеток памяти, необходимых для защиты от других патогенов.
Теоретически все выглядит просто. Избавившись от анергических Т-клонов, мы освободим иммунологические пространство для здоровых клеток других типов и специализаций, а том числе и для активных нацеленных на ЦМВ лимфоцитов.
Остается решить вопрос: как очистить организм от расплодившихся бездельников, оставив в живых всех (или хотя бы почти всех) их заложников, которых мы хотим избавить от угнетателей-тунеядцев. Онкологи уже располагают достаточно эффективными и не слишком вредными для организма в целом лекарственными и радиационными методами уничтожения сравнительно крупных опухолей в конкретных участках тела, однако этот подход неприменим в случае анергических Т-клеток, не сконцентрированных в отдельных местах, а распределенных по различным тканям и органам.
По той же причине бесполезно говорить о хирургическом вмешательстве. Опухоль можно вырезать (или как минимум урезать), добившись с определенным риском того или иного клинического улучшения. Однако в ближайшем будущем никаких способов индивидуального хирургического удаления анергических Т-клеток не предвидится.
Тем не менее, несмотря не неприменимость традиционных противораковых методов в качестве образца для разработки необходимой нам биотехнологии, последние впечатляющие успехи онкологов наводят на мысль о принципиальной возможности терапии, обеспечивающей избирательное избавление организма от не желающих умирать клеток.
Аромат Гливека
Даже если никто из ваших знакомых не болен раком, вы вполне могли слышать о гливеке (STI-571, или иматинибе), ирессе (ZD1839, или гефитинибе), герцептине (трастузумабе) и других менее известных или еще прокладывающих путь к больным лекарствах той же группы. Речь идет о так называемой "прицельной противораковой терапии", которую с полным основанием считают революционным новшеством. Даже формулировки типа "чудесных исцелений", абсурдно часто используемые в популярной медицинской литературе, не кажутся преувеличением тем, кто лично наблюдал исчезновение злокачественных опухолей в собственном теле или в организме своих близких, не сталкиваясь при этом с тяжелейшими побочными эффектами облучения и химиотерапии.Конечно, эти лекарства тоже дают побочные эффекты - от них не свободно ни одно "нарушающее метаболизм" средство. Например, герцептин нацелен на ростовой рецептор HER-2: связывая его, он препятствует неконтролируемому размножению раковых клеток, которое стимулируется избытком копий этого рецептора на их поверхности. Однако нормальные клетки размножаются "как надо" тоже благодаря HER-2-стимуляции, только сравнительно слабой.
А в результате применение герцептина может вызывать смертельно опасную застойную сердечную недостаточность - побочный эффект, который недавние исследования обнаружили также у некоторых пациентов, пользующихся гливеком, который считался в высшей степени безвредным медикаментом - именно потому, что нацелен только на аномальную форму одного из трансдукторов ростовых сигналов.
Аналогичным образом, влияя на устойчивость анергических Т-лимфоцитов к апоптозу, можно было бы стимулировать их "самоубийство", однако остается вопрос: как не погубить попутно нормальные клетки?
Мы сумеем воспользоваться уже применяемой прицельной противораковой терапией (и, очевидно, будущими ее методами, еще находящимися на разных стадиях клинической разработки), создав на этой основе "умные бомбы", разрушающие анергические Т-клетки (и другие типы внутренних врагов, которые мы обсудим позже) с минимальными потерями для здоровых компонентов организма. Можно, например, было бы соединять тщательно подобранные токсины с молекулами, которые избирательно связывались бы с характерными поверхностными белками анергических клонов, в результате непосредственно убивая таких паразитов, а не просто вызывая в них метаболические нарушения.
Свет убивает вампиров
Один из противораковых методов, который можно было адаптировать для уничтожения наших анергетических Т-клеток, - фотодинамическая терапия (ФДТ). Больной получает лекарство, которое при освещении лазером либо сильно разогревается, либо выделяет массу свободных радикалов. Уже известны вещества, обладающие такими свойствами и избирательно поглощаемые раковыми клетками, в результате фотосенсибилизируя их, но, при этом, практически не изменяя свойств нормальных тканей.Эти средства не дают эффекта, пока на них не действует определенное низкоэнергетическое лазерное облучение, которое со своей стороны никак не сказывается на людях, не получавших таких медикаментов: лучи без всякого вреда проходят сквозь их тело. Однако, когда они проникают в клетки, накопившие фотодинамическое лекарство, его свойства приводят к их резкому разогреванию или насыщению свободными радикалами. В результате эти раковые клетки гибнут, а все остальные (не считая находящихся в непосредственной близости) никак не страдают.
Первое ФДТ-средство, Фотофрин, было допущено в развитых странах для лечения далеко зашедшего рака легких, пищеварительного тракта и мочевыводящих путей еще в начале 1990-х. Сейчас используются или находятся в завершающей стадии разработки более совершенные варианты такой терапии.
Самое перспективное из ее средств, Рс-4, избирательно накапливается в определенных типах раковых клеток, поскольку хорошо растворяется в жирах, которыми особенно богаты эти клетки. Проникнув в них, Рс-4 благодаря особенностям своей структуры встраиваются в митохондрии. Последующее лазерное облучение запускает свободнорадикальную бомбежку, которая либо индуцирует апоптоз, либо - в худшем случае - убивает раковые клетки "грязным способом", сшивая их белки, окисляя липидные мембраны, разрушая ДНК мутациями.
Ди Грей Обри
medbe.ru
Как замедлить старение
Наш организм рассчитан на жизнь в 120 лет. Ресурс «отсчитывают» части ДНК – теломеры. То есть, чтобы замедлить процесс старения, достаточно заботиться о состоянии теломер. Как – читайте далее.
Теломеры – это повторяющиеся последовательности ДНК, что находятся на концах хромосом. При каждом делении клетки теломеры укорачиваются. Со временем они совсем «стираются», что приводит к старению клетки, а затем – к ее гибели. Накопление таких клеток в организме повышает риск развития заболеваний. Согласно теории предела Хейфлика, потенциальная продолжительность жизни человека составляет 120 лет. К этому возрасту в организме становится слишком много клеток, не способных делиться и поддерживать его жизнедеятельность.
Фермент теломераза восстанавливает укороченную ДНК. У взрослого человека он почти неактивен. Зато обладает высокой активностью в клетках эмбрионов и злокачественных опухолей.
Почему стресс старит
Многие пагубные для здоровья возрастные изменения организма связаны с укорочением теломер. В первую очередь, это заболевания сердца, ожирение, сахарный диабет и дегенерация хрящевой ткани. Согласно исследованиям, люди с короткими теломерами быстро устают, у них рано появляются морщины и часто возникают простудные заболевания.
Продолжительность жизни напрямую зависит от стресса: чем больше нервничает человек, тем интенсивнее укорачиваются теломеры. Это, в свою очередь, ускоряет биологическое старение клеток. Хронический стресс и депрессия означают плохое состояние теломер, их подверженность преждевременному укорочению. Это является основной причиной того, что стресс старит человека.
Базовое питание для теломер
Восстановить теломеры помогает фермент теломеразы. Активность этого фермента можно активизировать умеренными физическими нагрузками, а также сбалансированным питанием, которое включает витамины и полиненасыщенные жирные кислоты. Тем более, что исследования доказывают, что длина теломер у людей, ведущих правильный образ жизни, значительно больше, чему тех, кто злоупотребляет алкоголем, не следит за своим питанием и весом, ведет малоактивный образ жизни.
Длину теломер можно и нужно поддерживать при помощи питания, поскольку важнейшие процессы не будут проходить, если организме нехватка витаминов В6, В12 и фолиевой кислоты.
Ежедневный рацион должен обязательно включать белки, особенно серосодержащие. Не обойтись без молочных продуктов, яиц, мяса, курицы, бобовых, орехов и зерновых. Яйца особенно важны потому, что являются наиболее богатым источником холина. А для восстановления повреждений в ДНК необходим магний и цинк.
Питание является отличным механизмом для замедления износа организма, если с пищей получать достаточное количество антиоксидантов. Это биологически активные вещества, которые защищают клетки от окисления. Самые известные и доступные антиоксиданты – витамины C и E. Обеспечив организм антиоксидантами, вы не только защищаете клетки и замедляете старение, но и выводите себя из группы рыска по раку.
Использованы фото depositphotos
feelgood.ua
Теломеры – индикатор биологического возраста
Теломеры: можно ли сделать их бессмертными и остановить клеточное старение
Существуют ли способы обнулить счётчик делений клетки и остановить клеточное старение, а значит, и старение организма? В настоящее время учёные всего мира бьются над решением этого вопроса. И определённые сдвиги есть. Так, в 2009 году Нобелевский комитет присудил премию исследователям Калифорнийского университета Кэрол Грейдер, Элизабет Блэкберн и Джеку Шостаку за открытие ими в 1984 году фермента, обеспечивающего наращивание теломеры. Новое органическое вещество белковой природы получило название теломераза. Частица -аза в конце слова указывает на принадлежность к ферментам.
Одиннадцатью годами ранее, в 1973 году, существование особого вещества, способного удлинять концевые участки хромосом, предположил советский биолог, специалист Института Биохимической физики РАН Алексей Матвеевич Оловников.
Теломераза присоединяется к концу ДНК, спрятанному под теломерой, и использует его в качестве стартовой точки для добавления пар нуклеотидов и наращивания концевых участков хромосомы.
К сожалению, активно функционирующий «молодильный» фермент обнаружен лишь в трёх типах клеток человеческого организма: половых, стволовых и раковых. Остальным типам клеток не повезло: ген теломеразы в них прекращает своё функционирование уже в эмбриональный период развития, как бы выключается, и клетка даже не подозревает о его существовании.
Однако наука не стоит на месте. Учёные нашли способ заставить работать омолаживающий клетки фермент и даже встроить его ген в любую клетку. Правда, по понятным причинам массовые эксперименты пока проводились лишь на животных. Заслуживают внимания результаты исследования, организованного в 2012 году специалистами Испанского национального центра по исследованию рака. Двум группам мышей – взрослым и старым – вводили вирус, активизирующий теломеразу. Это позволило значительно увеличить продолжительность их жизни: взрослых животных – на 24 %, старых – на 13 %.
Воодушевлённая такими результатами 44-летняя глава фармкомпании из США Элизабет Пэрриш повторила опыт на себе. Ей вкололи ослабленный аденоассоциированный вирус, в который был предварительно встроен ген теломеразы. Уже спустя 6 месяцев теломеры женщины удлинились на 9 %, что соответствует омоложению тканей на 20 лет.
Однако радоваться рано: безопасность подобных экспериментов ещё не исследована. Чем они могут аукнуться в дальнейшем для здоровья человека и его потомков пока неизвестно. Некоторые специалисты предполагают, что такие опыты на людях могут закончиться увеличением количества онкологических и других смертельно опасных заболеваний. Время покажет. А пока расскажем о безопасных способах удлинить теломеры.
osteomed.su
Фармкомпания из России создает лекарство, которое "затормозит" старение
МОСКВА, 7 ноя – РИА Новости. Петр Белый, директор фармацевтической компании NCPharm, рассказал РИА Новости о том, как его корпорация создает препараты, которые могли бы замедлить или даже остановить процессы старения, и о том, какие проблемы они могут вызвать в обществе и в медицине.
Ученые выяснили, почему оксиданты сокращают жизньРазработка этих лекарств, по словам Белого, напрямую связана с теломерами — концевыми участками хромосом, которые имеются в ядре каждой клетки. Теломеры защищают ДНК от повреждений, и при каждом делении клетки они становятся короче. Когда их длины оказывается недостаточно для нового деления, клетка погибает или перестает делиться, переходя в особый "режим старости".
Подобный процесс происходит только во "взрослых" клетках тела – теломеры у стволовых клеток и в клетках зародышей постоянно обновляются особыми ферментами теломеразами, что позволяет им делиться неограниченное число раз и фактически быть бессмертными. В последние годы ученые активно ищут способы включения этих ферментов и "рычаги" управления их активностью для того, чтобы затормозить или даже остановить процесс старения и массовой гибели и дряхления клеток из-за потери ими способности делиться.
Ученые, возможно, раскрыли секрет самых долгоживущих людей на планетеК примеру, в январе прошлого года биологи из Стэнфордского университета смогли "включить" теломеразы в культуре клеток в пробирке, используя специальные РНК-молекулы, удлинив теломеры примерно на тысячу "букв"-нуклеотидов. Это в некотором роде омолодило клетки и позволило им совершить еще около 30 делений после времени наступления старости.Изображение процесса репликации молекулы РНК
— Расскажите подробно, как именно вы планируете использовать теломеры для борьбы со старостью и ее внешними проявлениями?
— Если вы помните, Нобелевская премия 2009 года была присуждена за открытие, которое на самом деле совершил наш ученый, Алексей Оловников, но вопреки протоколу премию дали не ему, а тем людям, которые подтвердили его теорию и доказали существование теломер и выделили теломеразу как фермент.
Сейчас весь мир работает над тем, чтобы найти какой-то "спусковой механизм", который бы заставил теломеразу работать в соматических клетках тела человека. Почему это важно? Теломераза в естественном виде присутствует или в половых клетках, или в онкологических клетках. Это объясняет, почему из двух половых клеток может вырасти целый организм, и при этом они не становятся престарелыми. То же самое характерно и для раковых клеток – благодаря активным теломеразам они являются фактически бессмертными.
Голые землекопы станут ключом к бессмертию человека, считает биологС другой стороны, "нормальные" клетки могут делиться ограниченное число раз из-за того, что теломеры не обновляются и сокращаются. Соответственно, чем ближе мы к этому пределу и чем больше наше тело содержит престарелых клеток, тем больше риски вырождения и перерождения клеток, развития онкологических заболеваний, снижения иммунитета и всего прочего. Поэтому мы сегодня, как и наши коллеги за рубежом, пытаемся найти такое вещество, которое бы включало бы теломеразы в обычных клетках и заставляло их удлинять теломеры.
Подобная процедура удлинения теломер вызывает множество эффектов в разных органах тела, в том числе омоложение в некоторых тканях организма, которые подвержены естественной возрастной деградации – к примеру, в сетчатке глаза, в хрящевой ткани суставов, в половых железах.
С другой стороны, подобный прием может дать большую отсрочку, может быть даже ремиссию на всю жизнь, например, для носителей ВИЧ. Почему?
Лаборатория, где разрабатывается лекарство для «торможения старости»
— ВИЧ?
— Когда ВИЧ заражает человека, с ним начинают бороться целые "полки" лимфоцитов, тучных клеток, макрофагов и других компонентов иммунной системы. Этот полк появляется не просто так, а в результате деления клеток. В итоге иммуннокомпетентные клетки тела у таких людей исчерпывают пределы деления и становятся "престарелыми". Тогда вирус спокойно выходит и без всякого сопротивления размножается в организме.
С другой стороны, если мы будем искусственно поддерживать длину теломер у таких больных, то понятно, что ВИЧ в таком случае никогда не перейдет в СПИД. Это, конечно, не излечение вируса как такового, но пожизненная ремиссия, которая позволит таким людям жить полноценной жизнью и не умирать от неизлечимого заболевания.
Ученые выяснили, почему зарядка продлевает жизньВ принципе, последствий от того, что мы научимся управлять теломеразами, может быть огромное количество, и их фактически невозможно все перечислить. Что интереснее всего? И наши люди, занимающиеся разработкой таких препаратов, и их западные коллеги говорят, что часы, управляющие ходом нашей жизни, заключаются в другом, они скрыты где-то в структуре мозга. Если мы их откроем, то только тогда мы сможем обратить возраст вспять.
Все это кажется невероятным сегодня, однако так же на теломеры смотрели ученые до 1973 года, когда они были открыты в живых клетках. Этот же ученый говорит, что если мы их откроем и докажем их существование, мы совершим огромный рывок в увеличении продолжительности жизни, здорового молодого возраста.
— Как именно действует на теломеразы препарат, над которым работают ваши специалисты?
— Существует бесчисленное множество путей, которыми мы можем влиять на работу и длину теломер и экспрессию теломераз. Мы взяли и разобрались с тем, как работают препараты, созданные в прошлом американской компанией Geron (ТА-65), одной из первой работавшей над подобными веществами, и поняли, из чего состоит их продукт.
Второе, мы задумались о том, что произойдет, если соединить эти вещества с теми очень небольшими белковыми молекулами, над которыми на протяжении более 30 лет работали наши исследователи. Наши предварительные результаты показывают, что это очень и очень многообещающая комбинация.
Сейчас мы работаем над тем, чтобы провести клинические исследования и разрабатываем систему инъекций, причиняющей минимальные неудобства человеку. Пока, конечно, у нас нет лекарства в готовой инъекционной форме, которую можно было бы показать публике.
Обе части нашего продукта уже проходили или проходят клинические исследования, и мы хотим показать, что их сочетание является большим шагом вперед, и на предварительных данных мы это видим. Здесь, как ни странно, наша наука успела уйти вперед, и то, что Нобелевку 2009 года дали фактически за русское открытие, показывает, что мы здесь что-то действительно имеем.
— Когда будет готов ваш препарат?
— Мы ожидаем, что он будет готов уже в ближайшее время, и что через два-три года мы получим регистрационное удостоверение. Сначала в России, а дальше уже будет сложнее из-за сложной регуляторной системы в США и Европе. В странах с менее строгим контролем все будет протекать гораздо быстрее.
 Скулачев: Нобелевский комитет "забыл" дать премию российскому биологу
Скулачев: Нобелевский комитет "забыл" дать премию российскому биологу — Это будет лекарство или некая форма БАД?
— Вообще мы фармацевтическая компания, и в нашем портфолио более 100 лекарственных средств, у нас есть большой завод, тысячи рабочих, мы производим все виды препаратов. Поэтому история с БАДами для нас является исключением – нам хочется иметь на руках что-то, что мы могли бы использовать, и поэтому нам пришлось пойти таким путем и сделать простую сертификацию, чтобы иметь хотя бы какой-то легальный статус.
Но мы гордимся не этим – мы гордимся тем, что мы ведем реальные исследования и занимаемся доказательной медициной, мы разрабатываем новые формы лекарств, которых пока не применяются на практике. И в данном случае у нас есть очень перспективная медицинская разработка.
— Одной из причин того, почему клетки перестают делиться, является защита от рака. Если мы включим теломеразы, не повысит ли это вероятность развития онкологических заболеваний?
— Это вопрос номер один, который возникает всегда, когда мы обсуждаем последствия от включения теломераз. Здесь нужно понимать, что речь идет об очень небольшом сегменте состояний, когда такое возможно. Обычные клетки с нормальными теломерами не поменяют своей жизнедеятельности в том случае, если их теломеры удлинить. Наоборот, это, скорее всего, омолодит их и сделает их более энергичными.
Ученые: тяготы в детстве сокращают жизнь на клеточном уровнеЕсли клетка уже и так является раковой, то тогда у нее теломеры и так являются длинными, и она сама по себе будет бессмертной и без нашей помощи. Соответственно, у нас есть только те состояния, которые мы можем считать условно опасными – так называемые предраковые клетки, возвращение способности к делению которых может привести к опасным последствиям.Этот вопрос беспокоил не одних нас, и опыты американских ученых показывают, что включение теломераз в таких клетках не приводит к увеличению числа новообразований при приеме того вещества, которое нас интересует. Поэтому мы считаем, что на этот вопрос уже есть ответ на общетеоретическим уровне, но конечно, тесты на онкогенность проводятся и при проверке любого лекарства, и для наших препаратов такие опыты тоже будут проводиться.
Культура раковых клеток в «перенаселенной» пробирке
— Многие перспективные лекарства и вакцины, особенно от ВИЧ и ряда других опасных болезней, часто работают в опытах на грызунах и приматах, но проваливаются в ходе клинических испытаний на добровольцах. Опасаетесь ли вы подобного исхода событий?
— У нас есть основания думать, что наши шансы в данном случае гораздо выше нормы по следующей причине: и тот, и другой компонент нашего препарата уже проверялся на человеке, и эти опыты показали интересные результаты. Мы добиваемся синергетического эффекта в том случае, когда уже есть задокументированные положительные эффекты в испытаниях на людях.
— Как отреагируют на появление таких лекарств представители церкви и различных религиозных конфессий? Совместимы ли подобные препараты с их духовными принципами?
— Если говорить конкретно о теломерах и наших веществах, то он не имеет глубокой философской подоплеки, о которой можно подумать. Скорее, подобные мысли могут возникнуть, если говорить и думать о тех структурах в мозге, которые сейчас пытаются найти ученые и о которых думал Оловников. В тех случаях мы действительно можем говорить о продлении жизни как таковой, на лишние 20-30 лет относительно средней продолжительности жизни человека.
 Длину жизни птицы можно узнать по длине хвостов ее хромосом
Длину жизни птицы можно узнать по длине хвостов ее хромосом Здесь, поскольку теломеры и их длина не являются в строгом смысле часами, отмеряющими наш срок на Земле, мы не можем говорить об этом. Теломеры управляют и являются индикатором не возраста человека в целом, а отдельных функциональных органов и тканей, в основном тех, которые подвержены возрастной деградации.
Соответственно, мы говорим не о том, что мы продлеваем жизнь, а о том, что мы существенно улучшаем качество жизни человека в рамках отмеренного ему срока. Иными словами, человек существенно дольше будет оставаться молодым и здоровым, но к сожалению или счастью, мы не меняем общий срок жизни.
— В последние годы геронтологи активно спорят о том, есть ли какой-то предельный возраст человека, при достижении которого большинство из нас умирает. Насколько возможно перешагнуть через него?
— Пока геронтологи склоняются к тому, что 100-120 лет возраста являются пределом для человека. И пока никто еще не подошел к тому, чтобы увидеть то, что находится за этим рубежом. С другой стороны, мы можем констатировать следующее: за последние 70 лет средняя продолжительность жизни увеличилась на 20 лет.
Ученые из США заключили новое пари о пределах жизни человекаПроизошло это по целому ряду факторов, в том числе и благодаря неожиданным вещам, таким как появление антибиотиков. Тогда никто из нас не думал о том, что простое влияние на жизнь и развитие бактерий может так существенно отразиться на продолжительности жизни человека в целом. Средний возраст в 80 лет сейчас считается чем-то само собой разумеющимся в большинстве развитых и средне-развитых стран. И даже наше правительство сегодня задумывается о том, чтобы увеличить возраст выхода на пенсию.
Соответственно, вопросы, касающиеся долгожителей, затрагивают не только жителей Японии и других регионов с самыми долгоживущими людьми в мире, а всех нас, по крайней мере, тех, кто имеет трехразовое питание и живет более-менее нормально в стране, где есть дороги и электричество. Нам хотя бы нужно адаптироваться к этой реальности, к 80 годам, и только потом думать о ста годах и больше. Мы только сделали большой рывок, но пока не видно биологических механизмов, которые позволили бы выйти на рубеж в 140-150 лет.
Старейшая жительница земли Эмма Морано
ria.ru
















