Содержание
Получение водорода в домашних условиях
Библиографическое описание:
Шапилова, В. В. Получение водорода в домашних условиях / В. В. Шапилова, Г. И. Талапчук. — Текст : непосредственный // Юный ученый. — 2018. — № 1.1 (15.1). — С. 97-98. — URL: https://moluch.ru/young/archive/15/1180/ (дата обращения: 27.12.2022).
На Земле водород в чистом виде почти не встречается, и в повседневной жизни мы с ним не сталкиваемся. Но в соединениях — это второй по количеству атомов элемент в земной коре после кислорода. Все живые существа на Земле, включая нас с вами, примерно на 2/3 состоят из водорода.
Ключевые слова: водород, получение водорода.
Так что же такое водород? Каковы его свойства? Как его получают и применяют в земных условиях? Можно ли получить водород в домашних условиях, и как это делать лучше всего? На эти и другие вопросы мы постараемся ответить в ходе нашей научной работы.
Водород — это самый простой элемент в природе, состоящий из одного протона и вращающегося вокруг него электрона. Впервые получение водорода упоминается у английского учёного Роберта Бойля, который в 1671 году проводил реакцию между железными стружками и разбавленными кислотами. Русское наименование «водород» предложил химик М. Ф. Соловьев в 1824 году — по аналогии с «кислородом» М. В. Ломоносова. Официальное латинское название водорода «Hydrogenium».
В промышленности водород получают в основном из ископаемого топлива. В первую очередь это природный газ, метан, с которым большинство из нас может встретится на кухне, если вас есть газовая плита. Водород получают из лёгких фракций нефти. Третий по популярности источник водорода — это уголь.
Наиболее доступным для повторения в домашних условиях является разложение воды электрическим током (электролиз).
Для проведения нашего эксперимента мы взяли старую зарядку на 5 В 750мА и угольные электроды, извлечённые из обычных солевых батареек.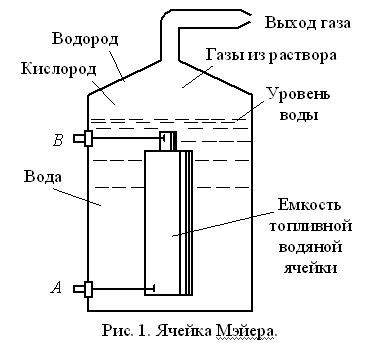 Для измерения протекающего тока использовался мультиметр.
Для измерения протекающего тока использовался мультиметр.
Для сбора и измерения получающихся газов, в бутылки налили воды, и закрепили их на основной ёмкости горлышком вниз, погрузив его при этом в электролит. Таким образом, чтобы воздух в бутылку попадать не смог. Всего в ёмкости и бутылках получилось около 1,5 литров воды. Как и ожидалось, с чистой водой, после подачи напряжения с зарядного устройства ничего не произошло. Мультиметр показывал почти нулевой ток. Но, когда в воду добавили две чайные ложки соды, электролиз пошёл бодрее, на обоих электродах начали появляться пузырьки газа, а мультиметр показал ток 15 мА. С таким маленьким током за сутки (24 часа) удалось собрать только 0,11 литра водорода (примерно полстакана). Во второй бутылке при этом собралось примерно в 2 раза меньше кислорода. Это означает, что в воде водорода в два раза больше, чем кислорода.
Наблюдение выделения водорода в результате взаимодействия металлов с разбавленными кислотами было самых первым в истории химии. И его относительно просто повторить в домашних условиях. Для этого нам понадобится металл, желательно поактивнее и кислота. В нашем эксперименте мы выбрали электролит для свинцовых аккумуляторов, который можно найти в ближайшем автомобильном магазине и цинк из использованных солевых батареек. Для сбора водорода, как и в случае электролиза, использовали перевёрнутую бутылку с опущенным в воду горлышком. Электролит дополнительно развели водой в пропорции 50 мл раствора серной кислоты на 150 мл. воды. Цинка из батарейки получилось примерно 1 г. За 12 часов весь металл растворился и мы получили 0.7 литра водорода.
И его относительно просто повторить в домашних условиях. Для этого нам понадобится металл, желательно поактивнее и кислота. В нашем эксперименте мы выбрали электролит для свинцовых аккумуляторов, который можно найти в ближайшем автомобильном магазине и цинк из использованных солевых батареек. Для сбора водорода, как и в случае электролиза, использовали перевёрнутую бутылку с опущенным в воду горлышком. Электролит дополнительно развели водой в пропорции 50 мл раствора серной кислоты на 150 мл. воды. Цинка из батарейки получилось примерно 1 г. За 12 часов весь металл растворился и мы получили 0.7 литра водорода.
Другой популярный метод — взаимодействие металлов с щелочами. Для эксперимента мы выбрали два варианта, которые были под рукой — кусочки провода и фольгу для запекания. Щёлочь (гидроксид натрия) можно найти в бытовых магазинах как средство для прочистки канализационных труб (КРОТ, например). Установку для получения использовали почти такую же, что и в опыте с кислотой и цинком. Раствор в обоих опытах был одинаковым: 20 мл щёлочи и 200 мл воды. В первом опыте использовали проволоку диаметром 1.5 мм, во втором — кусочки фольги. В обоих случаях масса алюминия была 1 г. В первом опыте удалось получить 1.2 л водорода, заняло это 34 часа. Во втором опыте фольга растворилась за 1 час 20 минут, выделив 1.4 л водорода. Из этих опытов можно сделать вывод, что скорость реакции сильно зависит от площади поверхности, на которой она происходит. В опыте с фольгой площадь поверхности была во много раз выше, чем в опыте с проволокой. Ещё большей скорости можно добиться, если взять алюминий в порошке. В этом случае соотношение площади поверхности к массе будет наибольшим.
Раствор в обоих опытах был одинаковым: 20 мл щёлочи и 200 мл воды. В первом опыте использовали проволоку диаметром 1.5 мм, во втором — кусочки фольги. В обоих случаях масса алюминия была 1 г. В первом опыте удалось получить 1.2 л водорода, заняло это 34 часа. Во втором опыте фольга растворилась за 1 час 20 минут, выделив 1.4 л водорода. Из этих опытов можно сделать вывод, что скорость реакции сильно зависит от площади поверхности, на которой она происходит. В опыте с фольгой площадь поверхности была во много раз выше, чем в опыте с проволокой. Ещё большей скорости можно добиться, если взять алюминий в порошке. В этом случае соотношение площади поверхности к массе будет наибольшим.
Таким образом, в экспериментах по получению водорода наиболее быстрым и доступным способом оказался вариант взаимодействия алюминиевой фольги со щёлочью. Но если необходимо получать водород регулярно и в больших количествах, то на первое место должен выйти электролиз, так как он не требует никаких расходных материалов кроме воды.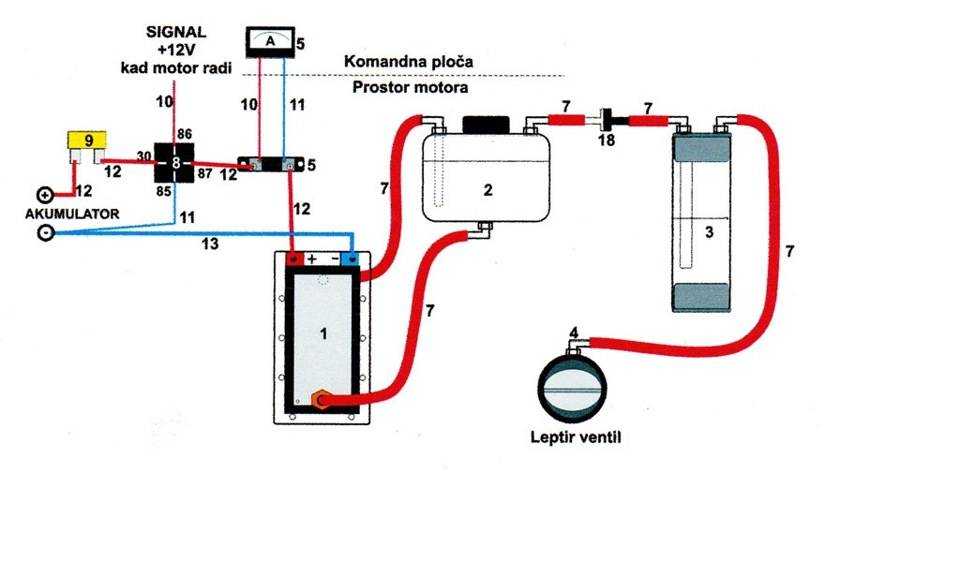 Правда для этого понадобится более серьёзная установка, чем зарядка от телефона и пара бутылок.
Правда для этого понадобится более серьёзная установка, чем зарядка от телефона и пара бутылок.
В ходе научной работы мы познакомились с самым распространённым, но таким редким в быту веществом, как водород. Научились получать его различными способами и выбрали наиболее удобный для осуществления в домашних условиях — воздействие средства для прочистки труб, содержащего щёлочь, на алюминиевую фольгу.
Так же мы на собственном опыте убедились, что водород — горючий и взрывоопасный газ, но им вполне можно наполнять воздушные шарики, чтобы они летали. Правда при этом стоит держать их подальше от открытого огня.
Основные термины (генерируются автоматически): водород, получение водорода, опыт, алюминиевая фольга, научная работа, литр водорода, площадь поверхности.
Из
опыта подготовки исследовательского проекта школьников по…
Известные технологии получения водорода из связанного состояния энергозатратные, дорогие и сложны в эксплуатации [4, с. 8]. Существует необходимость в поиске методов получения водорода из связанного состояния, лишенных перечисленных недостатков.
8]. Существует необходимость в поиске методов получения водорода из связанного состояния, лишенных перечисленных недостатков.
Водород — топливо будущего? | Статья в журнале…
Получение водорода методом электролиза неэффективно с энергетической точки зрения, количество затраченной на это энергии значительно превышает количество энергии, содержащейся в водороде. Процесс получения водорода из ископаемых видов топлива…
Исследование методов
получения водорода в соответствии…
Говоря о водороде как о экологически чистом топливе будущего, считается, что его производство не наносит вреда окружающей среде.
Настоящая работа направлена на исследование способов получения водорода в соответствии с принципами «зелёной химии».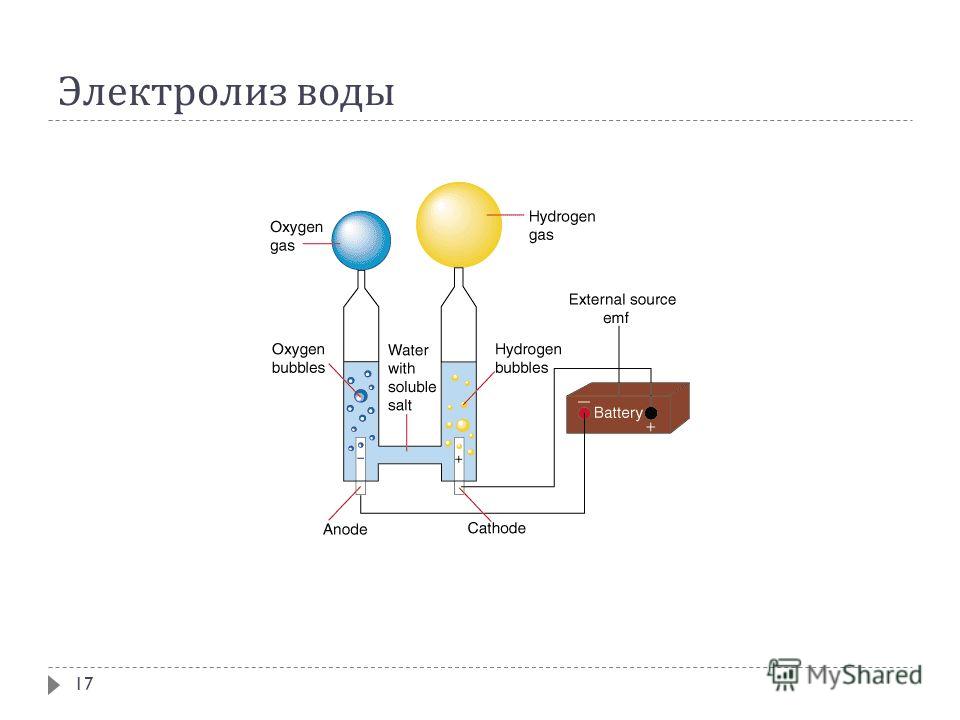
Создание технологий
водородной энергетики | Статья в журнале…
Введение. Понятие — «водородная энергетика» сформировалось в середине 70-х г. XX столетия. Водородную энергетику можно определить, как научно техническое направление, охватывающее проблемы получения, хранения, транспортировки и использования водорода.
Краткий обзор опытно-конструкторских
работ по использованию…
При подаче водорода соответственно уменьшалось количество бензина в смеси. Как видно, добавка водорода при неизменной энергии
2. Трелин Ю. А. Исследование особенностей работы ДВС с искровым зажиганием при добавках водорода в бензовоздушную смесь: дисс…
К вопросу применения
водорода на двигателях внутреннего. ..
..
Первое практическое использование водорода в качестве добавки к топливу для авиационных ДВС относится к 1927г. В Советском Союзе работы по применению Н2 в качестве топлива для ДВС проводятся в секторе неоднородных средств АН СССР под руководством академика В.В…
Особенности топливных систем двигателей, работающих на…
Получение водорода разложением воды в многоступенчатых термохимических циклах на транспортных энергоустановках практически невозможно из-за высоких и различных на разных ступенях температур (до 450-9000С) и использования большого количества цветных металлов.
Технология очистки отходящих газов высокоамперных…
Технология улавливания фтористого водорода в системе сухой газоочистки основана на способности глинозема поглощать фтористый водород. В реакторе-адсорбере в режиме аэровзвеси, происходит процесс соединения фтористого водорода с оксидом алюминия [2]
Анализ условий самовоспламенения сжатого
водорода. Обзор
Обзор
Проведен обзор работ за последние 15 лет по проблеме водородной безопасности. Приведены условия, при которых происходит самовоспламенение струи водорода, истекающей под высоким давлением в воздух. Показано, что воспламенение водорода возможно даже при…
Водород из воды: просто и дешево
Тема дня
Главная
Наука
08 июля, 2005, 00:00
Распечатать
Выпуск № 26, 8 июля-15 июля 2005г.
Российский исследователь сконструировал электролизер, позволяющий получать водород из воды, затрачивая на это очень мало энергии…
ЗЕРКАЛО НЕДЕЛИ, УКРАИНА
Архив номеров
|
Последние статьи<
>Как отжать миллиард долларов — мастер-класс от бондхолдеров Приватбанка
К чему Лондонский арбитраж, если есть Киевская «хозяйка»?
Опрос читателейАвторЮлия Самаева
Статья
26 декабря 17:00
Четыре мифа о новых правилах конкурса в Конституционный суд Украины
В рамках продолжения дискуссии
Опрос читателейАвторДенис Маслов
Статья
26 декабря 13:00
Замглавы комитета ВРУ по экономразвитию Дмитрий Кисилевский: «Задача государства — за десять лет достичь 20% доли перерабатывающей промышленности в ВВП»
С 2007-го доля переработки в ВВП сократилась с 18 до 10%
Опрос читателейАвторРоман Ивченко
Статья
26 декабря 08:30
«Гонения» и война Московского патриархата в Украине
АвторЕкатерина Щеткина
Статья
25 декабря 17:00
Банкам пора признать неработающие кредиты, НБУ — создавать новую политику
Кризис реально решить переговорами с заемщиками
Опрос читателейАвторЕлена Граждан
Статья
25 декабря 13:00
«НотаЕнота»: развенчиваем мифы и фейки со школьной скамьи
Быть эрудированным, умным, сообразительным — круто, легко, интересно
АвторАлла Котляр
Статья
25 декабря 08:30
- Вам также будет интересно
>
«Дизайнерские дети»: за и против
14.
 12 17:02
12 17:02Украинская наука — как оценивать?
12.12 17:00
Национальный фонд исследований Украины: впечатления от четырехлетней деятельности
03.12 13:13
Как поддержать украинскую науку и украинских ученых
10.11 13:00
Открытая наука — второй шанс для украинской научной системы?
Опрос читателей
26. 10 13:00
10 13:00Не просто победа Украины: зачем нужна научно-техническая деградация России
Опрос читателей
23.10 08:30Аномальные температуры: будет ли зима холодной
Инфографика
Опрос читателей
15.10 08:30Куда приглашают украинских ученых во время войны
Опрос читателей
30. 08 13:05
08 13:05Харьковских школьников встретили невероятными аплодисментами на международном турнире. Почему и как это было?
08.08 13:00
Наука может стать локомотивом, который вытащит Украину из экономической пропасти
Инфографика
Опрос читателей
06.08 13:40Как оценивать украинскую науку: четыре важные вещи
Опрос читателей
02. 08 13:00
08 13:00В чем нуждаются украинские научные работники во время войны и что они могут дать стране?
Опрос читателей
31.07 13:00
Последние новости
Украина вышла из одного из соглашений СНГ о пенсиях: как это повлияет на выплаты
17:39
Россия стягивает к Кременной огромное количество военных — Гайдай
17:21
СБУ передала в Харьковский музей колокол из уничтоженного российскими захватчиками храма в Купянске
17:17
«Океан Ельзи» опубликовал видео выступления Вакарчука на Антоновском мосту
17:16
К украинской электросети подключили два блока ТЭС – Шмыгаль
17:08
Все новости
Добро пожаловать!
Регистрация
Восстановление пароля
Авторизуйтесь, чтобы иметь возможность комментировать материалы
Зарегистрируйтесь, чтобы иметь возможность комментировать материалы
Введите адрес электронной почты, на который была произведена регистрация и на него будет выслан пароль
Забыли пароль?
Войти
Пароль может содержать большие и маленькие буквы латинского алфавита, а также цифры
Введенный e-mail содержит ошибки
Зарегистрироваться
Имя и фамилия должны состоять из букв латинского алфавита или кирилицы
Введенный e-mail содержит ошибки
Данный e-mail уже существует
У поля Имя и фамилия нет ошибок
У поля E-mail нет ошибок
Напомнить пароль
Введенный e-mail содержит ошибки
Нет учетной записи? Зарегистрируйтесь!
Уже зарегистрированы? Войдите!
Нет учетной записи? Зарегистрируйтесь!
}
Химия для детей — Как разделить воду на водород и кислород с помощью электролиза
Нам всем говорили, что вода состоит из водорода и кислорода.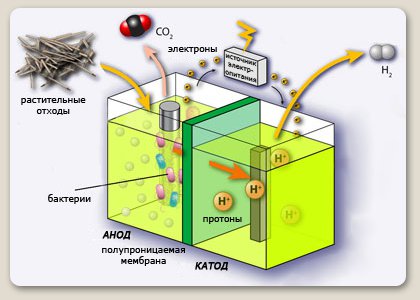 Но как мы действительно знаем это? Может ли это влажное вещество, утоляющее нашу жажду и охлаждающее наши тела в жаркие летние дни, действительно состоять из двух газов ?
Но как мы действительно знаем это? Может ли это влажное вещество, утоляющее нашу жажду и охлаждающее наши тела в жаркие летние дни, действительно состоять из двух газов ?
Мы пытались разделить воду на кислород и водород с помощью электролиза. Нам удалось это сделать после серии экспериментов, которые оставили у нас еще больше вопросов, чем до того, как мы начали. Что не обязательно плохо — любопытство — отличное состояние обучения! (см. таинственный случай отсутствия кислорода, ниже.)
Вы можете воспользоваться нашими ошибками и провести электролиз быстрым способом. Вот как можно разделить воду на водород и кислород с помощью электролиза. Потом я расскажу вам о том, что мы сделали сначала, что произвело совсем другой газ.
Как разделить воду на водород и кислород
Что вам понадобится
- стеклянная или пластиковая ванна
- 2 резинки
- 2 пробирки (по возможности с крышками)
- двууглекислая сода (1 ст.
 л.)
л.) - графитовые грифели
- вода
- (мы использовали 6В, примерно как эта)
- 2 пары зажимов типа «крокодил»
- водонепроницаемая лента
Батарейка
Аппарат для электролиза
Чем вы занимаетесь
Подробные инструкции по установке смотрите в этом видео – расположение эластичных лент идеально удерживает пробирки на месте.
Если вы не можете посмотреть видео, вот его суть: Подсоедините один конец каждого зажима-крокодила к кусочку графита, а другой к батарее. Прикрепите концы графита ко дну ванны так, чтобы графит торчал вверх, и поместите перевернутую пробирку на каждый кусок графита (удерживаемый эластичными лентами). Растворите бикарбонат соды в воде и наполните ванну. Наконец, выньте каждую пробирку, наполните ее водой и осторожно поставьте на графит. Любые газы, собранные во время электролиза, заменят воду в трубках, поэтому убедитесь, что нет пузырьков воздуха.
Что происходит
На каждом электроде быстро начинают образовываться пузырьки газа. На отрицательном электроде (катоде) собирается больше газа, чем на положительном (аноде).
На отрицательном электроде (катоде) собирается больше газа, чем на положительном (аноде).
Как проверить свои газы
Когда вы соберете достаточное количество газа на каждом электроде, осторожно закройте пробирки крышками (пока они находятся под водой).
Для проверки на водород
Мы предположили, что газ на нашем (отрицательном) катоде был (положительно заряженным) водородом. Водород взрывоопасен. В таких количествах он не разрушит ваш дом, но будет издавать прохладный хлопающий звук в присутствии зажженной щепки. Вы можете услышать это в видео ниже.
Для проверки на кислород
Мы проверяем на кислород с помощью светящейся шины. Если кислорода достаточно, шина воспламеняется. Газ, который мы собрали на нашем аноде, дал кратковременное свечение, которое подтвердило, что это кислород, но после возбуждения от взрыва водорода мы были немного разочарованы. Позже мы произвели намного больше кислорода, используя другой метод — см. ниже видео о нашей повторно зажженной шине.
Если кислорода достаточно, шина воспламеняется. Газ, который мы собрали на нашем аноде, дал кратковременное свечение, которое подтвердило, что это кислород, но после возбуждения от взрыва водорода мы были немного разочарованы. Позже мы произвели намного больше кислорода, используя другой метод — см. ниже видео о нашей повторно зажженной шине.
Как работает электролиз?
Вода представляет собой ковалентную молекулу (h30), удерживаемую общими электронами в ковалентных связях.
Во время электролиза молекулы восстанавливаются на катоде до газообразного водорода и окисляются на аноде до газообразного кислорода.
Чистая вода не проводит электричество, поэтому нам нужно добавить электролит, например двууглекислую соду. (Вы не поверите, сколько веб-сайтов советуют использовать соль. Мы попробовали и получили совершенно другой газ. Подробнее об этом позже.)
Производится вдвое больше водорода, чем кислорода, что отражает молекулярный состав вода.
Credit – J Squish
Вот довольно простое объяснение электролиза воды.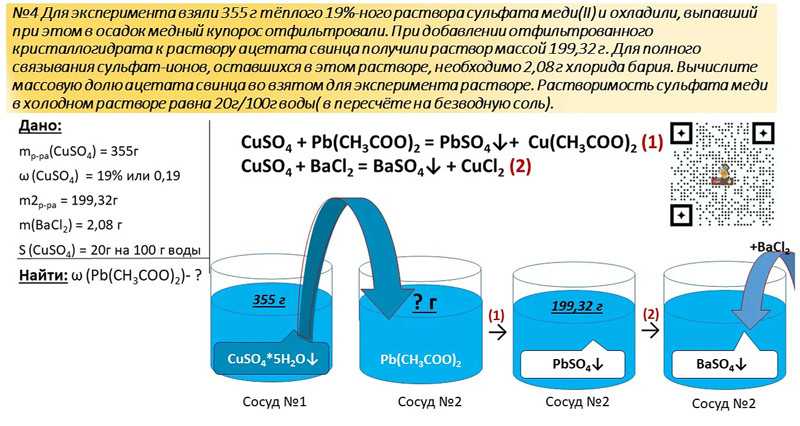
Если вам нужно более подробное объяснение, см. Википедию.
{Большое спасибо, Сара, за то, что указали на мое прежнее недоразумение и сделали этот пост более точным!}
Загадочный случай отсутствия кислорода
(Или что происходит, когда вы используете соль в качестве электролита.)
Прежде чем мы успешно разделили воду на водород и кислород, используя описанный выше метод, мы пытались добавить соль, чтобы помочь нашей воде проводить электричество. И не только щепотку соли. Я решил, что если немного соли немного поможет, то много соли будет еще лучше. (В конце концов, это работает для кристаллов.)
Мы проводим наш электролиз, используя тот же аппарат, что и выше, но на этот раз с насыщенным раствором соли. И вот мы сидели, жадно выискивая наши пузыри водорода и кислорода.
Что случилось? Ну, много на нашем катоде. Газ быстро начал заполнять пробирку. Мы протестировали его и обнаружили, что это водород. А на положительном электроде? Ни единого пузырька газа! Что случилось с кислородом из наших молекул воды?
Ночью я провел небольшое исследование.
Похоже, что во время электролиза раствора хлорида натрия (соли) хлорид натрия распадается на положительном электроде с образованием газообразного хлора и раствора гидроксида натрия. (Нажмите на ссылку, чтобы получить более подробное объяснение.) Хлор легко растворяется в воде, поэтому не будет собираться в виде газа, пока раствор не станет насыщенным и не сможет больше поглощать хлор.
Итак, если наш положительный электрод был занят притяжением хлора, а на катоде собирался водород… что случилось с кислородом? Или в натрий из нашего хлорида натрия (NaCl), если уж на то пошло? По словам химиков, натрий и кислород объединяются, образуя раствор гидроксида натрия. Требовалось дальнейшее расследование.
Мы оставили наш аппарат настроенным — отключенным от батареи — на ночь. Мы решили изучить его на наличие зацепок.
Дальнейшие исследования
Какие изменения произошли в результате электролиза?
Наш солевой раствор приобрел коричневатый цвет. Был ли это растворенный хлор? Сломанный графит? Проржавел зажим-крокодил (который был прикреплен к аноду)?
Был ли это растворенный хлор? Сломанный графит? Проржавел зажим-крокодил (который был прикреплен к аноду)?
Изменения в результате электролиза
Фильтрация раствора .
Часть нашего положительного электрода (анода) сломалась, оставив в растворе черные частицы. Мы используем графит в электролизе, потому что это инертный (нереакционноспособный) металл, но, возможно, большое количество произведенного нами хлора вызвало его реакцию? Мы отфильтровали коричневый раствор, чтобы увидеть, остались ли какие-либо нерастворимые частицы. Они этого не сделали. Но мы заметили несколько белых пятен на фильтровальной бумаге — должно быть, хлор, образующийся на нашем положительном электроде, обесцветил бумагу!
Отбеленная фильтровальная бумагаПосле электролиза наш раствор был слегка кислым
Тестирование рН раствора
Мы предположили, что раствор будет слегка щелочным из-за гидроксида натрия. Но когда мы проверили его, мы обнаружили обратное. Он был слегка кислым — как хлор. Мы предположили, что это означает, что раствор должен содержать больше хлора, чем гидроксида.
Мы предположили, что это означает, что раствор должен содержать больше хлора, чем гидроксида.
Больше удовольствия от кислорода
Здесь я немного отклоняюсь от темы, но обещал рассказать, как мы создали достаточное количество кислорода, чтобы успешно протестировать его. Идея пришла к нам после перехода к 9 0007 Магия кислорода Шоу в Королевском институте. Я хотел бы поделиться с вами одной из демонстраций, которые мы там видели.
Ведущие спросили, могут ли они одолжить у меня купюру в 10 фунтов, а потом подожгли ее! Вот видео моих пылающих денег.
Невредимая банкнота номиналом 10 фунтов стерлингов
Магия кислорода Ученые также продемонстрировали, как сделать «зубную пасту для слонов», расщепляя перекись водорода. Мы вспомнили, как когда-то сами делали зубную пасту для слонов. Когда мы вернулись домой, мы решили снова сделать зубную пасту для слонов и использовать светящуюся шину для проверки на кислород.
Мы вспомнили, как когда-то сами делали зубную пасту для слонов. Когда мы вернулись домой, мы решили снова сделать зубную пасту для слонов и использовать светящуюся шину для проверки на кислород.
Изготовление зубной пасты для слонов
Когда вы помещаете светящуюся шину в кислород, она снова загорается.
Почему это мой любимый способ заниматься наукой на дому
Как вы понимаете, это была не та демонстрация науки на дому, где мама точно знает, что произойдет и почему. Я изучал химию до шестнадцати лет – почти тридцать лет назад! Я не знал ответов на многие вопросы, возникающие в результате этих экспериментов.
Я изучал химию до шестнадцати лет – почти тридцать лет назад! Я не знал ответов на многие вопросы, возникающие в результате этих экспериментов.
Но незнание того, что произойдет, вызвало у меня любопытство и вдохновило узнать больше, а дети определенно были увлечены моим волнением. И я рад, что мы совершили «ошибку», использовав сначала соль в качестве электролита, потому что иначе мы упустили бы очень интересную науку!
Занимались ли вы в последнее время какой-нибудь интересной наукой?
Вы когда-нибудь расследовали случай отсутствия кислорода?
***
С благодарностью присоединяюсь сюда:
Итоги недели – Странные несоциализированные домашние школьники
Пятница с коллажами – Доморощенные ученики Adventures in Mommydom
Finishing Strong — начинается в восемь
The Hip Homeschool Hop — Hip Homeschool Moms
Метод изготовления кислорода из воды в нулевой гравитации повышает надежду на расстояние космических поездок
Поделиться на Facebook
Share на Twitter
Share на Reddit
Поделиться по электронной почте
Распечатать
Share Share On SintininInIin3
.
Художественный рендеринг марсохода с искусственной гравитацией. Предоставлено: NASA
Следующее эссе перепечатано с разрешения The Conversation, интернет-издания, посвященного последним исследованиям.
Космические агентства и частные компании уже разработали планы по отправке людей на Марс в ближайшие несколько лет и, в конечном счете, его колонизации. А с растущим числом открытий похожих на Землю планет вокруг ближайших звезд дальние космические путешествия никогда не казались более захватывающими.
Однако людям нелегко выживать в космосе в течение продолжительных периодов времени. Одной из главных проблем дальних космических полетов является транспортировка достаточного количества кислорода для дыхания астронавтов и достаточного количества топлива для питания сложной электроники. К сожалению, в космосе мало кислорода, а большие расстояния затрудняют быстрое восполнение запасов.
Но теперь новое исследование, опубликованное в Nature Communications, показывает, что можно производить водород (для топлива) и кислород (для жизни) только из воды, используя полупроводниковый материал и солнечный свет (или звездный свет) в невесомости, что делает устойчивые космические путешествия — реальная возможность.
Использование неограниченных ресурсов солнца для обеспечения энергией нашей повседневной жизни является одной из самых больших проблем на Земле. Поскольку мы медленно уходим от нефти к возобновляемым источникам энергии, исследователей интересует возможность использования водорода в качестве топлива. Лучший способ сделать это — разделить воду (h3O) на составляющие: водород и кислород. Это возможно с помощью процесса, известного как электролиз, который включает пропускание тока через образец воды, содержащий некоторое количество растворимого электролита. Это расщепляет воду на кислород и водород, которые выделяются отдельно на двух электродах.
Хотя этот метод технически возможен, он еще не стал доступным на Земле, поскольку нам нужно больше инфраструктуры, связанной с водородом, такой как станции заправки водородом, чтобы масштабировать его.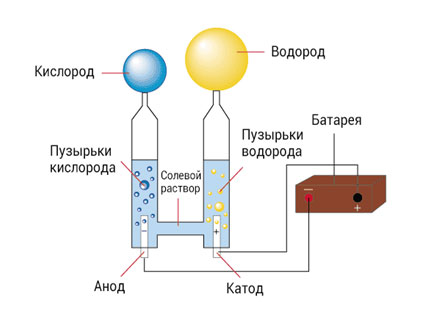
Солнечная энергия
Водород и кислород, полученные таким образом из воды , также могут использоваться в качестве топлива на космических кораблях. Запуск ракеты с водой на самом деле был бы намного безопаснее, чем запуск с дополнительным ракетным топливом и кислородом на борту, которые могут быть взрывоопасными. Оказавшись в космосе, специальная технология сможет расщепить воду на водород и кислород, которые, в свою очередь, можно будет использовать для поддержания жизни или для питания электроники с помощью топливных элементов.
Это можно сделать двумя способами. Один из них включает электролиз, как мы делаем на Земле, с использованием электролитов и солнечных элементов , чтобы улавливать солнечный свет и преобразовывать его в ток.
Альтернативой является использование «фотокатализаторов», которые работают, поглощая частицы света — фотоны — полупроводниковым материалом, помещенным в воду. Энергия фотона поглощается электроном в материале, который затем прыгает, оставляя после себя дыру.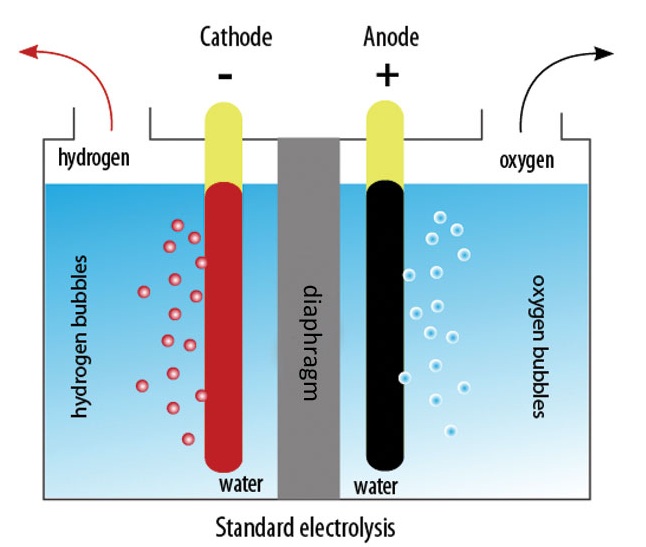 Свободный электрон может реагировать с протонами (которые вместе с нейтронами составляют атомное ядро) в воде с образованием водорода. Между тем, дырка может поглощать электроны из воды с образованием протонов и кислорода.
Свободный электрон может реагировать с протонами (которые вместе с нейтронами составляют атомное ядро) в воде с образованием водорода. Между тем, дырка может поглощать электроны из воды с образованием протонов и кислорода.
Процесс также может быть обратным. Водород и кислород можно объединить или «рекомбинировать» с помощью топливного элемента, возвращая солнечную энергию, полученную в результате «фотокатализа» — энергию, которую можно использовать для питания электроники. В результате рекомбинации в качестве продукта образуется только вода, а это означает, что вода также может быть использована повторно. Это ключ к дальним космическим путешествиям.
Процесс с использованием фотокатализаторов – лучший вариант для космических полетов, так как вес оборудования намного меньше, чем для электролиза. По идее должно работать легко. Отчасти это связано с тем, что интенсивность солнечного света намного выше, а атмосфера Земли не поглощает его в больших количествах на пути к поверхности.
Управление пузырьками
В новом исследовании исследователи сбросили полную экспериментальную установку для фотокатализа в 120-метровую башню, создав среду, подобную микрогравитации. По мере того, как объекты ускоряются к Земле в свободном падении, эффект гравитации уменьшается, поскольку силы, действующие под действием гравитации, уравновешиваются равными и противоположными силами из-за ускорения. Это противоположно перегрузкам, которые испытывают космонавты и летчики-истребители, когда они разгоняются в своих самолетах.
Исследователям удалось показать, что в этой среде действительно возможно разделить воду. Однако, когда вода расщепляется с образованием газа, образуются пузырьки. Избавление от пузырьков из когда-то образовавшегося материала катализатора важно, так как пузырьки мешают процессу образования газа. На Земле гравитация заставляет пузырьки автоматически всплывать на поверхность (вода у поверхности плотнее пузырьков, что делает их гибкими), освобождая место на катализаторе для образования следующего пузыря.
В условиях невесомости это невозможно, и пузырек останется на катализаторе или рядом с ним. Однако ученые скорректировали форму наночастиц в катализаторе, создав пирамидальные зоны, в которых пузырек мог легко отделиться от кончика и уплыть в среду.
Но остается одна проблема. В отсутствие гравитации пузырьки останутся в жидкости, даже если они были вытеснены из самого катализатора. Гравитация позволяет газам легко выходить из жидкости, что очень важно для использования чистого водорода и кислорода. Без гравитации никакие пузырьки газа не всплывают на поверхность и не отделяются от смеси — вместо этого весь газ остается для создания пены.
Это резко снижает эффективность процесса из-за блокировки катализаторов или электродов. Инженерные решения этой проблемы будут иметь ключевое значение для успешного внедрения технологий в космосе, причем одной из возможностей будет использование центробежных сил от вращения космического корабля для отделения газов от раствора.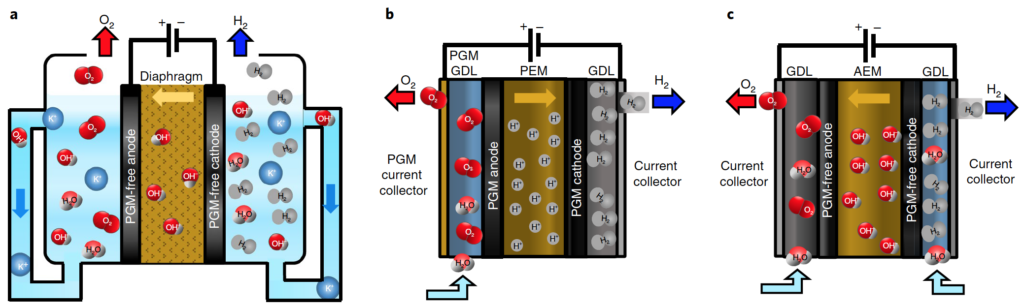

 12 17:02
12 17:02 10 13:00
10 13:00 08 13:05
08 13:05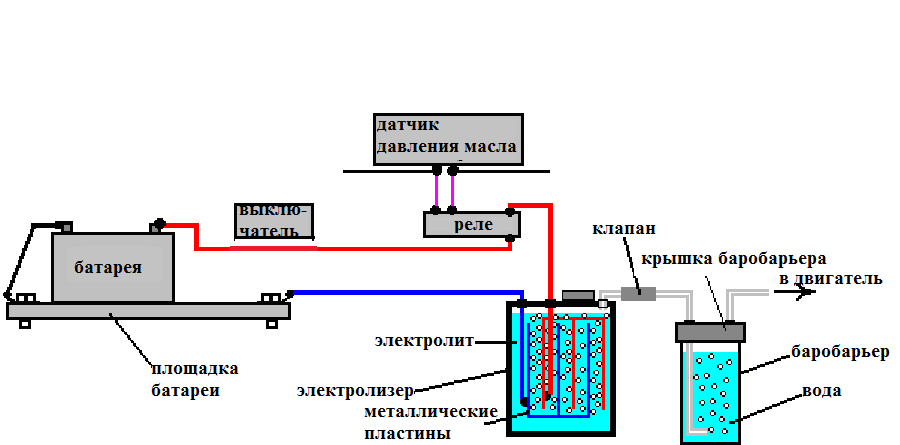 08 13:00
08 13:00.jpg) л.)
л.)