Содержание
Российские ученые разработали высокочувствительный «электронный нос» для определения свежести продуктов
8 июня, 2021 12:51
Источник:
Пресс-служба РНФ
Российские ученые разработали первый в мире «электронный нос», чувствительный сразу к нескольким токсичным газам. Полученные сенсоры не требуют большой мощности батареи, стабильны при высокой влажности и способны распознать наличие всего 30 молекул диоксида азота или этилмеркаптана, обеспечивающего «запах газа», среди миллиарда молекул азота и кислорода, из которых состоит воздух. Такие устройства помогут отслеживать состояние окружающей среды, регулировать работу промышленных предприятий и оценивать свежесть скоропортящейся еды. С результатами работы можно ознакомиться в журнале Scientifc Reports. Проект поддержан грантом Российского научного фонда (РНФ).
Поделиться
Токсичные газы, такие как оксиды азота, сероводород, меркаптаны и аммиак, представляют большой интерес для исследователей, поскольку связаны с загрязнением воздуха промышленными предприятиями и двигателями внутреннего сгорания. В то же время, обнаруженные в выдыхаемом воздухе человека, эти соединения могут быть маркерами ряда опасных заболеваний. Например, у пациентов с астмой концентрация оксида азота в выдыхаемом воздухе возрастает с приближением приступа. Компактное устройство, детектирующее этот газ предупредит больного и позволит вовремя принять лекарства. Кроме того, продукты питания при порче выделяют аммиак и сероводород, сенсоры к которым можно интегрировать в холодильники или «умную» упаковку. С помощью такого «электронного носа» можно будет легко определить, какие продукты еще можно безопасно употреблять, уменьшив количество выброшенных свежих продуктов, а какие уже пора списывать, что снизит частоту пищевых отравлений.
Крайне перспективными для этого класса задач сегодня считаются газовые сенсоры на основе тонких пленок органических полупроводников. Когда на эти пленки попадают молекулы токсичного газа, их электрические свойства немного изменяются. Чтобы регистрировать слабые сигналы с пленок, ученые собрали из них специальную систему, называемую транзистором. Она позволяет усилить сигнал и зарегистрировать малейшие концентрации токсичного газа.
Сенсоры на основе транзисторов обычно плохо отличают разные молекулы и нестабильны, особенно во влажном воздухе, что затрудняет их использование. Для решения этой проблемы ученые из Института синтетических полимерных материалов имени Н. С. Ениколопова РАН (Москва) решили объединить несколько различных сенсоров в массив и обрабатывать приходящие с него сигналы методами машинного обучения. Такой подход имитирует работу обоняния млекопитающих, где множество сенсоров выполняет функцию обонятельного эпителия с большим количеством разных рецепторов, а машинное обучение — роль обонятельной коры в мозге. Именно поэтому изобретение назвали «электронным носом».
Именно поэтому изобретение назвали «электронным носом».
«Ранее наш коллектив разработал способ управления чувствительностью таких сенсоров к отдельным газам, а в данной работе мы смогли объединить большое количество датчиков на одном чипе и продемонстрировали электронную систему на основе органических транзисторов, работающую как обоняние», — сообщил руководитель гранта РНФ Сергей Пономаренко, доктор химических наук, директор и заведующий лабораторией функциональных материалов для органической электроники и фотоники ИСПМ РАН.
Ученые покрыли синтезированные в ИСПМ РАН пленки дополнительными рецепторными слоями. Эти слои содержали вещества, называемые металлопорфиринами, в которые включены ионы металлов. Прямоугольный чип с 20 сенсорами последовательно окунали в три различных раствора с модифицирующими соединениями. Это позволило объединить на малой площади четыре группы сенсоров, которые по-разному реагировали на исследованные газы. Далее электрические сигналы от каждой из этих групп анализировали методами машинного обучения с целью обнаружить характерные «отпечатки», свойственные определенным газам. Именно разница в откликах нескольких групп сенсоров позволила различать между собой диоксид азота, сероводород, этилмеркаптан и аммиак. Чувствительность полученного анализатора позволяет обнаружить всего несколько десятков молекул серо- и азотсодержащих газов среди миллиарда молекул окружающего воздуха.
Далее электрические сигналы от каждой из этих групп анализировали методами машинного обучения с целью обнаружить характерные «отпечатки», свойственные определенным газам. Именно разница в откликах нескольких групп сенсоров позволила различать между собой диоксид азота, сероводород, этилмеркаптан и аммиак. Чувствительность полученного анализатора позволяет обнаружить всего несколько десятков молекул серо- и азотсодержащих газов среди миллиарда молекул окружающего воздуха.
Фото датчика вместе с чипом. Монетка для масштаба. Источник: Сергей Пономаренко
На основе такого массива сенсоров ученые создали прототип портативного устройства для испытаний без использования дорогостоящего и массивного лабораторного оборудования. Прибор интерпретировал сигналы с чувствительных слоев и выводил информацию об обнаруженных газах и их концентрациях конечному пользователю. Поскольку при порче мясных продуктов выделяются летучие производные сероводорода и аммиака, формирующие неприятный запах, ученые решили проверить собранную установку на практике. Для этого исследователи установили сенсор на крышку пищевого контейнера с сырым мясом и следили за изменением сигнала. Уже на десятом часу хранения уровень сигнала позволил сказать о том, что мясо испорчено.
Для этого исследователи установили сенсор на крышку пищевого контейнера с сырым мясом и следили за изменением сигнала. Уже на десятом часу хранения уровень сигнала позволил сказать о том, что мясо испорчено.
Благодаря низкой стоимости и малому энергопотреблению, большое количество таких датчиков, объединенных в «умную» сеть, можно будет использовать в современных городах и на промышленных предприятиях для своевременного обнаружения выбросов опасных газов в атмосферу и точной локализации их источника.
«Предложенный подход по конструированию массива сенсоров позволит собирать высокоспецифичные наборы рецепторных слоев для различных задач. В работе мы продемонстрировали одно из таких применений — портативное устройство для определения свежести мяса. Мы надеемся, что в будущем наша технология позволит создавать «умные» холодильники или целые комнаты хранения продуктов», — отметил первый автор статьи Даниил Анисимов, младший научный сотрудник ИСПМ РАН.
На следующем шаге ученые планируют создать компактную станцию контроля качества воздуха для «умных» городов и испытать ее в Москве, а также доработать и апробировать «электронный нос» в качестве портативного прибора ранней диагностики воспалительных заболеваний легких. Сейчас вторы оптимизируют производственные процессы и собирают новые данные для более точной классификации различных газов методами машинного обучения.
Сейчас вторы оптимизируют производственные процессы и собирают новые данные для более точной классификации различных газов методами машинного обучения.
Теги
Пресс-релизы
Ученые создали электронный нос-долгожитель — РИА Новости, 25.07.2018
https://ria.ru/20180419/1518957945.html
Ученые создали электронный нос-долгожитель
Ученые создали электронный нос-долгожитель — РИА Новости, 25.07.2018
Ученые создали электронный нос-долгожитель
Ученые Саратовского государственного технического университета имени Гагарина Ю.А. совместно с коллегами Технологического института Карлсруэ (Германия) и… РИА Новости, 19.04.2018
2018-04-19T10:03
2018-04-19T10:03
2018-07-25T16:39
/html/head/meta[@name=’og:title’]/@content
/html/head/meta[@name=’og:description’]/@content
https://cdnn21.img.ria.ru/images/sharing/article/1518957945.jpg?15088463121532525992
РИА Новости
1
5
4. 7
7
96
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
2018
РИА Новости
1
5
4.7
96
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
Новости
ru-RU
https://ria.ru/docs/about/copyright.html
https://xn--c1acbl2abdlkab1og.xn--p1ai/
РИА Новости
1
5
4.7
96
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
РИА Новости
1
5
4.7
96
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
РИА Новости
1
5
4.7
96
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og. xn--p1ai/awards/
xn--p1ai/awards/
саратовский государственный технический университет имени гагарина ю.а. (сгту имени гагарина ю.а.), университетская наука
Наука, Саратовский государственный технический университет имени Гагарина Ю.А. (СГТУ имени Гагарина Ю.А.), Университетская наука
МОСКВА, 19 апр – РИА Новости. Ученые Саратовского государственного технического университета имени Гагарина Ю.А. совместно с коллегами Технологического института Карлсруэ (Германия) и Университета «Манас» (Киргизия) разработали эффективный способ обучения электронных носов. Результаты исследования опубликованы в «Sensors».
Электронные носы – компактные устройства для распознавания запаха широкого класса химических веществ. В отличие от простых датчиков газов, они могут не только различать смеси, но и запоминать новые запахи благодаря обучению с помощью систем искусственного интеллекта.
Уже 30 лет ученые пытаются создать эффективно работающие электронные носы. Базовая идея состоит в том, чтобы не определять, какие молекулы запаха появляются в воздухе, а просто взять набор газовых сенсоров, которые реагируют на появление определенных примесей в воздухе. А дальше используется «искусственный интеллект» – компьютер учится распознавать конкретные запахи.
А дальше используется «искусственный интеллект» – компьютер учится распознавать конкретные запахи.
20 сентября 2017, 11:42
Физики из России создали электронный «нос» из титановых нанотрубок
Обучение электронного носа похоже на тренировку поисковых собак: компьютеру, оборудованному сенсорами, показывается нужный запах, который закрепляется его обозначением. Представим, что сенсор направлен на поиск в атмосфере запаха розы. Компьютер запоминает, какой у розы «образ» и впоследствии отличает ее, например, от аромата квашеной капусты.
Но, в отличие от биологической системы обоняния, электронный нос, при помещении в реальные условия, когда в окружающей атмосфере возникает много неконтролируемых примесей, начинает «путаться» буквально через несколько дней. Ученые, часто имеющие дело с газовыми сенсорами, конечно, знают в чем дело.
«Дело в том, что сенсоры нестабильны и их показания дрейфуют со временем, – поясняет один из авторов, профессор кафедры «Физика» СГТУ имени Гагарина Ю. А. Виктор Сысоев. – Потому нужны стабильные сенсоры, избегающие дрейфа. Мы продемонстрировали, как подойти к этой проблеме на примере электронного носа, основанного на мультисенсорной матрице из оксида металла».
А. Виктор Сысоев. – Потому нужны стабильные сенсоры, избегающие дрейфа. Мы продемонстрировали, как подойти к этой проблеме на примере электронного носа, основанного на мультисенсорной матрице из оксида металла».
В Саратовском государственном техническом университете имени Гагарина Ю.А. были разработаны стабильные высокочувствительные сенсоры на основе монокристаллических нановолокон. Но, оказалось, что электронные носы на их основе могут безошибочно распознавать запахи лишь неделю-другую, а потом требуют перекалибровки.
Поэтому специалисты Саратовского государственного технического университета имени Гагарина Ю.А. попытались посмотреть на эту проблему с другой стороны. Речь идет о быстром алгоритме перекалибровки сенсоров с возможностью тонкой подстройки по ходу работы прибора.
«Мы выяснили, что стабильность электронного носа зависит в основном от случайных изменений состава окружающего воздуха, а ввод процедуры дообучения носа обеспечивает его стабильность на протяжении многих лет, – добавляет Виктор Сысоев. – Более того, мы впервые доказали способность прибора функционировать более восьми лет, – никто еще не демонстрировал такой долгой и успешной работы искусственных носов».
– Более того, мы впервые доказали способность прибора функционировать более восьми лет, – никто еще не демонстрировал такой долгой и успешной работы искусственных носов».
Для реализации и проверки идеи в Технологическом Институте Карлсруэ был установлен «демонстратор» электронного носа, который тщательно откалибровали (в течение двух недель) на воздействие трех «запахов»: зажигалки, фломастера и «чистого» воздуха. Потом устройство стали «дообучать» согласно развитому алгоритму. То есть, если поднести к электронному носу лежащий неподалеку фломастер, сенсоры распознают его запах и автоматически используют полученные данные для своей подстройки к текущему состоянию воздуха. Эта система безошибочно работает с 2009 года.
Данная разработка имеет большое значение для практиков, так как на ее основе может быть создан «идеальный» электронный нос, являющийся стабильным и простым техническим инструментом для анализа состава газовых сред.
Российские ученые создали «электронный нос» для определения свежести продуктов — Газета.
 Ru
Ru
Российские ученые создали «электронный нос» для определения свежести продуктов — Газета.Ru | Новости
«Тампа» отстранила обладателя Кубка Стэнли из-за скандала с сексуальными…
05:10
Евросоюз стал применять новый подход к санкциям в отношении России
05:09
«Я бы съел индейца»: соперники раскопали каннибалистическое высказывание…
05:07
Дочь Марка Захарова обжалует решение суда в споре с театром «Ленком»
04:53
Мама Кокорина уверена, что игрок сможет перезапустить карьеру
04:50
В Ливане заявили о вхождении сторожевого катера ВМС Израиля…
04:42
Экс-посол Украины вышел из себя из-за каверзного вопроса о сыне и ВСУ
04:35
Хавбек «Спартака» Умяров сравнил одноклубника Соболева с форвардом…
04:30
Певцу SHAMAN посоветовали выпускать больше песен
04:25
Погибшая при подрыве Крымского моста пара из Петербурга снимала фильм…
04:17
Наука
close
100%
Российские ученые разработали первый в мире «электронный нос», чувствительный сразу к нескольким токсичным газам. Полученные сенсоры не требуют большой мощности батареи, стабильны при высокой влажности и способны распознать наличие всего 30 молекул диоксида азота или этилмеркаптана, обеспечивающего «запах газа», среди миллиарда молекул азота и кислорода, из которых состоит воздух. Такие устройства помогут отслеживать состояние окружающей среды, регулировать работу промышленных предприятий и оценивать свежесть скоропортящейся еды. С результатами работы можно ознакомиться в журнале Scientifc Reports. Проект поддержан грантом Российского научного фонда (РНФ).
Полученные сенсоры не требуют большой мощности батареи, стабильны при высокой влажности и способны распознать наличие всего 30 молекул диоксида азота или этилмеркаптана, обеспечивающего «запах газа», среди миллиарда молекул азота и кислорода, из которых состоит воздух. Такие устройства помогут отслеживать состояние окружающей среды, регулировать работу промышленных предприятий и оценивать свежесть скоропортящейся еды. С результатами работы можно ознакомиться в журнале Scientifc Reports. Проект поддержан грантом Российского научного фонда (РНФ).
Токсичные газы, такие как оксиды азота, сероводород, меркаптаны и аммиак, представляют большой интерес для исследователей, поскольку связаны с загрязнением воздуха промышленными предприятиями и двигателями внутреннего сгорания. В то же время, обнаруженные в выдыхаемом воздухе человека, эти соединения могут быть маркерами ряда опасных заболеваний. Например, у пациентов с астмой концентрация оксида азота в выдыхаемом воздухе возрастает с приближением приступа. Компактное устройство, детектирующее этот газ предупредит больного и позволит вовремя принять лекарства. Кроме того, продукты питания при порче выделяют аммиак и сероводород, сенсоры к которым можно интегрировать в холодильники или «умную» упаковку. С помощью такого «электронного носа» можно будет легко определить, какие продукты еще можно безопасно употреблять, уменьшив количество выброшенных свежих продуктов, а какие уже пора списывать, что снизит частоту пищевых отравлений.
Компактное устройство, детектирующее этот газ предупредит больного и позволит вовремя принять лекарства. Кроме того, продукты питания при порче выделяют аммиак и сероводород, сенсоры к которым можно интегрировать в холодильники или «умную» упаковку. С помощью такого «электронного носа» можно будет легко определить, какие продукты еще можно безопасно употреблять, уменьшив количество выброшенных свежих продуктов, а какие уже пора списывать, что снизит частоту пищевых отравлений.
Крайне перспективными для этого класса задач сегодня считаются газовые сенсоры на основе тонких пленок органических полупроводников. Когда на эти пленки попадают молекулы токсичного газа, их электрические свойства немного изменяются. Чтобы регистрировать слабые сигналы с пленок, ученые собрали из них специальную систему, называемую транзистором. Она позволяет усилить сигнал и зарегистрировать малейшие концентрации токсичного газа.
Сенсоры на основе транзисторов обычно плохо отличают разные молекулы и нестабильны, особенно во влажном воздухе, что затрудняет их использование. Для решения этой проблемы ученые из Института синтетических полимерных материалов имени Н. С. Ениколопова РАН (Москва) решили объединить несколько различных сенсоров в массив и обрабатывать приходящие с него сигналы методами машинного обучения. Такой подход имитирует работу обоняния млекопитающих, где множество сенсоров выполняет функцию обонятельного эпителия с большим количеством разных рецепторов, а машинное обучение — роль обонятельной коры в мозге. Именно поэтому изобретение назвали «электронным носом».
Для решения этой проблемы ученые из Института синтетических полимерных материалов имени Н. С. Ениколопова РАН (Москва) решили объединить несколько различных сенсоров в массив и обрабатывать приходящие с него сигналы методами машинного обучения. Такой подход имитирует работу обоняния млекопитающих, где множество сенсоров выполняет функцию обонятельного эпителия с большим количеством разных рецепторов, а машинное обучение — роль обонятельной коры в мозге. Именно поэтому изобретение назвали «электронным носом».
«Ранее наш коллектив разработал способ управления чувствительностью таких сенсоров к отдельным газам, а в данной работе мы смогли объединить большое количество датчиков на одном чипе и продемонстрировали электронную систему на основе органических транзисторов, работающую как обоняние», — сообщил руководитель гранта РНФ Сергей Пономаренко, доктор химических наук, директор и заведующий лабораторией функциональных материалов для органической электроники и фотоники ИСПМ РАН.
Ученые покрыли синтезированные в ИСПМ РАН пленки дополнительными рецепторными слоями. Эти слои содержали вещества, называемые металлопорфиринами, в которые включены ионы металлов. Прямоугольный чип с 20 сенсорами последовательно окунали в три различных раствора с модифицирующими соединениями. Это позволило объединить на малой площади четыре группы сенсоров, которые по-разному реагировали на исследованные газы. Далее электрические сигналы от каждой из этих групп анализировали методами машинного обучения с целью обнаружить характерные «отпечатки», свойственные определенным газам. Именно разница в откликах нескольких групп сенсоров позволила различать между собой диоксид азота, сероводород, этилмеркаптан и аммиак. Чувствительность полученного анализатора позволяет обнаружить всего несколько десятков молекул серо- и азотсодержащих газов среди миллиарда молекул окружающего воздуха.
Эти слои содержали вещества, называемые металлопорфиринами, в которые включены ионы металлов. Прямоугольный чип с 20 сенсорами последовательно окунали в три различных раствора с модифицирующими соединениями. Это позволило объединить на малой площади четыре группы сенсоров, которые по-разному реагировали на исследованные газы. Далее электрические сигналы от каждой из этих групп анализировали методами машинного обучения с целью обнаружить характерные «отпечатки», свойственные определенным газам. Именно разница в откликах нескольких групп сенсоров позволила различать между собой диоксид азота, сероводород, этилмеркаптан и аммиак. Чувствительность полученного анализатора позволяет обнаружить всего несколько десятков молекул серо- и азотсодержащих газов среди миллиарда молекул окружающего воздуха.
На основе такого массива сенсоров ученые создали прототип портативного устройства для испытаний без использования дорогостоящего и массивного лабораторного оборудования. Прибор интерпретировал сигналы с чувствительных слоев и выводил информацию об обнаруженных газах и их концентрациях конечному пользователю. Поскольку при порче мясных продуктов выделяются летучие производные сероводорода и аммиака, формирующие неприятный запах, ученые решили проверить собранную установку на практике. Для этого исследователи установили сенсор на крышку пищевого контейнера с сырым мясом и следили за изменением сигнала. Уже на десятом часу хранения уровень сигнала позволил сказать о том, что мясо испорчено.
Поскольку при порче мясных продуктов выделяются летучие производные сероводорода и аммиака, формирующие неприятный запах, ученые решили проверить собранную установку на практике. Для этого исследователи установили сенсор на крышку пищевого контейнера с сырым мясом и следили за изменением сигнала. Уже на десятом часу хранения уровень сигнала позволил сказать о том, что мясо испорчено.
Благодаря низкой стоимости и малому энергопотреблению, большое количество таких датчиков, объединенных в «умную» сеть, можно будет использовать в современных городах и на промышленных предприятиях для своевременного обнаружения выбросов опасных газов в атмосферу и точной локализации их источника.
«Предложенный подход по конструированию массива сенсоров позволит собирать высокоспецифичные наборы рецепторных слоев для различных задач. В работе мы продемонстрировали одно из таких применений — портативное устройство для определения свежести мяса. Мы надеемся, что в будущем наша технология позволит создавать «умные» холодильники или целые комнаты хранения продуктов», — отметил первый автор статьи Даниил Анисимов, младший научный сотрудник ИСПМ РАН.
На следующем шаге ученые планируют создать компактную станцию контроля качества воздуха для «умных» городов и испытать ее в Москве, а также доработать и апробировать «электронный нос» в качестве портативного прибора ранней диагностики воспалительных заболеваний легких. Сейчас вторы оптимизируют производственные процессы и собирают новые данные для более точной классификации различных газов методами машинного обучения.
Подписывайтесь на «Газету.Ru» в Новостях, Дзен и Telegram.
Чтобы сообщить об ошибке, выделите текст и нажмите Ctrl+Enter
Новости
Дзен
Telegram
Картина дня
«Это акт терроризма». Бастрыкин доложил Путину о взрыве на Крымском мосту
Путин: авторы, исполнители и заказчики теракта на Крымском мосту — спецслужбы Украины
Турция собирает саммит стран Запада и РФ по Украине. В Кремле об этом ничего не известно
Турция предложила переговоры в Стамбуле по ситуации на Украине между РФ и США с союзниками
Украина получит от США ракеты GMLRS. Что это изменит для российских военных
Что войдет в новый пакет военной помощи ВСУ от США
Медведев: ответом на теракт на Крымском мосту может быть только уничтожение террористов
Стремоусов: на Андреевском направлении взяты в плен офицеры военной разведки Украины
«Ведомости»: магазины «Иль де Ботэ» возобновляют работу в России вместо Sephora
Медведев заявил о «стандартном раздолбайстве» при мобилизации в России
Новости и материалы
«Тампа» отстранила обладателя Кубка Стэнли из-за скандала с сексуальными домогательствами
Евросоюз стал применять новый подход к санкциям в отношении России
«Я бы съел индейца»: соперники раскопали каннибалистическое высказывание Болсонару
Дочь Марка Захарова обжалует решение суда в споре с театром «Ленком»
Мама Кокорина уверена, что игрок сможет перезапустить карьеру
В Ливане заявили о вхождении сторожевого катера ВМС Израиля в территориальные воды страны
Экс-посол Украины вышел из себя из-за каверзного вопроса о сыне и ВСУ
Хавбек «Спартака» Умяров сравнил одноклубника Соболева с форвардом «Манчестер Сити» Холандом
Певцу SHAMAN посоветовали выпускать больше песен
Погибшая при подрыве Крымского моста пара из Петербурга снимала фильм о Романовых
Источник: у Роналду нет конфликта с тренером «Манчестер Юнайтед» тен Хагом
На Кубе почтили память Че Гевары в 55-ю годовщину его гибели
В Китае предрекли крах американской гегемонии
Шахматистка Горячкина назвала любимую фигуристку
Власти Запорожской области сообщили об ударах в подконтрольном Украине Запорожье
В ЦКБ «Рубин» раскрыли подробности о российской атомной подлодке будущего
Численность серых китов в Северной Америке сокращается последние два года
Тренер «Ростова» Карпин сравнил быстрый гол от «Краснодара» с ушатом холодной воды
Все новости
Военная операция России на Украине. День 228-й
День 228-й
Онлайн-трансляция военной спецоперации РФ на Украине — 228-й день
Крысы, шум и горы мусора: почему нью-йоркцы выступают против веранд ресторанов
В Нью-Йорке отказались закрыть веранды ресторанов, несмотря на требования жителей
«Еды и выпивки на столах не будет». Интервью с Валдисом Пельшем о шоу «Поем на кухне всей страной»
Валдис Пельш рассказал о самых необычных участниках шоу «Поем на кухне всей страной»
«Клуб полуночников» — сериал, где подростки из хосписа пугают друг друга в ожидании смерти
Рецензия на сериал «Клуб полуночников» от автора «Призраков дома на холме» Майка Флэнагана
«Освобождение от колониальных соглашений». Как закончился экономический саботаж на Сахалине
Экономист Крутаков объяснил, как создание нового оператора проекта «Сахалин-1» помогло защитить российские активы
Дальнобойщик и гиды. Кто погиб при взрыве на Крымском мосту
Стало известно о заказчике и водителе взорвавшейся на Крымском мосту фуры
Лучшие фотографии недели
Как происходит транспортное сообщение после взрыва на Крымском мосту
Песков: президент Путин проведет оперативное совещание с Совбезом РФ 10 октября
«Красные линии обозначены». В МИДе назвали границы, которые нельзя переступать Украине и Западу
В МИДе заявили, что поставки дальнобойных вооружений Украине станут «красной линией» для РФ
«Нерушимое братство» отменено: Киргизия отказалась проводить учения ОДКБ
В Минобороны Киргизии сообщили, что учения «Нерушимое братство» в рамках ОДКБ отменены
«Носферату, симфонии ужаса» — 100 лет. 5 фактов о первом вампирском фильме в истории
Вдова автора «Дракулы» пыталась уничтожить все копии картины, но не преуспела
«Риторика США была глупой». Трамп рассказал, что повлияло на решение Путина начать спецоперацию
Экс-президент США Трамп призвал Россию и Украину незамедлительно начать мирные переговоры
«Переправа стабильно работает». Что сейчас с Крымским мостом
The New York Times: взрыв на Крымском мосту организовали спецслужбы Украины
Алена Солнцева
Вещи на память
О неохоте к перемене мест
Ольга Васильева
Малыш и гаджет
О том, как смартфоны влияют на развитие и образование детей
Мария Дегтерева
Щас спою
О том, можно ли запрещать украинские песни
Анастасия Миронова
Готовы нa фронт, но от пирогов нa ночь откaзaться не могут
О том, почему у нac столько добровольцев с ожирением, диaбетом и гипертонией
Марина Ярдаева
К станку, не отходя от колыбели
О том, что такое самореализация в декрете
—>
Читайте также
Найдена ошибка?
Закрыть
Спасибо за ваше сообщение, мы скоро все поправим.
Продолжить чтение
Познакомьтесь с электронным носом, который действительно нюхает
Я работаю отоларингологом более двух десятков лет. Мои пациенты говорят мне, что хотят более естественного звучания, большего удовольствия от музыки и, прежде всего, лучшего понимания речи, особенно в условиях фонового шума — так называемого
проблема коктейльной вечеринки. В течение 15 лет моя команда из Геттингенского университета в Германии сотрудничала с коллегами из Фрайбургского университета и других университетов, чтобы заново изобрести кохлеарный имплант поразительно нелогичным способом: с использованием света.
Мы понимаем, что современные кохлеарные импланты наталкиваются на жесткие ограничения техники и физиологии человека. Поэтому мы разрабатываем кохлеарный имплант нового типа, в котором используются излучатели света и генетически измененные клетки, реагирующие на свет. Используя точные лучи света вместо электрического тока для стимуляции кохлеарного нерва, мы ожидаем, что наши оптические кохлеарные имплантаты будут лучше воспроизводить полный спектральный характер звуков и лучше имитировать естественный слух. Мы стремимся начать клинические испытания в 2026 году, и, если все пойдет хорошо, мы можем получить одобрение регулирующих органов на наше устройство в начале следующего десятилетия. Тогда люди во всем мире могли начать слышать свет.
Используя точные лучи света вместо электрического тока для стимуляции кохлеарного нерва, мы ожидаем, что наши оптические кохлеарные имплантаты будут лучше воспроизводить полный спектральный характер звуков и лучше имитировать естественный слух. Мы стремимся начать клинические испытания в 2026 году, и, если все пойдет хорошо, мы можем получить одобрение регулирующих органов на наше устройство в начале следующего десятилетия. Тогда люди во всем мире могли начать слышать свет.
На этих трехмерных микроскопических изображениях анатомии уха мыши видны оптические имплантаты [пунктирные линии], проходящие через сложную структуру нормальной улитки, которая содержит волосковые клетки; при глухоте эти клетки утрачиваются или повреждаются. Слева волосковые клетки [голубая спираль] соединяются с кохлеарными нервными клетками [синие нити и точки]. На среднем и правом изображениях костяной корпус улитки мыши окружает это тонкое устройство. ..»> Даниэль Кеппелер
Как работают кохлеарные импланты
Немного
По данным Всемирной организации здравоохранения, 466 миллионов человек во всем мире страдают от инвалидизирующей потери слуха, требующей вмешательства. Потеря слуха в основном возникает в результате повреждения улитки, вызванного болезнью, шумом или возрастом, и до сих пор неизлечимо. Слух можно частично восстановить с помощью слуховых аппаратов, которые, по сути, передают усиленную версию звука оставшимся сенсорным волосковым клеткам улитки. Люди с глубокими нарушениями слуха получают больше пользы от кохлеарных имплантатов, которые, как упоминалось выше, пропускают дисфункциональные или потерянные волосковые клетки и непосредственно стимулируют кохлеарный, или слуховой, нерв.
В 2030-х годах люди во всем мире смогут начать слышать свет.
Сегодняшние кохлеарные имплантаты являются наиболее успешными нейропротезами на сегодняшний день. Первое устройство было одобрено Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США в 1980-х годах.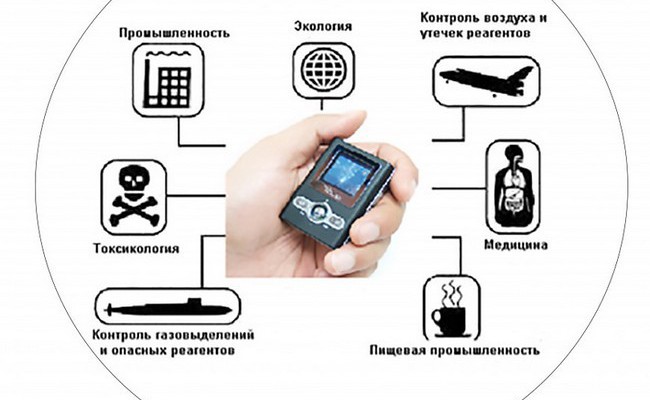
к 2019 году во всем мире было имплантировано почти 737 000 устройств. Тем не менее, они ограниченно используют нейроны, доступные для кодирования звука в улитке. Чтобы понять почему, сначала нужно понять, как работает естественный слух.
В функционирующем человеческом ухе звуковые волны направляются в слуховой проход и приводят в движение барабанную перепонку, которая, в свою очередь, вызывает вибрацию крошечных косточек в среднем ухе. Эти кости передают вибрации на улитку внутреннего уха, структуру в форме улитки размером с горошину. Внутри заполненной жидкостью улитки мембрана колеблется в ответ на звуковые вибрации, и эти рябь перемещают пучки сенсорных волосковых клеток, которые выступают с поверхности этой мембраны. Эти движения заставляют волосковые клетки высвобождать нейротрансмиттеры, которые вызывают электрический сигнал в нейронах кохлеарного нерва. Все эти электрические сигналы кодируют звук, и сигнал проходит по нерву в мозг. Независимо от того, какую звуковую частоту они кодируют, кохлеарные нейроны представляют интенсивность звука скоростью и синхронизацией своих электрических сигналов: частота срабатывания может достигать нескольких сотен герц, а синхронизация может достигать точности до миллисекунды.
Волосковые клетки в разных частях улитки реагируют на разные частоты звука: клетки в основании спиралевидной улитки обнаруживают высокие звуки частотой примерно до 20 кГц, а клетки в верхней части спирали — низкие. звучит примерно до 20 Гц. Эта частотная карта улитки также доступна на уровне нейронов, которые можно рассматривать как спиралевидный массив приемников. Кохлеарные имплантаты извлекают выгоду из этой структуры, стимулируя нейроны в основании улитки, чтобы создать восприятие высокого тона и так далее.
Коммерческий кохлеарный имплант сегодня имеет микрофон, процессор и передатчик, которые носят на голове, а также приемник и имплантированные электроды. Обычно он имеет от 12 до 24 электродов, которые вставляются в улитку для непосредственной стимуляции нерва в разных точках. Но солевой раствор внутри улитки является проводящим, поэтому ток от каждого электрода распространяется и вызывает широкую активацию нейронов по частотной карте улитки. Поскольку частотная избирательность электрической стимуляции ограничена, качество искусственного слуха также ограничено. Естественный процесс слуха, при котором волосковые клетки воздействуют на определенные точки улиткового нерва, можно представить себе как игру пальцами на пианино; кохлеарные импланты больше похожи на игру с кулаками. Хуже того, это большое перекрытие стимуляции ограничивает способ стимуляции слухового нерва, поскольку заставляет нас активировать только один электрод за раз.
Естественный процесс слуха, при котором волосковые клетки воздействуют на определенные точки улиткового нерва, можно представить себе как игру пальцами на пианино; кохлеарные импланты больше похожи на игру с кулаками. Хуже того, это большое перекрытие стимуляции ограничивает способ стимуляции слухового нерва, поскольку заставляет нас активировать только один электрод за раз.
Как работает оптогенетика
Идея лучшего способа возникла еще в 2005 году, когда я начал слышать о новой методике, впервые примененной в неврологии, под названием
оптогенетика. Немецкие исследователи одними из первых обнаружили в водорослях светочувствительные белки, регулирующие поток ионов через клеточную мембрану. Затем другие исследовательские группы начали экспериментировать, беря гены, кодирующие такие белки, и используя безвредный вирусный вектор для встраивания их в нейроны. В результате облучение этих генетически измененных нейронов могло заставить их открыть потенциалзависимые ионные каналы и, таким образом, сработать или активироваться, что позволило исследователям напрямую контролировать мозг и поведение живых животных. С тех пор оптогенетика стала важным инструментом в исследованиях в области неврологии, и клиницисты экспериментируют с медицинскими приложениями, включая восстановление зрения и кардиостимуляцию.
С тех пор оптогенетика стала важным инструментом в исследованиях в области неврологии, и клиницисты экспериментируют с медицинскими приложениями, включая восстановление зрения и кардиостимуляцию.
Меня давно интересовало, как кодируется звук и как это кодирование нарушается при нарушениях слуха. Мне пришло в голову, что стимуляция улиткового нерва светом вместо электричества могла бы обеспечить гораздо более точный контроль, потому что свет можно точно сфокусировать даже в солевой среде улитки.
Мы предлагаем новый тип имплантируемого медицинского устройства, который будет сочетаться с новым типом генной терапии.
Если бы мы использовали оптогенетику, чтобы сделать кохлеарные нервные клетки чувствительными к свету, мы могли бы точно поражать эти цели лучами низкоэнергетического света, чтобы производить гораздо более тонкие слуховые ощущения, чем с электрическим имплантатом. Теоретически мы могли бы иметь более чем в пять раз больше целей, разнесенных по всей улитке, возможно, 64 или 128. Звуковые стимулы можно было бы электронным способом разделить на множество дискретных частотных диапазонов, что дало бы пользователям гораздо более богатый опыт звука. Эта общая идея была подхвачена ранее
Звуковые стимулы можно было бы электронным способом разделить на множество дискретных частотных диапазонов, что дало бы пользователям гораздо более богатый опыт звука. Эта общая идея была подхвачена ранее
Клаус-Питер Рихтер из Северо-Западного университета, который предложил прямую стимуляцию слухового нерва высокоэнергетическим инфракрасным светом, хотя эта концепция не была подтверждена другими лабораториями.
Наша идея была захватывающей, но мы с коллегами увидели множество проблем. Мы предлагали новый тип имплантируемого медицинского устройства, которое будет сочетаться с новым типом генной терапии, оба из которых должны соответствовать самым высоким стандартам безопасности. Нам нужно определить лучший источник света для использования в оптогенетической системе и как передать его в нужные точки в улитке. Нам нужно было найти правильный светочувствительный белок для использования в клетках улитки, и мы должны были выяснить, как лучше всего доставить гены, кодирующие эти белки, в нужные части улитки.
Но за эти годы мы добились большого прогресса. В 2015 году Европейский исследовательский совет выразил нам вотум доверия, когда
профинансировал наш проект OptoHear, а в 2019 году мы выделили компанию под названием OptoGenTech для работы над коммерциализацией нашего устройства.
Каналродопсины, микросветодиоды и волоконная оптика
Наши ранние эксперименты по проверке концепции на мышах исследовали как биологию, так и технологию, задействованную в нашей миссии. Поиск подходящего светочувствительного белка, или каналородопсина, оказался долгим процессом. Многие ранние попытки оптогенетики использовали
канал родопсин-2 (ChR2), который открывает ионный канал в ответ на синий свет. Мы использовали его в экспериментальном эксперименте на мышах, который продемонстрировал, что оптогенетическая стимуляция слухового пути обеспечивает лучшую частотную избирательность, чем электрическая стимуляция.
В нашем продолжающемся поиске лучшего канального родопсина для нашей цели мы попробовали вариант ChR2, названный
кальций-транслокирующий каналродопсин (CatCh) из лаборатории биофизики Института Макса Планка Эрнста Бамберга, одного из пионеров оптогенетики в мире. Мы доставили CatCh в кохлеарные нейроны монгольских песчанок, используя безвредный вирус в качестве вектора. Затем мы обучили песчанок реагировать на слуховой раздражитель, научив их избегать определенной области, когда они слышали звук. Затем мы оглушили песчанок, применив лекарство, убивающее волосковые клетки, и вставили крошечный оптический кохлеарный имплант, чтобы стимулировать чувствительные к свету нейроны улитки. Глухие животные реагировали на это световое раздражение так же, как и на слуховой раздражитель.
Мы доставили CatCh в кохлеарные нейроны монгольских песчанок, используя безвредный вирус в качестве вектора. Затем мы обучили песчанок реагировать на слуховой раздражитель, научив их избегать определенной области, когда они слышали звук. Затем мы оглушили песчанок, применив лекарство, убивающее волосковые клетки, и вставили крошечный оптический кохлеарный имплант, чтобы стимулировать чувствительные к свету нейроны улитки. Глухие животные реагировали на это световое раздражение так же, как и на слуховой раздражитель.
Оптический кохлеарный имплант позволит людям различать голоса на оживленных собраниях и ценить тонкости любимых песен.
Однако использование CatCh имеет две проблемы: во-первых, требуется синий свет, связанный с
фототоксичность. Когда свет, особенно высокоэнергетический синий свет, падает прямо на клетки, которые обычно находятся в темноте внутри тела, эти клетки могут быть повреждены и в конечном итоге отмирают. Другая проблема с CatCh заключается в том, что он медленно перезагружается. При температуре тела, когда CatCh активируется светом, требуется около дюжины миллисекунд, чтобы закрыть канал и быть готовым к следующей активации. Такая медленная кинетика не поддерживает точное время активации нейронов, необходимое для кодирования звука, для которого может потребоваться более сотни импульсов в секунду. Многие люди говорили, что кинетика каналородопсинов делает наши поиски невозможными — что даже если мы получим спектральное разрешение, мы потеряем временное разрешение. Но мы восприняли эти сомнения как сильную мотивацию для поиска более быстрых канальных родопсинов, которые реагируют на красный свет.
При температуре тела, когда CatCh активируется светом, требуется около дюжины миллисекунд, чтобы закрыть канал и быть готовым к следующей активации. Такая медленная кинетика не поддерживает точное время активации нейронов, необходимое для кодирования звука, для которого может потребоваться более сотни импульсов в секунду. Многие люди говорили, что кинетика каналородопсинов делает наши поиски невозможными — что даже если мы получим спектральное разрешение, мы потеряем временное разрешение. Но мы восприняли эти сомнения как сильную мотивацию для поиска более быстрых канальных родопсинов, которые реагируют на красный свет.
Мы были взволнованы, когда лидер в области оптогенетики,
Эдвард Бойден из Массачусетского технологического института открыл более быстродействующий канальный родопсин, который его команда назвала Хроносом. Хотя для активации по-прежнему требовался синий свет, Chronos был самым быстрым канальным родопсином на сегодняшний день: для закрытия при комнатной температуре требовалось около 3,6 миллисекунд. Более того, мы обнаружили, что он закрылся примерно за 1 мс при более высокой температуре тела. Однако потребовались некоторые дополнительные приемы, чтобы заставить Chronos работать в улитке: нам пришлось использовать мощные вирусные векторы и определенные генетические последовательности, чтобы улучшить доставку белка Chronos к клеточной мембране нейронов улитки. С помощью этих трюков как отдельные нейроны, так и популяция нейронов реагировали надежно и с хорошей временной точностью на оптическую стимуляцию с более высокой частотой, примерно до 250 Гц. Таким образом, Хронос позволил нам получить почти естественную частоту возбуждения нейронов, предполагая, что мы можем иметь как частотное, так и временное разрешение. Но нам все еще нужно было найти сверхбыстрый канальный родопсин, работающий с более длинноволновым светом.
Более того, мы обнаружили, что он закрылся примерно за 1 мс при более высокой температуре тела. Однако потребовались некоторые дополнительные приемы, чтобы заставить Chronos работать в улитке: нам пришлось использовать мощные вирусные векторы и определенные генетические последовательности, чтобы улучшить доставку белка Chronos к клеточной мембране нейронов улитки. С помощью этих трюков как отдельные нейроны, так и популяция нейронов реагировали надежно и с хорошей временной точностью на оптическую стимуляцию с более высокой частотой, примерно до 250 Гц. Таким образом, Хронос позволил нам получить почти естественную частоту возбуждения нейронов, предполагая, что мы можем иметь как частотное, так и временное разрешение. Но нам все еще нужно было найти сверхбыстрый канальный родопсин, работающий с более длинноволновым светом.
Мы объединились с Бамбергом, чтобы принять вызов. Сотрудничество было нацелено на Chrimson, канальный родопсин, впервые описанный Бойденом, который лучше всего стимулируется оранжевым светом.
Первыми результатами наших инженерных экспериментов с Chrimson были быстрый Chrimson (f-Chrimson) и очень быстрый Chrimson (vf-Chrimson). Мы были рады обнаружить, что f-Chrimson позволяет кохлеарным нейронам надежно реагировать на красный свет при частоте стимуляции примерно 200 Гц. Vf-Chrimson еще быстрее, но хуже экспрессируется в клетках, чем f-Chrimson; до сих пор vf-Chrimson не продемонстрировал заметного преимущества перед f-Chrimson, когда речь идет о высокочастотной стимуляции кохлеарных нейронов.
Эта гибкая матрица микро-светодиодов, изготовленная во Фрайбургском университете, намотана на стеклянный стержень диаметром 1 миллиметр. Массив показан с выключенными 144 диодами [слева] и работающими на 1 миллиампер [справа]. Фрайбургский университет/Frontiers
Мы также изучаем наши варианты имплантированного источника света, который будет запускать оптогенетические клетки. Имплантат должен быть достаточно маленьким, чтобы поместиться в ограниченном пространстве улитки, достаточно жестким для хирургического введения, но достаточно гибким, чтобы плавно повторять кривизну улитки. Его корпус должен быть биосовместимым, прозрачным и достаточно прочным, чтобы прослужить десятилетиями. Мои соавторы
Имплантат должен быть достаточно маленьким, чтобы поместиться в ограниченном пространстве улитки, достаточно жестким для хирургического введения, но достаточно гибким, чтобы плавно повторять кривизну улитки. Его корпус должен быть биосовместимым, прозрачным и достаточно прочным, чтобы прослужить десятилетиями. Мои соавторы
Ульрих Шварц и Патрик Рутер, тогда работавшие во Фрайбургском университете, начали с разработки первых микросветоизлучающих диодов (микро-светодиодов) для оптических кохлеарных имплантов.
Мы нашли микро-светодиоды полезными, потому что это очень зрелая коммерческая технология с хорошей энергоэффективностью. Мы провели
несколько экспериментов с тонкопленочными микросветодиодами, изготовленными из микроволокна, и продемонстрировали, что мы можем оптогенетически стимулировать кохлеарный нерв в наших целевых диапазонах частот. Но у микросветодиодов есть недостатки. Во-первых, трудно установить гибкую, прозрачную и прочную герметичную изоляцию вокруг имплантированных микросветодиодов. Кроме того, микросветодиоды с наивысшей эффективностью излучают синий свет, что возвращает нас к проблеме фототоксичности. Вот почему мы также смотрим на другой путь вперед.
Кроме того, микросветодиоды с наивысшей эффективностью излучают синий свет, что возвращает нас к проблеме фототоксичности. Вот почему мы также смотрим на другой путь вперед.
Вместо того, чтобы поместить сам полупроводниковый излучатель в улитку, альтернативный подход помещает источник света, такой как лазерный диод, дальше в герметичный титановый корпус. Затем оптические волокна доставляют свет в улитку и к светочувствительным нейронам. Оптические волокна должны быть биосовместимыми, прочными и достаточно гибкими, чтобы проходить через улитку, что может быть затруднительно при использовании обычных стеклянных волокон. В настоящее время ведутся интересные исследования гибких полимерных волокон, которые могут иметь лучшие механические характеристики, но пока что они не могут сравниться со стеклом по эффективности распространения света. Волоконно-оптический подход может иметь недостатки в эффективности, потому что мы потеряем некоторое количество света, когда он идет от лазерного диода к волокну, когда он проходит по волокну и когда он идет от волокна к улитке. Но подход кажется многообещающим, так как он гарантирует, что оптоэлектронные компоненты могут быть надежно запечатаны и, вероятно, облегчит вставку гибкой решетки волноводов.
Но подход кажется многообещающим, так как он гарантирует, что оптоэлектронные компоненты могут быть надежно запечатаны и, вероятно, облегчит вставку гибкой решетки волноводов.
Другая возможность конструкции оптических кохлеарных имплантатов заключается в использовании лазерных диодов в качестве источника света и сопряжении их с оптическими волокнами, изготовленными из гибкого полимера. Лазерный диод можно было бы безопасно инкапсулировать вне улитки, что уменьшило бы опасения по поводу нагревания, в то время как массивы полимерных волноводов [изображения слева и справа] закручивались бы в улитку, чтобы доставлять свет к клеткам. OptoGenTech
Путь к клиническим испытаниям
Поскольку мы рассматриваем возможность сборки этих компонентов в коммерческое медицинское устройство, мы сначала ищем части существующих кохлеарных имплантов, которые мы могли бы использовать. Аудиопроцессоры, которые работают с современными кохлеарными имплантами, можно адаптировать для наших целей; нам просто нужно разделить сигнал на большее количество каналов с меньшими частотными диапазонами. Внешний передатчик и имплантированный приемник также могут быть аналогичны существующим технологиям, что значительно облегчит наш путь регулирования. Но действительно новые части нашей системы — оптический стимулятор и генная терапия для доставки канальных родопсинов в улитку — потребуют тщательного изучения.
Аудиопроцессоры, которые работают с современными кохлеарными имплантами, можно адаптировать для наших целей; нам просто нужно разделить сигнал на большее количество каналов с меньшими частотными диапазонами. Внешний передатчик и имплантированный приемник также могут быть аналогичны существующим технологиям, что значительно облегчит наш путь регулирования. Но действительно новые части нашей системы — оптический стимулятор и генная терапия для доставки канальных родопсинов в улитку — потребуют тщательного изучения.
Операция по кохлеарной имплантации достаточно зрелая и обычно занимает максимум пару часов. Для простоты мы хотим, чтобы наша процедура была как можно ближе к существующим операциям. Но ключевая часть операции будет совсем другой: вместо того, чтобы вставлять электроды в улитку, хирурги сначала введут вирусные векторы, чтобы доставить гены каналородопсина в клетки улитки, а затем имплантируют в улитку излучатель света.
Поскольку оптогенетическая терапия только начинает проходить клинические испытания, все еще существует некоторая неопределенность в отношении того, как лучше всего заставить эту технику работать на людях. Мы все еще думаем, как заставить вирусный вектор доставлять необходимые гены в нужные нейроны улитки. Вирусный вектор, который мы использовали в экспериментах до сих пор,
Мы все еще думаем, как заставить вирусный вектор доставлять необходимые гены в нужные нейроны улитки. Вирусный вектор, который мы использовали в экспериментах до сих пор,
Аденоассоциированный вирус — это безвредный вирус, который уже был одобрен для использования в нескольких генных терапиях, и мы используем некоторые генетические приемы и местное введение для целенаправленного воздействия на кохлеарные нейроны. Мы уже начали собирать данные о стабильности оптогенетически измененных клеток и о том, потребуются ли им повторные инъекции генов каналородопсина, чтобы оставаться чувствительными к свету.
Наша дорожная карта для клинических испытаний очень амбициозна. Сейчас мы работаем над завершением и заморозкой конструкции устройства, и у нас продолжаются доклинические исследования на животных, чтобы проверить фототоксичность и доказать эффективность основной идеи. Мы стремимся начать наше первое исследование на людях в 2026 году, в ходе которого мы найдем самую безопасную дозу для генной терапии. Мы надеемся начать крупное клиническое испытание фазы 3 в 2028 году для сбора данных, которые мы будем использовать при подаче устройства на одобрение регулирующих органов, которое мы можем выиграть в начале 2030-х годов.
Мы надеемся начать крупное клиническое испытание фазы 3 в 2028 году для сбора данных, которые мы будем использовать при подаче устройства на одобрение регулирующих органов, которое мы можем выиграть в начале 2030-х годов.
Мы предвидим будущее, в котором лучи света смогут создавать богатые звуковые ландшафты для людей с глубокой потерей слуха или глухотой. Мы надеемся, что оптический кохлеарный имплант позволит им различать голоса на оживленном совещании, ценить тонкости своих любимых песен и воспринимать весь спектр звука — от трели птиц до гулких басовых нот. Мы думаем, что эта технология может осветить их слуховой мир.
Электронный нос: новые биомаркеры в диагностике рака легких
Воутер Х. ван Геффен, Кевин Ламот, Адриен Костантини, Лизза Э.Л. Хендрикс, Наджиб М. Рахман, Торстен Г. Блюм, Ян ван Меербек
Breathe 2019 15: e135-e141; Doi: 10.1183/20734735.0309-2019
- Статья
- Рисунки и данные
- Информация и метрики
Аннотация
LUNG RACE очень распространена, а самая распространенная компания. Несмотря на недавний прогресс в системном лечении рака легкого (ингибиторы контрольных точек и ингибиторы тирозинкиназы), ежегодно от этого заболевания умирает более 1,5 миллиона человек. У большинства пациентов с раком легких на момент постановки диагноза заболевание уже находится на поздней стадии. Скрининг с помощью компьютерной томографии у лиц с высоким риском может выявить рак легких на более ранней стадии, но ценой ложноположительных результатов. Биомаркеры могут привести к уменьшению этих ложноположительных результатов и более ранней диагностике рака легких, а также могут улучшить результаты и мониторинг лечения. На сегодняшний день таких биомаркеров для рака легких и других злокачественных новообразований грудной клетки не хватает, хотя биомаркеры, полученные из электронного носа (e-nose), представляют интерес.
Несмотря на недавний прогресс в системном лечении рака легкого (ингибиторы контрольных точек и ингибиторы тирозинкиназы), ежегодно от этого заболевания умирает более 1,5 миллиона человек. У большинства пациентов с раком легких на момент постановки диагноза заболевание уже находится на поздней стадии. Скрининг с помощью компьютерной томографии у лиц с высоким риском может выявить рак легких на более ранней стадии, но ценой ложноположительных результатов. Биомаркеры могут привести к уменьшению этих ложноположительных результатов и более ранней диагностике рака легких, а также могут улучшить результаты и мониторинг лечения. На сегодняшний день таких биомаркеров для рака легких и других злокачественных новообразований грудной клетки не хватает, хотя биомаркеры, полученные из электронного носа (e-nose), представляют интерес.
Методика E-nose с использованием измерения компонентов выдыхаемого воздуха позволяет выявить рак легкого с чувствительностью от 71% до 96% и специфичностью от 33 до 100%. В некоторых сериях такие результаты были проверены, но в основном используется внутренняя проверка, и, следовательно, требуется дополнительная работа. Кроме того, отсутствуют стандартизированные методы отбора проб и анализа, что затрудняет сравнение между исследованиями и клиническое применение. В этом описательном обзоре мы представляем обзор имеющихся в настоящее время данных о технологии E-nose для обнаружения рака легких.
В некоторых сериях такие результаты были проверены, но в основном используется внутренняя проверка, и, следовательно, требуется дополнительная работа. Кроме того, отсутствуют стандартизированные методы отбора проб и анализа, что затрудняет сравнение между исследованиями и клиническое применение. В этом описательном обзоре мы представляем обзор имеющихся в настоящее время данных о технологии E-nose для обнаружения рака легких.
Abstract
Методы электронного носа с использованием измерения компонентов выдыхаемого воздуха позволяют отличить больных раком легких как от здоровых людей, так и от пациентов с незлокачественными респираторными заболеваниями http://bit.ly/2QVttNr
Ключевые моменты методы, использующие измерения компонентов выдыхаемого воздуха, позволили отличить больных раком легких как от здоровых людей, так и от пациентов с незлокачественными респираторными заболеваниями.
Биомаркер рака легкого может способствовать более ранней диагностике и улучшению мониторинга лечения.
Рак легких является наиболее частой причиной смерти от рака во всем мире [1]. Несмотря на недавний прогресс в системном лечении рака легких (ингибиторы контрольных точек и ингибиторы тирозинкиназы), ежегодно от рака легких умирает более 1,5 млн человек [2]. Более чем у половины пациентов с раком легкого на момент постановки первоначального диагноза заболевание находится на поздних стадиях [2]. Ключевыми шагами к снижению смертности, связанной с раком легких, являются более ранняя диагностика рака легких (и других злокачественных новообразований грудной клетки, таких как мезотелиома) и улучшение выявления бессимптомных пациентов. Скрининг может быть ключом к увеличению шансов на излечение или увеличение продолжительности жизни [3]. В настоящее время большинство скрининговых исследований и программ включают компьютерную томографию (КТ), но ценой ложноположительных результатов. Добавление биомаркера, полученного неинвазивно, могло бы обеспечить столь необходимую ценность этих программ, как для рака легких, так и для мезотелиомы [3, 4], за счет повышения специфичности и уменьшения ложноположительных результатов или обеспечения более персонализированного последующего наблюдения.
Что такое биомаркеры?
Согласно Рабочей группе по биомаркерам Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США и Национальных институтов здравоохранения, биомаркер определяется как «характеристика, которая измеряется как показатель нормальных биологических процессов, патогенных процессов или реакции на воздействие или вмешательство, включая терапевтические вмешательства. Молекулярные, гистологические, радиографические или физиологические характеристики являются типами биомаркеров. Биомаркер — это не оценка того, как человек себя чувствует, функционирует или выживает». Категории биомаркеров [5] включают:
susceptibility/risk biomarkers
diagnostic biomarkers
monitoring biomarkers
prognostic biomarkers
predictive biomarkers
pharmacodynamic/response biomarkers
safety biomarkers
Биомаркер должен соответствовать таким критериям, как возможность обнаружения в точке, где он может изменить путь пациента или исход заболевания, или указывать на другие тесты в диагностических или скрининговых условиях.
Зачем нужны биомаркеры при раке легких?
Диагностические биомаркеры
Биомаркер, если он доступен, может быть полезен в трех важных целях. Во-первых, это может помочь в постановке диагноза рака легких, особенно в рамках программы скрининга рака грудной клетки с относительно высоким процентом ложноположительных результатов. Это также может помочь в отборе пациентов с высоким риском для программы скрининга КТ. При раке легкого такие биомаркеры не были одобрены для клинического использования, но в других областях такие биомаркеры представляли интерес (9).0178 напр. простатспецифический антиген и карциноэмбриональный антиген). Для рака легких в настоящее время проводятся испытания ECLS и bio-MILD для оценки онкомаркеров в крови.
Кроме того, золотым стандартом диагностики рака грудной клетки является отчет о патологии, указывающий на злокачественные клетки. Однако довольно часто (90 178, например, 90 179 у пациентов с тяжелым течением ХОБЛ, у которых невозможно безопасно получить биопсию) невозможно получить достаточное количество ткани для установления диагноза, и междисциплинарная команда принимает решения на основе рентгенологических и клинических данных. Диагностический биомаркер был бы полезен, чтобы помочь этим командам принять решение о вероятности злокачественного новообразования.
Диагностический биомаркер был бы полезен, чтобы помочь этим командам принять решение о вероятности злокачественного новообразования.
Прогностические биомаркеры
Вторая важная роль биомаркеров заключается в прогнозировании будущего ответа на лечение. Обнаружение мутаций рецептора эпидермального фактора роста ( EGFR ) и ALK или других драйверных мутаций считается успешным биомаркером при немелкоклеточном раке легкого (НМРЛ) [6, 7]. Другим биомаркером, используемым для прогнозирования ответа на лечение, является показатель пропорции опухоли лиганда запрограммированной смерти 1 (PD-L1). PD-L1 связан с эффективностью ингибитора контрольной точки на стадии IV и, возможно, также на стадии III, НМРЛ. В клинических испытаниях мезотелиомы, мелкоклеточного рака легкого и других стадий НМРЛ PD-L1 также привлекает все больше клинического внимания. Однако тесты на PD-L1 далеки от совершенства, с низкой чувствительностью и специфичностью [2]. Значительный объем исследовательской деятельности направлен на разработку новых стратегий и биомаркеров для замены или улучшения PD-L1. Необходимо улучшить чувствительность и специфичность этого биомаркера с потенциалом улучшения за счет новых или дополнительных биомаркеров.
Необходимо улучшить чувствительность и специфичность этого биомаркера с потенциалом улучшения за счет новых или дополнительных биомаркеров.
Биомаркеры для мониторинга
В-третьих, биомаркер может помочь в серийном мониторинге эффекта лечения или в различении прогрессирования заболевания и токсичности от лечения, такого как лучевая терапия или иммунотерапия. Такой биомаркер можно было бы эффективно использовать параллельно с информацией, полученной с помощью компьютерной томографии или позитронно-эмиссионной томографии. При раке легкого таких биомаркеров нет. Однако эта роль биомаркеров в настоящее время используется в других методах лечения рака, например, с помощью простатспецифического антигена и карциноэмбрионального антигена.
В идеале диагностический биомаркер, предназначенный для оптимизации эффективности и безопасности низкодозового КТ-скрининга рака легкого и последующей инвазивной диагностики, должен обладать высокой чувствительностью и специфичностью, должен быть получен неинвазивно, прост в использовании и недорог. Анализ выдыхаемого воздуха может соответствовать этому профилю при обнаружении злокачественных новообразований грудной клетки. В этом описательном обзоре мы представляем обзор имеющихся в настоящее время данных об электронном носе (e-nose) в качестве потенциального диагностического, прогностического или мониторингового биомаркера для лечения рака легких.
Анализ выдыхаемого воздуха может соответствовать этому профилю при обнаружении злокачественных новообразований грудной клетки. В этом описательном обзоре мы представляем обзор имеющихся в настоящее время данных об электронном носе (e-nose) в качестве потенциального диагностического, прогностического или мониторингового биомаркера для лечения рака легких.
Электронный нос может обнаруживать летучие органические соединения (ЛОС). Он используется как в медицинских, так и в немедицинских целях. Электронный нос в медицинских целях чаще всего используется для измерения ЛОС в выдыхаемом воздухе пациентов, но также использовался для оценки нескольких биологических образцов, включая фекалии, биоптаты, слюну и кожу [8–10].
Летучие органические соединения
Что такое ЛОС?
ЛОС были идентифицированы в 1970-х годах [11]. С тех пор анализ дыхания превратился в высокопроизводительную область исследований в области дыхательной томики, где в дыхании человека было обнаружено более 3000 различных летучих органических соединений [12, 13]. Большинство частиц в воздухе являются биогенными и испускаются в результате внешних процессов, таких как окружающая среда и загрязнение атмосферы [10]. Однако из-за метаболических процессов в организме человека могут выделяться ЛОС или изменяться характер ЛОС [13]. Эти процессы могут быть физиологическими, но также могут быть вызваны или изменены болезнью. Поэтому считается, что эти ЛОС вызывают специфический «запах» или «отпечаток дыхания» при различных заболеваниях. Когда концентрация ЛОС измеряется непосредственно или измеряется после улавливания и хранения ( напр. через мешков для сбора или контейнеров) могут быть обнаружены различные следы дыхания или узоры [14].
Большинство частиц в воздухе являются биогенными и испускаются в результате внешних процессов, таких как окружающая среда и загрязнение атмосферы [10]. Однако из-за метаболических процессов в организме человека могут выделяться ЛОС или изменяться характер ЛОС [13]. Эти процессы могут быть физиологическими, но также могут быть вызваны или изменены болезнью. Поэтому считается, что эти ЛОС вызывают специфический «запах» или «отпечаток дыхания» при различных заболеваниях. Когда концентрация ЛОС измеряется непосредственно или измеряется после улавливания и хранения ( напр. через мешков для сбора или контейнеров) могут быть обнаружены различные следы дыхания или узоры [14].
ЛОС при других заболеваниях
Ранее было показано, что ЛОС и обнаружение следов дыхания с помощью электронных носов эффективны при респираторных заболеваниях [15]. Для ХОБЛ этот метод не только позволяет диагностировать ХОБЛ, но также может определить происхождение обострений ХОБЛ и может быть использован в дифференциальной диагностике ХОБЛ и астмы [15-17]. При астме он используется для выявления заболевания и определения его фенотипа. ЛОС используются при муковисцидозе и для выявления туберкулеза [18]. Кроме того, нереспираторные заболевания можно обнаружить с помощью электронного носа (9).0178 напр. 90–179 Пищевод Барретта и воспалительные заболевания кишечника) [8, 19]. Для других типов рака были опубликованы положительные исследования электронного носа, включая рак головы и шеи, мочевого пузыря и толстой кишки [20].
При астме он используется для выявления заболевания и определения его фенотипа. ЛОС используются при муковисцидозе и для выявления туберкулеза [18]. Кроме того, нереспираторные заболевания можно обнаружить с помощью электронного носа (9).0178 напр. 90–179 Пищевод Барретта и воспалительные заболевания кишечника) [8, 19]. Для других типов рака были опубликованы положительные исследования электронного носа, включая рак головы и шеи, мочевого пузыря и толстой кишки [20].
ЛОС при раке легких
В основе исследования характера дыхания при раке лежит исследование McCulloch et al . [21]. Это испытание показало, что обученные собаки способны выявлять больных раком легких в группе добровольцев, включая здоровых людей. В 1980-х годах специфические ЛОС впервые были продемонстрированы у пациентов с раком легкого [22]. Затем исследования были сосредоточены на выявлении конкретных летучих органических соединений. Оценивались различные отдельные летучие органические соединения: пропранолол, изопрен, ацетон, пентан, гексаналь и бензол [23]. Однако в то время это оказалось недостаточно точным, дорогим и трудоемким [24].
Однако в то время это оказалось недостаточно точным, дорогим и трудоемким [24].
Таким образом, проценты уменьшились. По мере развития технологий и разработки более совершенных датчиков интерес вновь возник, и в лаборатории были проведены новые тесты на тканях и клеточных линиях [9, 25]. Датчики, используемые в настоящее время, сосредоточены на распознавании образов. Эти шаблоны должны быть сначала «выучены» машиной с использованием искусственного интеллекта аналогично дрессировке собак, использованной в оригинальном исследовании Маккаллоха [21]. С помощью этого принципа теперь стало возможным дифференцировать рак легких у здоровых людей и у пациентов с ХОБЛ [14, 26–28]. В настоящее время проблемы, препятствующие распространению метода в клинической практике, включают стабильность ЛОС, а также стабильность и взаимозаменяемость устройств [29].]. Если эти проблемы удастся решить, мы ожидаем, что электронные носы смогут найти свое применение в повседневной практике.
Прогресс также достигнут в лечении мезотелиомы. Первые тесты были опубликованы в 2012 году [30, 31], показывая, что распознавание молекулярных паттернов выдыхаемого воздуха может отличать пациентов с мезотелиомой от здоровых людей. Совсем недавно это было подтверждено исследованием, сочетающим анализ дыхания с помощью газовой хроматографии-масс-спектрометрии и электронного носа [32, 33].
Первые тесты были опубликованы в 2012 году [30, 31], показывая, что распознавание молекулярных паттернов выдыхаемого воздуха может отличать пациентов с мезотелиомой от здоровых людей. Совсем недавно это было подтверждено исследованием, сочетающим анализ дыхания с помощью газовой хроматографии-масс-спектрометрии и электронного носа [32, 33].
Электронные носы
В разных электронных носах используются разные технологические принципы. Различия между электронными носами возникают на многих уровнях, наиболее очевидным из которых является метод отбора проб воздуха. Некоторым носам требуется удерживающая канистра, в то время как в других используется воздух внутри баллона с образцом. Почти каждая система нуждается в изолированной среде в момент отбора проб и измерений для предотвращения загрязнения, особенно для уменьшения влияния дезинфицирующих средств или сигаретного дыма [24, 34].
Дополнительные различия возникают на уровне методических принципов. Некоторые более старые электронные носы измеряли отдельные ЛОС в отличие от других, более современных носов, которые оценивают закономерности, последние требуют обучения на тестовых наборах и проверки в независимом наборе, прежде чем получать полезные результаты. Большинство носов распознавания образов используются в сочетании с искусственным интеллектом [7].
Большинство носов распознавания образов используются в сочетании с искусственным интеллектом [7].
Самое важное отличие, однако, заключается в различных типах датчиков, используемых внутри технологии. Наиболее часто используемыми методами являются газовая хроматография, спектрометрия, колориметрия, поверхностные акустические волны и кондуктометрия [34].
Газовая хроматография
Этот метод позволяет разделять различные типы молекул. Проба воздуха соединяется с газом-носителем и затем движется против неподвижной составляющей, в результате чего возникает реакция. Разные вещества дают разные отклики, очевидным примером является простая хроматография [34, 35].
Спектрометрия
Спектрометры чаще всего сочетаются с газовой хроматографией. Они используются в качестве устройств для идентификации конкретных химических веществ. После ионизации соединений ионы от молекул отделяются в соответствии с отношением массы к заряду. Это разделение обычно происходит в вакууме с магнитным полем. Техника громоздка, дорога и сложна в транспортировке, и на сегодняшний день ни одна система по месту оказания медицинской помощи с этой техникой не используется широко [34, 36].
Техника громоздка, дорога и сложна в транспортировке, и на сегодняшний день ни одна система по месту оказания медицинской помощи с этой техникой не используется широко [34, 36].
Колориметрия
Колориметрические устройства работают с датчиками с химически чувствительными красителями. Эти красители могут быть адаптированы в зависимости от целевых летучих органических соединений. В одном датчике можно использовать несколько красителей, что позволяет обнаруживать закономерности ЛОС [36].
Поверхностная акустическая волна
Акустические датчики работают, подвергая свои датчики воздействию газов. Затем газы изменяют уже испущенную акустическую волну из-за реакции с поверхностью датчика. Затем эти волны анализируются на наличие ЛОС или идентификацию паттерна [34].
Кондуктометрия
Этот метод работает с сенсорами ( например, оксидно-металлическими или полимерными сенсорами), которые состоят из различных металлов, допускающих различные взаимодействия с летучими соединениями. Выдыхаемый воздух направляется на эти датчики, позволяя происходить окислительно-восстановительным реакциям, что приводит к изменению проводимости датчиков [16, 34, 37].
Выдыхаемый воздух направляется на эти датчики, позволяя происходить окислительно-восстановительным реакциям, что приводит к изменению проводимости датчиков [16, 34, 37].
Вопросы для самооценки
Какое из следующих утверждений относительно скрининга рака легких верно?
а. PD-L1 является подходящим биомаркером.
б. Жидкая биопсия дает подходящий биомаркер.
в. Анализ электронного носа (e-nose) дает подходящий биомаркер.
д. Нет подходящего биомаркера.
Какое из следующих утверждений относительно летучих органических соединений (ЛОС) верно?
а. Их могут учуять только собаки.
б. Их можно вынюхать только электронными носами.
в. Их могут учуять как собаки, так и электронные носы.
д. Их нельзя вынюхивать.
Когда впервые была опубликована идея измерения летучих органических соединений для выявления рака легких?
У больных раком легкого электронный нос:
а.
 бесполезно.
бесполезно.б. можно использовать для различения здоровых людей и больных раком легких.
в. может заменить обнаружение PD-L1.
д. может заменить компьютерную томографию грудной клетки.
Предлагаемые ответы
d.
в.
а.
б.
Текущий уровень доказательности и текущие ограничения
Диагностические биомаркеры электронного носа
Когда мы оцениваем потенциальную роль биомаркеров при торакальных заболеваниях, большинство исследований, основанных на ЛОС, были посвящены выявлению рака. На сегодняшний день электронные носы способны выявлять рак в различных условиях и прошли испытания 9.0178 in vitro . Они позволяют отличить больных раком легкого от здоровых пациентов как у добровольцев, так и у лиц с подозрением на рак [38]. Такие исследования чаще всего оценивают летучие органические соединения, испускаемые клетками, в лабораторных условиях, при этом проводится около исследований in vivo , но в основном в экспериментальной форме.
Эти исследования продемонстрировали обнаружение рака легкого с чувствительностью от 71% до 96% и специфичностью от 33 до 100% (таблица 1). Было предпринято несколько попыток подтвердить эти результаты, но в основном они проводились только с использованием внутренней проверки. Отсутствует стандартизированный метод отбора проб и анализа, что затрудняет сравнение между исследованиями и клиническую реализацию [29]., 43, 44].
Таблица 1
Наиболее важные опубликованные исследования по оценке эффективности e-nose при раке легкого
Прогностические биомаркеры e-nose
Исследования роли биомаркеров в прогнозировании будущих ответов на лечение очень ограничены. В небольшом пилотном исследовании электронный нос смог различать EGFR -мутантный и EGFR дикого типа НМРЛ; однако необходимы дополнительные исследования для оценки этого [45]. В недавно опубликованном исследовании тестировался электронный нос для прогнозирования ответа на терапию анти-PD-1 у пациентов с НМРЛ, при этом площадь под кривой, подтвержденная в валидационном наборе, составила 0,85 [46].
Мониторинг биомаркеров электронного носа
Для этой конкретной роли на данном этапе мы не нашли опубликованных данных. Тем не менее, усилия по изучению этой специфической роли электронного носа предпринимаются.
Резюме
Методы электронного носа, использующие измерение компонентов выдыхаемого воздуха, могут обнаруживать рак легких с чувствительностью от 71% до 96% и специфичностью от 33 до 100%. Однако на данный момент отсутствуют стандартизированные методы отбора проб и анализа, что затрудняет сравнение между исследованиями и клиническое применение.
Будущие исследования
Будущие направления исследований в этой области включают использование искусственного интеллекта для повышения специфичности и чувствительности при обнаружении рака легких. В настоящее время необходимы широкомасштабные валидационные исследования с использованием различных устройств в разных местах в соответствии с рекомендованными техническими стандартами для продвижения вперед в этой области [5, 43, 44, 47]. Такие новые исследования могут проверить, может ли электронный нос быть полезным в качестве биомаркера для целей скрининга населения. Испытание с таким дизайном в настоящее время регистрируется (www.clinicaltrials.gov, идентификатор NCT02612532), в котором планируется включить 4000 субъектов. Другие области будущих исследований включают оценку электронного носа в прогнозировании ответа на лечение, мониторинг лечения или дифференциацию осложнений лечения (9).0178 напр. пневмонит) от прогрессирования заболевания [46,48]. Потенциал объединения различных ЛОС и радиологических или патологических маркеров для снижения предполагаемых рисков, связанных с каждым из них, и повышения их эффективности является плодородной областью для будущих исследований [49].
Такие новые исследования могут проверить, может ли электронный нос быть полезным в качестве биомаркера для целей скрининга населения. Испытание с таким дизайном в настоящее время регистрируется (www.clinicaltrials.gov, идентификатор NCT02612532), в котором планируется включить 4000 субъектов. Другие области будущих исследований включают оценку электронного носа в прогнозировании ответа на лечение, мониторинг лечения или дифференциацию осложнений лечения (9).0178 напр. пневмонит) от прогрессирования заболевания [46,48]. Потенциал объединения различных ЛОС и радиологических или патологических маркеров для снижения предполагаемых рисков, связанных с каждым из них, и повышения их эффективности является плодородной областью для будущих исследований [49].
Сноски
Конфликт интересов: Д-р ван Геффен сообщает о грантах от Novartis, помимо представленной работы.
Конфликт интересов: К. Ламот сообщает о грантах от Kom op tegen Kanker (Противодействие раку), Фламандского онкологического общества, во время написания этой статьи.

Конфликт интересов: А. Костантини нечего раскрывать.
Конфликт интересов: L.E.L. Хендрикс сообщает о гонорарах, выплаченных ее учреждению за участие в консультативном совете от Boehringer Ingelheim и BMS, о поддержке командировок от Roche и BMS, о финансировании исследований, оплаченных ее учреждению от Roche, Boehringer Ingelheim и AstraZeneca, о программе наставничества с ключевыми лидерами общественного мнения, финансируемой AstraZeneca, и персональные сборы за образовательные вебинары от Quadia, помимо представленной работы.
Конфликт интересов: Н.М. Рахману нечего раскрывать.
Конфликт интересов: Т.Г. Блуму нечего раскрывать.
Конфликт интересов: J. van Meerbeeck не раскрывает ничего.
http://creativecommons.org/licenses/by-nc/4.0/
Статьи Breathe находятся в открытом доступе и распространяются в соответствии с условиями некоммерческой лицензии Creative Commons Attribution 4. 0.
0.
Ссылки
- ↵
- Рак Сегодня
. Информационные бюллетени по раку. https://gco.iarc.fr/today/fact-sheets-cancers.
- ↵
- Planchard D,
- Popat S,
- Kerr K, et al.
Метастатический немелкоклеточный рак легкого: Клинические практические рекомендации ESMO по диагностике, лечению и последующему наблюдению. Энн Онкол 2018; 29: Доп. 4, iv192–iv237. doi:10.1093/annonc/mdy275
- ↵
- Seijo LM,
- Peled N,
- Ajona D, et al.
Биомаркеры в скрининге рака легких: достижения, перспективы и проблемы. J Thorac Oncol 2019; 14: 343–357. doi:10.1016/j.jtho.2018.11.023
- ↵
- Lamote K,
- Brinkman P,
- Vandermeersch L, et al.
Анализ дыхания с помощью газовой хроматографии, масс-спектрометрии и электронного носа для скрининга мезотелиомы плевры: перекрестное исследование случай-контроль.
 Онкотаргет 2017; 8: 91593–91602. doi:10.18632/oncotarget.21335
Онкотаргет 2017; 8: 91593–91602. doi:10.18632/oncotarget.21335 - ↵
- Рабочая группа FDA-NIH по биомаркерам
. ЛУЧШИЙ ресурс (биомаркеры, конечные точки и другие инструменты). Silver Spring, Food and Drug Administration, 2016.
- ↵
- Goossens N,
- Nakagawa S,
- Sun X, et al.
Открытие и проверка биомаркеров рака. Transl Cancer Res 2015; 4: 256–269.
- ↵
- Нарди-Агмон I,
- Пелед N
. Анализ выдыхаемого воздуха для раннего выявления рака легких: последние разработки и перспективы на будущее. Рак легких 2017; 8: 31–38.
- ↵
- Huiskamp H,
- Bartelink ME
. Su1830 — Возможности электронного носа для обнаружения воспалительных заболеваний кишечника.
 Гастроэнтерология 2018; 154: С-599. doi:10.1016/S0016-5085(18)32176-0
Гастроэнтерология 2018; 154: С-599. doi:10.1016/S0016-5085(18)32176-0 - ↵
- Filipiak W,
- Filipiak A,
- Sponring A, et al.
Сравнительный анализ летучих органических соединений (ЛОС) от пациентов, опухолей и трансформированных клеточных линий для проверки маркеров дыхания, полученных при раке легких. J Breath Res 2014; 8: 027111. doi:10.1088/1752-7155/8/2/027111
- ↵
- Kesselmeier J,
- Staudt M
. Биогенные летучие органические соединения (ЛОС): обзор выбросов, физиологии и экологии. J Atmos Chem 1999; 33: 23–88. doi:10.1023/A:1006127516791
- ↵
- Pauling L,
- Robinson AB,
- Teranishi R, et al.
Количественный анализ паров мочи и дыхания методом газожидкостной распределительной хроматографии.
 Proc Natl Acad Sci USA 1971; 68: 2374–2376. doi:10.1073/pnas.68.10.2374
Proc Natl Acad Sci USA 1971; 68: 2374–2376. doi:10.1073/pnas.68.10.2374 - ↵
- Rocco G,
- Pennazza G,
- Santonico M, et al.
Отпечатки дыхания и ранняя диагностика рака легких. J Thorac Oncol 2018; 13: 883–894. doi:10.1016/j.jtho.2018.02.026
- ↵
- Behera B,
- Joshi R,
- Anil Vishnu GK, et al.
Электронный нос: неинвазивная технология анализа дыхания больных диабетом и раком легких. J Breath Res 2019; 13: 024001. doi:10.1088/1752-7163/aafc77
- ↵
- De Vries R,
- Brinkman P,
- Van Der Schee MP, et al.
Интеграция технологии электронного носа со спирометрией: проверка нового подхода к анализу выдыхаемого воздуха. J Breath Res 2015; 9: 046001.
 doi:10.1088/1752-7155/9/4/046001
doi:10.1088/1752-7155/9/4/046001 - ↵
- де Врис Р.,
- Дагелет YWF,
- Спур П. и др.
Клинико-воспалительное фенотипирование с помощью дыхательной томики при хронических заболеваниях дыхательных путей независимо от диагностической метки. Eur Respir J 2018; 51: 1701817. DOI: 10.1183/13993003.01817-2017
- ↵
- Van Geffen WH,
- Bruins M,
- KerstJens Ham
. Диагностика вирусных и бактериальных респираторных инфекций при обострениях ХОБЛ с помощью электронного носа: пилотное исследование. J Breath Res 2016; 10: 036001. doi:10.1088/1752-7155/10/3/036001
- ↵
- Fens N,
- de Nijs SB,
- Peters S, et al.
Молекулярное профилирование выдыхаемого воздуха в зависимости от воспалительного подтипа и активности при ХОБЛ.
 Eur Respir J 2011; 38: 1301–1309. doi:10.1183/0
Eur Respir J 2011; 38: 1301–1309. doi:10.1183/036.00032911
- ↵
- Saktiawati AMI,
- Stienstra Y,
- Subronto YW, et al.
Чувствительность и специфичность электронного носа в диагностике туберкулеза легких у больных с подозрением на туберкулез. PLoS One 2019; 14: e0217963.
- ↵
- Visrodia K,
- Zakko L,
- Allen J, et al.
Tu1111 – текущая разработка скринингового теста на пищевод Барретта с использованием устройства «электронный нос» для анализа выдыхаемых летучих органических соединений. Гастроэнтерология 2018; 154: С-894. doi:10.1016/S0016-5085(18)33018-X
- ↵
- van de Goor RMGE,
- Leunis N,
- van Hooren MRA, et al.
Применение технологии электронного носа для различения карциномы головы и шеи, мочевого пузыря и толстой кишки.
 Eur Arch Оториноларингол 2017; 274: 1053–1060. doi:10.1007/s00405-016-4320-y
Eur Arch Оториноларингол 2017; 274: 1053–1060. doi:10.1007/s00405-016-4320-y - ↵
- McCulloch M,
- Jezierski T,
- Броффман М. и др.
Диагностическая точность обнаружения собачьего запаха на ранних и поздних стадиях рака легкого и молочной железы. Интегр Рак Ther 2006; 5: 30–39. doi:10.1177/1534735405285096
- ↵
- Гордон С.М.,
- Сидон Дж.П.,
- Кротошинский Б.К., и др.
Летучие органические соединения в выдыхаемом воздухе больных раком легких. Clin Chem 1985; 31: 1278–1282.
- ↵
- Джиа З.,
- Патра А,
- Кутти В.К. и др.
Критический обзор анализа летучих органических соединений в выдыхаемом воздухе и культуре клеток in vitro для выявления рака легких.
 Метаболиты 2019; 9: Е52. doi:10.3390/metabo
Метаболиты 2019; 9: Е52. doi:10.3390/metabo52
- ↵
- Krilaviciute A,
- Heiss JA,
- Leja M, et al.
Обнаружение рака по выдыхаемому воздуху: систематический обзор. Онкотаргет 2015; 6: 38643–38657. doi:10.18632/oncotarget.5938
- ↵
- Wang Y,
- Wang D,
- Yu K, et al.
Анализ биомаркеров летучих органических соединений рака легких в выдыхаемом воздухе, тканях и клеточных линиях. Рак Биомарк 2012; 11: 129–137. doi:10.3233/CBM-2012-00270
- ↵
- Tirzite M,
- Bukovskis M,
- Strazda G, et al.
Обнаружение рака легких с помощью электронного носа и логистического регрессионного анализа. J Breath Res 2019; 13: 016006. doi:10.1088/1752-7163/aae1b8
- Kort S,
- Tiggeloven MM,
- Brusse-Keizer M, et al.

Многоцентровое проспективное исследование по диагностике подтипов рака легких по анализу выдыхаемого воздуха. Рак легких 2018; 125: 223–229. doi:10.1016/j.lungcan.2018.09.022
- ↵
- Huang CH,
- Zeng C,
- Wang YC, et al.
Исследование точности диагностики с использованием массива химических датчиков и метода машинного обучения для выявления рака легких. Датчики (Швейцария) 2018; 18: Е2845. doi:10.3390/s18092845
- ↵
- Hanna GB,
- Boshier PR,
- Markar SR, et al.
Точность и методологические проблемы тестов выдыхаемого воздуха на основе летучих органических соединений для диагностики рака: систематический обзор и метаанализ. JAMA Oncol 2019; 5: e182815. doi:10.1001/jamaoncol.2018.2815
- ↵
- Chapman EA,
- Thomas PS,
- Stone E, et al.

Дыхательный тест на злокачественную мезотелиому с использованием электронного носа. Eur Respir J 2012; 40: 448–454. doi:10.1183/0
36.00040911
- ↵
- Dragonieri S,
- Van Der Schee MP,
- Massaro T, et al.
Электронный нос отличает выдыхаемый воздух пациентов со злокачественной мезотелиомой плевры от контрольной группы. Рак легких 2012; 75: 326–331. doi:10.1016/j.lungcan.2011.08.009
- ↵
- Lagniau S,
- Lamote K,
- van Meerbeeck JP, et al.
Биомаркеры для ранней диагностики злокачественной мезотелиомы: нужен ли нам еще один лунный выстрел? Онкотаргет 2017; 8: 53751–53762. doi: 10.18632/oncotarget.17910
- ↵
- Lamote K,
- Vynck M,
- Thas O, et al.
Выдыхаемый воздух для выявления злокачественной мезотелиомы плевры: проверочное исследование.
 Eur Respir J 2017; 50: 1700919. doi:10.1183/13993003.00919-2017
Eur Respir J 2017; 50: 1700919. doi:10.1183/13993003.00919-2017 - ↵
- Рёк Ф,
- Барсан Н,
- Веймар У
02 9. Электронный нос: текущее состояние и будущие тенденции. Chem Rev 2008; 108: 705–725. doi:10.1021/cr068121q
- ↵
- Байтаревич А.,
- Агер К.,
- Пиенц М. и др.
Неинвазивная диагностика рака легких путем анализа выдыхаемого воздуха. BMC Рак 2009; 9: 348. doi:10.1186/1471-2407-9-348
- ↵
- Phillips M,
- Altorki N,
- Austin JHM, et al.
Выявление рака легких с помощью взвешенного цифрового анализа биомаркеров дыхания. Клин Чим Акта 2008; 393: 76–84. doi:10.1016/j.cca.2008.02.021
- ↵
- Kort S,
- Brusse-Keizer M,
- Schouwink H, et al.

Выявление немелкоклеточного рака легкого с помощью электронного носа. Рак легких 2017; 50: PA2032. doi:10.1183/1393003.congress-2017.PA2032
- ↵
- Thriumani R,
- Zakaria A,
- Hashim YZHY, et al.
Исследование летучих органических соединений, выделяемых культивируемыми in vitro клетками рака легких, с использованием матрицы газовых датчиков и SPME-GCMS. BMC Рак 2018; 18: 362. doi:10.1186/s12885-018-4235-7
- Dragonieri S,
- Annema JT,
- Schot R, et al.
Электронный нос в различении больных немелкоклеточным раком легкого и ХОБЛ. Рак легких 2009; 64: 166–170. doi:10.1016/j.lungcan.2008.08.008
- Д’Амико А,
- Пеннацца Г,
- Сантонико М
.
 Исследование по электронной носовой диагностике рака легких. Рак легких 2010; 68: 170–176. doi:10.1016/j.lungcan.2009.11.003
Исследование по электронной носовой диагностике рака легких. Рак легких 2010; 68: 170–176. doi:10.1016/j.lungcan.2009.11.003 - Gasparri R,
- Santonico M,
- Valentini C, et al.
Изменчивая сигнатура для ранней диагностики рака легких. J Breath Res 2016; 10: 016007. doi:10.1088/1752-7155/10/1/016007
- ван де Гур Р.,
- van Hooren M,
- Dingemans AM, et al.
Обучение и проверка портативного электронного носа для скрининга рака легких. J Thorac Oncol 2018; 13: 676–681. doi:10.1016/j.jtho.2018.01.024
- ↵
- Micheel CM,
- Ball JR
, ред. Оценка биомаркеров и суррогатных конечных точек при хронических заболеваниях. Вашингтон, National Academy Press, 2015.
- ↵
- Horváth I,
- Barnes PJ,
- Loukides S, et al.

Технический стандарт Европейского респираторного общества: биомаркеры выдыхаемого воздуха при заболеваниях легких. Eur Respir J 2017; 49: 1600965. doi:10.1183/13993003.00965-2016
- ↵
- Shlomi D,
- Abud M,
- Liran O, et al.
Обнаружение рака легких и мутации EGFR с помощью системы электронного носа. J Торак Онкол 2017; 12: 1544–1551. doi:10.1016/j.jtho.2017.06.073
- ↵
- de Vries R,
- Muller M,
- van der Noort V, et al.
Прогноз ответа на анти-PD-1 терапию у пациентов с немелкоклеточным раком легкого с помощью электронного носового анализа выдыхаемого воздуха. Энн Онкол 2019; 30: 1660–1666. doi:10.1093/annonc/mdz279
- ↵
- van der Schee MPC,
- Boschmans J,
- Смит Р.
 и др.
и др.
Раннее выявление рака легких с помощью анализа биомаркеров ЛОС в выдыхаемом воздухе: исследование LuCID. Eur Respir J 2017; 50: ОА1472.
- ↵
- Нарди-Агмон И.,
- Абуд-Хава М.,
- Лиран О. и др.
Анализ выдыхаемого воздуха для мониторинга ответа на лечение при распространенном раке легкого. J Thorac Oncol 2016; 11: 827–837. doi:10.1016/j.jtho.2016.02.017
- ↵
- Camidge DR,
- Doebele RC,
- Kerr KM
. Сравнение и противопоставление прогностических биомаркеров для иммунотерапии и таргетной терапии НМРЛ. Nat Rev Clin Oncol 2019; 16: 341–355. doi:10.1038/s41571-019-0173-9
ПредыдущийСледующий
Наверх
Специалисты по искусственному обонянию
Специалисты по искусственному обонянию
Концепция электронного носа
Концепция электронного носа возникла в семидесятых годах. До этого аналитическая химия была занята разработкой высокоспецифичных датчиков и методов, направленных на идентификацию уникальных
До этого аналитическая химия была занята разработкой высокоспецифичных датчиков и методов, направленных на идентификацию уникальных
Новые возможности персональных компьютеров позволили применять методы распознавания образов к сложным данным измерений. Важное следствие концепции заключается в том, что вещество или смеси веществ могут быть распознаны только после фазы калибровки: чтобы соответствовать образцу, это должно быть известно заранее («увидено» раньше) веществ.
Предложение состояло в том, чтобы иметь общую сенсорную систему с широким откликом, генерирующую сложные многомерные данные измерений, и использовать методы распознавания образов для сопоставления измеренных «образцов» с ранее «увиденными» образцами. Это аналогично тому, как мы обоняем, отсюда и название. «электронный нос». Это показано на рисунке.
Типы датчиков электронного носа
Основная концепция электронного носа, или машинного обоняния, представляет собой единицу измерения, которая генерирует сложные многомерные данные для каждого измерения в сочетании с методом распознавания образов, который интерпретирует сложные данные и связывает их с целевое значение или класс.
В академической литературе системы, основанные, например, на масс-спектрометре в сочетании с распознаванием образов, иногда представляются как приложение «электронный нос» или искусственное обоняние. Однако в этом разделе обсуждаются только относительно недорогие сенсорные технологии, которые в принципе подходят для настольных или портативных устройств.
Требование, чтобы генерировался многомерный измерительный сигнал, исключает отдельные элементы обнаружения, используемые, например, измерители PID. Это часто преодолевается за счет использования набора широко чувствительных элементов с различной чувствительностью к важным химическим соединениям. Поскольку устройство «электронный нос» часто подвергается воздействию летучих химических веществ, массивы потенциометрических датчиков непригодны для использования.
Последние предназначены для обнаружения утечек, так как содержат ограниченное количество реактивных химикатов (принцип работы аналогичен химической батарее), которые истощаются при контакте с целевыми веществами.
Возможными для применения технологиями являются QMB/SAW, проводящие полимеры и датчики на основе оксидов металлов.
QMB представляет собой кристалл кварца с химически активной поверхностью, обычно из полимера. Когда молекулы газа адсорбируются на поверхности, изменяется масса и сдвигается резонансная частота кристалла. Эти мельчайшие сдвиги необходимо измерять с помощью высокочастотной электроники (сложной, дорогой).
Небольшие колебания температуры приводят к аналогичным сдвигам частоты, что требует строгого контроля температуры окружающей среды. Разновидностью QMB является датчик SAW (поверхностных акустических волн), который также работает по принципу сдвига частоты.
Проводящие полимеры представляют собой полимеры, которые являются либо внутренне проводящими, либо непроводящими типами, которые были «нагружены» графитом. В первом типе проводимость может изменяться под воздействием летучих веществ. В последнем случае графит обеспечивает цепь электрического сопротивления, которую можно очень легко измерить. Когда молекулы газа связываются с полимером, он набухает, нарушая точки контакта между графитовыми частицами и тем самым изменяя сопротивление.
Когда молекулы газа связываются с полимером, он набухает, нарушая точки контакта между графитовыми частицами и тем самым изменяя сопротивление.
В этом случае изменения температуры также приведут к расширению/сжатию и, следовательно, к изменению сопротивления, поэтому для этого типа датчика также рекомендуется применять строгий контроль температуры окружающей среды.
Хотя возможные вариации полимеров огромны (и, следовательно, вариации массивов также огромны), они химически не очень стабильны. Сильные окислители, такие как хлор и озон, могут довольно легко разрушить полимер.
Датчики оксида металла
Основным датчиком является так называемый датчик на основе оксида металла (МОП) с микронагревом.
Некоторые оксиды металлов ведут себя как полупроводники при более высоких температурах. Датчики на его основе имеют нагревательный элемент и чувствительный элемент (спекшийся оксид металла с катализатором или без него). Оба элемента разделены очень тонкой изолирующей мембраной.
Окислительно-восстановительные реакции, происходящие на поверхности сенсора, приводят к изменению сопротивления, которое можно измерить. Эти окислительно-восстановительные реакции зависят от природы оксида металла/катализатора, реагирующего газа (газов) и температуры. Для нормальной работы требуется минимум 0,1% кислорода окружающей среды.
В зависимости от типа сенсора и температуры окислительно-восстановительную реакцию дает очень широкий спектр веществ. Заметными исключениями являются N2, CO2 (не окисляются дальше) и благородные газы, такие как гелий и аргон.
Текущий рынок
С 1980-х годов существует коммерческий рынок электронных носовых устройств, хотя и нишевый. В настоящее время лидером рынка является французская компания Alpha Mos, ориентированная на рынок очень дорогого и высокопроизводительного лабораторного оборудования.
Относительно более дешевые и портативные устройства Scensive Ltd (Bloodhound) и Smiths Detection (модели Cyranose), о которых часто сообщается в научной литературе, основаны на проводящих полимерных матрицах. Все современные устройства предназначены исключительно для использования в качестве лабораторных приборов, аналогичных ВЭЖХ/ГХ и спектрометрам. Все эти устройства должны быть индивидуально откалиброваны для конкретного применения.
Все современные устройства предназначены исключительно для использования в качестве лабораторных приборов, аналогичных ВЭЖХ/ГХ и спектрометрам. Все эти устройства должны быть индивидуально откалиброваны для конкретного применения.
Невозможно разработать приложение с использованием одного устройства, а затем применить эту модель к другому устройству того же типа без использования фактических калибровочных измерений с образцами того же типа.
Подход компании eNose
Философия компании eNose заключается не в том, чтобы конкурировать с существующим рынком специализированных лабораторий, а в том, чтобы ориентироваться на массовые рынки.
Это несуществующий в настоящее время сегмент недорогих, маломощных, массовых и массовых электронных носов. Цель состоит в том, чтобы создать крошечный электронный нос, работающий от батареи, с одинаковыми характеристиками от устройства к устройству, что позволит «откалибровать на одном устройстве, применить ко всем методам». Последнее требуется, чтобы сделать возможным массовое производство и массовое применение.
Последнее требуется, чтобы сделать возможным массовое производство и массовое применение.
Например, реальная цель состоит в том, чтобы иметь устройство, достаточно маленькое, чтобы его можно было встроить в мобильный телефон и распространять новые «запахи» (загружаемые калибровочные модели), которые можно разрабатывать независимо, не требуя какой-либо химической калибровки уже проданных мобильных телефонов.
Базовый модуль eNose
Рабочая лошадка и базовое ядро наших прикладных устройств eNose представляет собой автономный модуль в самой малой форме. Этот модуль имеет размеры 13,5×41,5 мм. Модуль содержит датчик с поддерживающей электроникой контроля и измерения температуры, микроконтроллер и оперативную и флэш-память. Модуль также имеет кремниевый чип серийного номера с уникальным идентификатором, который позволяет отслеживать и управлять каждым изготовленным модулем.
Микроконтроллер выполняет контроль температуры и калибровку нагревателя датчика, измеряет тепловые циклы в соответствии с настройками и буферизует измерения до тех пор, пока их можно будет выгрузить в центральное хранилище данных. Многочисленные настройки постоянно хранятся во встроенной ферростатической памяти (FRAM). Модуль связывается с хостом по системе последовательной шины.
Многочисленные настройки постоянно хранятся во встроенной ферростатической памяти (FRAM). Модуль связывается с хостом по системе последовательной шины.
На данный момент существует 5 типов датчиков с различным химическим составом, которые можно установить на модуль, что дает пять подтипов с одинаковой электроникой и встроенным программным обеспечением.
Термоциклирование
Как объяснялось в предыдущем разделе, окислительно-восстановительные реакции зависят от температуры. Это позволяет генерировать гораздо более конкретные узоры с помощью метода, называемого температурным циклированием. Это изображено на левом рисунке. В этом примере изображен синусоидальный температурный цикл с результирующими откликами датчика как функцией изменения температуры во времени. Временная ось одинакова для верхней и нижней частей рисунка. Различные вещества проявляют сильную реакцию при разных температурах для одного и того же типа химического датчика.
Взяв отклик полного цикла и нанеся график зависимости отклика от температуры, можно получить закономерности. Это показано на правом рисунке.
Это показано на правом рисунке.
Элегантность этого подхода заключается в том, что можно получить окислительно-восстановительные реакции, зависящие от температуры, на одном датчике. Относительная информация не зависит от устройства, как в случае массивов датчиков, используемых при статической температуре. Суть проблемы распознавания образов состоит в том, чтобы получить правильные значения фактической температуры во всех блоках/датчиках. Различия в производстве нагревательных элементов (даже с использованием МЭМС) могут привести к колебаниям температуры порядка ± 50 ° C между двумя датчиками одного типа.
Компания eNose разработала запатентованную уникальную методику автоматической калибровки температуры. При использовании этого метода стандартное отклонение межблочной вариации температуры составляет чуть менее 1°C. Это требование позволяет использовать модели калибровки, разработанные на одном устройстве, на другом «как есть» без изменений или химической настройки.
Анализ данных
Анализ данных является решающим фактором в любом устройстве электронного носа. Сложный характер измерений в сочетании с временными эффектами из-за механизмов выборки (таких как динамика воздействия/восстановления) создает многосторонние данные. Когда применяется метод термоциклирования 2.3, каждый датчик будет генерировать трехмерную матрицу времени (воздействия) по сравнению с тепловым циклом по сравнению со значением отклика. Когда для измерения образца используется комбинация сенсоров с различными химическими свойствами, химический состав сенсора формирует четвертое измерение многоходовых данных. Это показано в левой части рисунка ниже для системы с тремя датчиками A, B и C.
Классические многомерные методы распознавания образов требуют, чтобы одна измеренная выборка была представлена в виде одномерного вектора, дающего двумерную матрицу для набора данных в целом. Одно измерение матрицы представляет отдельные измерения, другое — элементы вектора, принадлежащего каждому измерению. Это показано в правой части рисунка, где каждая строка представляет один образец.
Это показано в правой части рисунка, где каждая строка представляет один образец.
Наивное развертывание трехмерных или четырехмерных данных для получения одномерного вектора невозможно, так как количество элементов результирующего вектора превысит количество измерений/выборок на порядки величины, что приведет к неразрешимая чрезмерная подгонка. Во многих случаях исследователи по необходимости прибегают к использованию лишь очень небольшого участка или даже одной точки данных измерений и таким образом теряют большую часть доступной информации. Таким образом, необходима форма предварительной обработки, которая генерирует одномерные векторы для каждого образца, сохраняя при этом важную информацию, необходимую для приложения.
Компания eNose разработала сложнейший гибридный алгоритм TUCKER3/PARAFAC, адаптированный к этому конкретному типу многосторонних данных. С помощью этого алгоритма полная информация, содержащаяся в измеренных данных, сохраняется при создании одномерных векторов для каждого измерения, в то же время элегантно удаляя избыточность, шум и информацию о масштабировании.

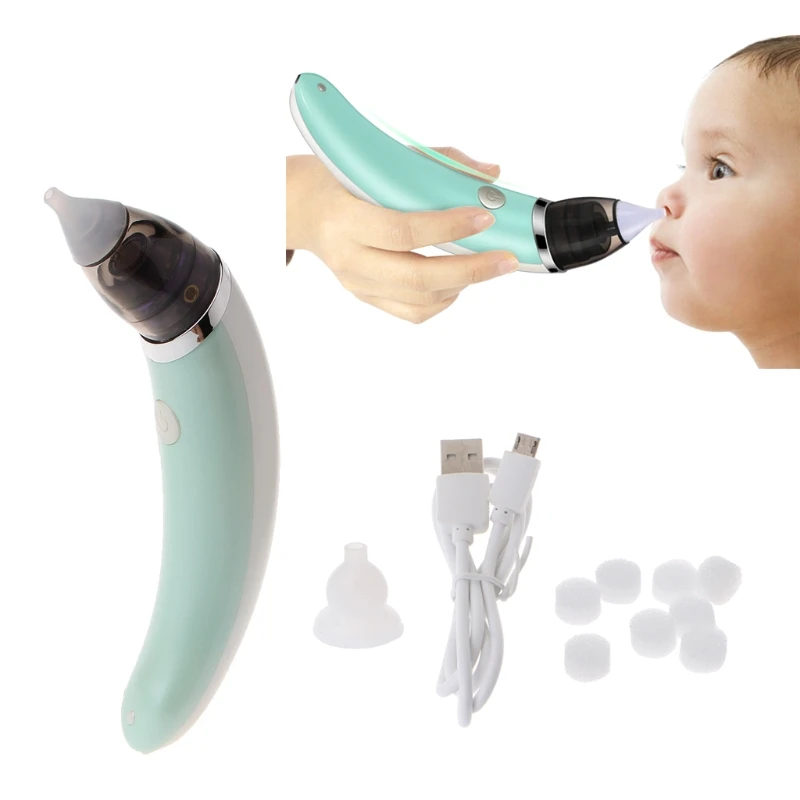 бесполезно.
бесполезно..jpg)
 Онкотаргет 2017; 8: 91593–91602. doi:10.18632/oncotarget.21335
Онкотаргет 2017; 8: 91593–91602. doi:10.18632/oncotarget.21335  Гастроэнтерология 2018; 154: С-599. doi:10.1016/S0016-5085(18)32176-0
Гастроэнтерология 2018; 154: С-599. doi:10.1016/S0016-5085(18)32176-0  Proc Natl Acad Sci USA 1971; 68: 2374–2376. doi:10.1073/pnas.68.10.2374
Proc Natl Acad Sci USA 1971; 68: 2374–2376. doi:10.1073/pnas.68.10.2374  doi:10.1088/1752-7155/9/4/046001
doi:10.1088/1752-7155/9/4/046001  Eur Respir J 2011; 38: 1301–1309. doi:10.1183/0
Eur Respir J 2011; 38: 1301–1309. doi:10.1183/0 Eur Arch Оториноларингол 2017; 274: 1053–1060. doi:10.1007/s00405-016-4320-y
Eur Arch Оториноларингол 2017; 274: 1053–1060. doi:10.1007/s00405-016-4320-y  Метаболиты 2019; 9: Е52. doi:10.3390/metabo
Метаболиты 2019; 9: Е52. doi:10.3390/metabo

 Eur Respir J 2017; 50: 1700919. doi:10.1183/13993003.00919-2017
Eur Respir J 2017; 50: 1700919. doi:10.1183/13993003.00919-2017 
 Исследование по электронной носовой диагностике рака легких. Рак легких 2010; 68: 170–176. doi:10.1016/j.lungcan.2009.11.003
Исследование по электронной носовой диагностике рака легких. Рак легких 2010; 68: 170–176. doi:10.1016/j.lungcan.2009.11.003 
 и др.
и др.