Содержание
Искусственная матка с ИИ-няней уже вынашивает несколько эмбрионов
02 февраля 2022
14:32
Ольга Мурая
В случае успеха этого эксперимента искусственная утроба позволит преодолеть проблему бесплодия.
Фото Pixabay.
Исследователи из КНР заявляют, что за этой технологией будущее вынашивания детей. Новая система не только обеспечивает жизнедеятельность «подопечных», но и способна предупреждать о возможных проблемах в развитии эмбрионов.
Ещё один популярный научно-фантастический сценарий превращается в реальность: китайские учёные заявили о создании «ИИ-няни», которая поможет выращивать эмбрионы в искусственной матке.
К слову, соответствующий аппарат, выполняющий функции материнского чрева, уже давно не предмет научной фантастики. Как и искусственные яйцеклетки и сперма.
Теоретически эту систему можно будет использовать, чтобы в будущем полностью освободить людей от бремени деторождения, а заодно повысить безопасность эмбрионального развития. Прекрасно это или ужасно — вопрос открытый.
Однако система пока находится на стадии разработки, и на решение этой этической проблемы у человечества ещё есть время.
А пока машина с ИИ-няней и несколькими искусственными матками, разработанная учёными из Сучжоуского института биомедицинской инженерии и технологий, уже «ухаживает» за эмбрионами мышей.
Этот процесс описан в исследовании, опубликованном в издании Journal of Biomedical Engineering 26 ноября 2021 года.
Эмбрионы содержатся в полностью искусственной матке, заполненной питательной жидкой средой, а их «няня» — роботизированный помощник, управляемый искусственным интеллектом.
Сложная система контейнеров с жидкостью, в которых развиваются эмбрионы, оснащена рядом регуляторов жидкости и системой подачи кислорода. Над контейнерами размещена камера, способная увеличивать изображения эмбрионов с впечатляющей детализацией.
Так ИИ-няня получает ключевую информацию о росте и развитии «подопечных». Система может отслеживать и записывать этапы процесса развития, никак не влияя при этом на жизнедеятельность эмбрионов.
Основываясь на этих данных, ИИ может даже различать эмбрионы по общему состоянию здоровья — если исследователям понадобится такая информация для какого-либо отбора.
Как заявляют разработчики, хотя потенциально такое устройство может «выходить» и человеческий эмбрион, международные законы в настоящее время запрещают такие эксперименты (что, впрочем, не останавливает некоторых учёных). Поэтому пока машина оптимизируется с использованием эмбрионов животных.
В настоящее время этот эксперимент проводится только на мышах, и пока нет никакой гарантии, что этот процесс будет когда-либо применим к человеческим эмбрионам.
Однако учёные пишут, что это устройство не только поможет лучше понять процесс зарождения жизни и эмбрионального развития человека, но и поможет выяснить причины врождённых дефектов и серьёзных проблем с репродуктивным здоровьем человека.
Напомним, ранее мы сообщали об успехе экспериментальной мужской беременности. Рассказывали мы и о том, что «мышиный эмбрион» удалось собрать прямо из стволовых клеток.
Также мы писали о том, что с помощью биопротеза яичников мыши смогли принести здоровое потомство, а ещё мы рассказывали об успешном использовании искусственной спермы.
Больше новостей из мира науки и медицины вы найдёте в разделах «Наука» и «Медицина» на медиаплатформе «Смотрим».
наука
медицина
беременность
роды
Китай/КНР
искусственный интеллект
матка
эмбрионы
общество
новости
Ранее по теме
Некоторые формы витамина К предотвращают смерть клеток
Российское приложение определит выгорание по ритму сердца
Хирурги пересадили пациенту ухо, выращенное из его собственных клеток
Российское аэротакси: с чего начать невероятную по окупаемости разработку
Паралич побеждён: помог искусственный спинной мозг
Внедрить бустеры сразу в вакцину пробуют учёные США
когда женщины перестанут вынашивать и рожать детей
Елизавета
Приставка
Новостной редактор
Исследователи считают, что в будущем человечество начнет развивать эмбрион вне матки: он сможет пройти процесс от оплодотворения до рождения без участия человека. «Хайтек» разбирается, как изменятся роды и беременность в будущем, а также что будет, если люди перестанут использовать свое тело для выращивания ребенка.
«Хайтек» разбирается, как изменятся роды и беременность в будущем, а также что будет, если люди перестанут использовать свое тело для выращивания ребенка.
Читайте «Хайтек» в
Сначала инкубатор, а потом биомешок и искусственная матка — так эволюционируют технологии, которые сохраняют плод и помогают ему развиться.
Как появилась идея не вынашивать детей, а выращивать их отдельно от организма матери?
Первая идея создать человеческий инкубатор появилась у акушера Стефан Тарнье в 1880 году: внешне конструкция напоминала деревянный ящик, в котором была специальная ячейка для хранения тары с теплой водой. Его назвали кювез. Простое устройство позволило уменьшить смертность среди младенцев почти в два раза.
Спустя 80 лет начались более серьезные эксперименты в этой области. Биологи хотели повторить функции человеческой матки, которая вынашивает плод. Для этого использовали эмбрионы кроликов, ягнят и коз. Исследователи решили, что так дешевле будет транспортировать ценный биоматериал с одного континента на другой.
Для этого использовали эмбрионы кроликов, ягнят и коз. Исследователи решили, что так дешевле будет транспортировать ценный биоматериал с одного континента на другой.
Оплодотворенные овечьи яйцеклетки имплантировали крольчихам, которых отправили из Англии в Южную Африку по цене всего лишь $8 за «пассажира». На месте эмбрионы подверглись еще одной пересадке — теперь уже в овечьи утробы. Спустя несколько месяцев родились несколько ягнят.
Но идея не закончилась успехом — плоды умирали от заражения, сбоев системы и множества других факторов.
Как работают современные инкубаторы?
Современные акушеры активно используют инкубаторы, без них не обходится ни одно учреждение родовспоможения. Такие инкубаторы могут следить за параметрами организма, круглосуточно отслеживать даже незначительные изменения в состоянии ребенка и температуру.
В инкубаторе дети могут находиться до трех-четырех месяцев. Устройство имитирует условия, которые максимально похожи на внутриутробные. Главное — создать оптимальную температуру для поддержания теплового обмена. Нельзя перегревать или переохлаждать ребенка.
Устройство имитирует условия, которые максимально похожи на внутриутробные. Главное — создать оптимальную температуру для поддержания теплового обмена. Нельзя перегревать или переохлаждать ребенка.
Современные акушеры активно используют инкубаторы, без них не обходится ни одно учреждение родовспоможения. Такие инкубаторы могут следить за параметрами организма, круглосуточно отслеживать даже незначительные изменения в состоянии ребенка и температуру
Что такое искусственная матка и биомешок?
Каким бы ни было отношение к беременности и родам, появление технологии искусственной матки, иначе говоря, эктогенеза, может полностью изменить его. Эта технология обещает множество медицинских преимуществ: женщины, у которых беременность протекает с осложнениями, получат возможность перенести плод в искусственную утробу и снизить риски для себя и ребенка. А недоношенные эмбрионы смогут продолжить свое развитие в искусственной матке и появиться на свет в положенный срок.
Исследователи создали биомешок и искусственную матку, чтобы продолжить жизнь плода вне утробы. Оба устройства работают похожим образом. Обычно это прототип искусственной матки, который использовали как внематочное устройство, где поддерживалась жизнь недоношенных плодов.
В 2017 году исследователи из США опубликовали работу, где заявили, что провели успешные испытания искусственной матки. В ней четыре недели выращивали недоношенных ягнят. По конструкции это пакет из пластика, который заполнен аналогом амниотической жидкости, иначе говоря, околоплодных вод. Кислород и другие необходимые вещества плод получает через пуповину.
Ученые перенесли недоношенных ягнят, которые были на 15-17-й неделе развития, в систему. В норме беременность у овец длится 21 неделю.
Есть ли аналогичные исследования в этой области?
Да, дальше всего в этом направлении продвинулись ученые из Израиля: они в 2021 году вырастили зародыши мышей — с работающими сердцем и мозгом — из пятидневных эмбрионов, состоящих всего из 250 клеток.
Исследователи вырастили эмбрионы мышей в стеклянных флаконах, наполненных питательной жидкостью. В состав этой жидкости входила сыворотка крови, взятая из пуповины человека. Стеклянные флаконы постоянно встряхивались, чтобы эмбрионы не прилипали к стенкам и не деформировались. Аппарат вентиляции подавал эмбрионам кислородную смесь под давлением. Прежде ученым никогда не удавалось вырастить эмбрионы до такого состояния без живой матки.
Сейчас исследователи думают, как провести подобный эксперимент с человеческим эмбрионом.
В 2019 году ученые из Нидерландов сказали, что им потребуется еще около 10 лет, чтобы создать первую искусственную матку.
В чем проблема искусственной матки и биомешка?
Пока что нельзя утверждать, что искусственную матку можно использовать для недоношенных детей. Одно из ограничений — уровень формирования мозга. Ранние эксперименты с ягнятами предполагали более высокий уровень развития мозга, поэтому в теории создать искусственную матку для ребенка будет гораздо сложнее, чем для животного. Также ягненок и ребенок имеют разный размер, поэтому устройство не будет универсальным.
Ранние эксперименты с ягнятами предполагали более высокий уровень развития мозга, поэтому в теории создать искусственную матку для ребенка будет гораздо сложнее, чем для животного. Также ягненок и ребенок имеют разный размер, поэтому устройство не будет универсальным.
К чему приведет искусственное выращивание детей?
Совершенствование биомешка и искусственной матки приведет к тому, что станет можно выращивать эмбрионы с самых ранних стадий. Это сделает ненужным естественный процесс беременности.
Ученые говорят, что такой формат может быть даже более безопасным для ребенка: например, исключается контакт плода с алкоголем и наркотиками, которые может принимать беременная женщина. Отпадет и необходимость в суррогатном материнстве.
Канадско-российский программист Виталик Бутерин, сооснователь криптопроекта Ethereum, предложил избавить женщин от «тяжкого бремени беременности» при помощи синтетических маток. Он сослался на статью Vox 2018 года, в которой говорится о заметном снижении доходов женщин после рождения первого ребенка:
Он сослался на статью Vox 2018 года, в которой говорится о заметном снижении доходов женщин после рождения первого ребенка:
Disparities in economic success between men and women are far larger once marriage+children enter the picture. Synthetic wombs would remove the high burden of pregnancy, significantly reducing the inequality.https://t.co/Zpin8tTlR6
— vitalik.eth (@VitalikButerin) January 18, 2022
Пока неизвестно, как повлияет на плод такая процедура вынашивания, возможно, определенный коктейль из гормонов, звуки извне, прикосновения к животу формируют здорового ребенка, а внутри искусственной матки он этого лишится. По подопытным животным (например, ягнятам) сложно отследить факторы, которые критически влияют на будущего человека.
Читать далее
Гиперзвуковой самолет на водороде развивает скорость до 12 Махов. Это почти 15 000 км/ч
Это почти 15 000 км/ч
Посмотрите на первый в мире одноступенчатый орбитальный корабль будущего
Самый большой в мире айсберг растаял. Ученые раскрыли, сколько воды он сбросил в океан
искусственных маток: грядущая эра бездетных родов?
С научной точки зрения это называется эктогенез , термин, введенный Дж.Б.С. Холдейн в 1924 году. Чрезвычайно влиятельный популяризатор науки, Холдейн сделал для своего поколения то, что Карл Саган сделал позже в том же столетии. Он заставлял людей думать и говорить о влиянии науки и техники на нашу цивилизацию, и для этого не стеснялся изобретать новые слова. Описывая эктогенез как беременность, происходящую в искусственной среде, от оплодотворения до рождения, Холдейн предсказал, что к 2074 году на это будет приходиться более 70 процентов человеческих рождений.
Возможно, его предсказание сбылось.
Обсуждая идею в своей работе Дедал — отсылка к изобретателю из греческой мифологии, который стремился своими изобретениями поднять людей до уровня богов, — Холдейн погрузился в вопросы своего времени, а именно евгенику и первые широкомасштабные дебаты о контрацепции и контроле над рождаемостью.
Подтвердится ли точка зрения Холдейна о конкретных сроках, когда эктогенез может стать популярным, или о количестве детей, рожденных таким образом, несомненно, что он был прав в том, что В то же время он был прав в том, что социальные последствия обязательно будут быть значительным по мере приближения возраста рождения без матери. Они не будут иметь тех же социальных последствий, которые были подчеркнуты в Дедал , однако.
Постепенное развитие технологий
Где мы сейчас находимся на пути к эктогенезу? Начнем с того, что за последние 20-30 лет прогресс определенно был быстрым. В середине 1990-х годов японским исследователям удалось в течение нескольких недель поддерживать зародыши коз в аппарате с искусственной амниотической жидкостью. В то же время в последние десятилетия наблюдается быстрый прогресс в области интенсивной терапии новорожденных, что отодвигает минимальный гестационный возраст, начиная с которого можно поддерживать жизнь человеческого плода. Сегодня существует возможность выжить недоношенному плоду при его удалении от матери в сроке гестации чуть менее 22 недель. Это чуть больше половины срока беременности (обычно 40 недель). И хотя спасение младенца, рожденного в такой ранний срок, требует сложного, дорогостоящего оборудования и ухода, возможности продолжают расти.
Сегодня существует возможность выжить недоношенному плоду при его удалении от матери в сроке гестации чуть менее 22 недель. Это чуть больше половины срока беременности (обычно 40 недель). И хотя спасение младенца, рожденного в такой ранний срок, требует сложного, дорогостоящего оборудования и ухода, возможности продолжают расти.
Всесторонний обзор, опубликованный Нью-Йоркской академией наук три года назад, освещает ряд достижений различных исследовательских групп, использующих среду матки ex vivo (вне тела) для поддержки плодов млекопитающих на ранних сроках беременности. По сути, быстро развиваются две области биотехнологии, которые потенциально могут обеспечить эктогенез у людей, и, попутно, то, что авторы обзора Академии называют частичным эктогенезом .
Поскольку плод существенно развивается в отношении внешней формы и внутренних органов во второй половине беременности, наша нынешняя способность рожать и поддерживать недоношенных детей фактически является своего рода частичным эктогенезом. При поддержке всего оборудования в отделении интенсивной терапии новорожденных (ОИТН) недоношенный ребенок продолжает свое развитие, как и нормальный плод того же гестационного возраста внутри матки матери, но с одним важным исключением. В матку поступает насыщенная кислородом кровь, а кровь, несущая отходы, выходит через плаценту и пуповину. Однако после родов недоношенный ребенок должен дышать через легкие, очищать кровь печенью и почками и получать питание через желудочно-кишечный тракт.
При поддержке всего оборудования в отделении интенсивной терапии новорожденных (ОИТН) недоношенный ребенок продолжает свое развитие, как и нормальный плод того же гестационного возраста внутри матки матери, но с одним важным исключением. В матку поступает насыщенная кислородом кровь, а кровь, несущая отходы, выходит через плаценту и пуповину. Однако после родов недоношенный ребенок должен дышать через легкие, очищать кровь печенью и почками и получать питание через желудочно-кишечный тракт.
Но поскольку эти системы органов, особенно легкие, на самом деле не готовы выполнять свою работу так рано, существует предел того, насколько рано развивающийся плод может быть перенесен из матки в отделение интенсивной терапии. Этот предел, известный как жизнеспособность, определенно был отодвинут благодаря специальным процедурам, которые применялись к матери до родов и сразу после рождения непосредственно в легкие недоношенного ребенка, а также при интенсивной поддержке. Но 22-недельный срок беременности может быть абсолютным пределом выживания плода, который должен будет зависеть от дыхания легкими, не говоря уже о других органах, а не от питаемой кровью матери.
Тем не менее, возможность расширить границы не за горами. Одной из двух разрабатываемых ключевых технологий является среда, наполненная искусственной амниотической жидкостью, которая продолжала развиваться с моделями лабораторных животных после работы с козами в 1990-х годах. Другая область — перенос эмбрионов. Мало того, что развивающееся млекопитающее может быть перенесено из матки его собственной матери в матку суррогатной матери, но постепенно исследователи воспроизводят эндометрий — клеточный слой матки, который содержит и питает беременность — в виде клеточной культуры или in vitro модель . Конвергенция этих технологий позволит перевести развивающегося человека в систему, включающую плаценту и пуповину и поставляющую все расходные материалы (кислород и пищу) и выводящую все отходы непосредственно через кровь.
Таким образом, выживание и дальнейшее развитие не будут зависеть от готовности легких и других органов выполнять свою работу. Применение такой системы к плоду, родившемуся в середине беременности, представляет собой настоящий частичный эктогенез.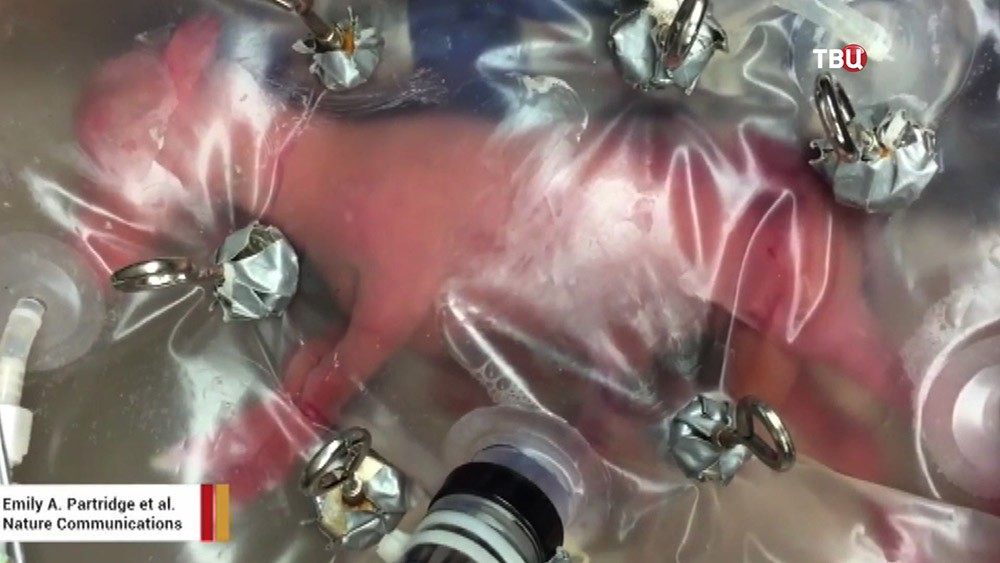 Кроме того, поскольку шунтирование развивающихся, не полностью функциональных органов может существенно улучшить выживаемость и может даже снизить затраты на крайние преждевременные роды, перемещение технологии из области исследований в клинику неизбежно.
Кроме того, поскольку шунтирование развивающихся, не полностью функциональных органов может существенно улучшить выживаемость и может даже снизить затраты на крайние преждевременные роды, перемещение технологии из области исследований в клинику неизбежно.
Как только это произойдет, не будет никаких препятствий для дальнейшего расширения границ, к полному эктогенезу. Но не будет никаких препятствий для раздвигания границ, подобно тому, как жизнеспособность легких стала препятствием для обычного досрочного ухода. В какой-то момент оплодотворенную in vitro яйцеклетку можно было посадить прямо в искусственную матку, и натуральная матка не требовалась даже на ранних стадиях.
Социальные последствия
Искусственная матка может звучать футуристично, и во времена Холдейна это, возможно, поддерживало представление о том, что реализация технологии будет сопровождаться контролем над рождаемостью и евгеникой, контролирующей, какие люди оживают и, следовательно, какие генетические черты приобретают передаются будущим популяциям. Но сегодня мы могли бы делать все это без эктогенеза. У нас есть множество методов контрацепции, и мы можем стерилизовать людей или сделать их более плодовитыми, в то время как беременность может быть вызвана имплантированными эмбрионами, полученными с помощью экстракорпорального оплодотворения.
Но сегодня мы могли бы делать все это без эктогенеза. У нас есть множество методов контрацепции, и мы можем стерилизовать людей или сделать их более плодовитыми, в то время как беременность может быть вызвана имплантированными эмбрионами, полученными с помощью экстракорпорального оплодотворения.
Если кто-то в настоящее время работает над евгенической программой, он может использовать суррогатных матерей и на самом деле не нуждается в искусственной матке — если только мы не представляем себе общество, которое регулярно и принудительно стерилизует всех женщин, так что тот, у кого есть искусственная матка, монополия на воспроизводство, эктогенез не имеет особого отношения к проблемам 1920-х годов. Вместо этого искусственная матка просто перемещала беременность за пределы тела женщины. При рассмотрении социальных последствий это главный фактор, который мы должны иметь в виду, и при этом мы видим, что он действительно имеет отношение ко многим спорным в настоящее время вопросам.
Принимая во внимание, например, аборт, хотя утверждение о том, что плод, даже эмбрион, является личностью, имеющей «право на жизнь», является религиозным верованием, которое не может быть навязано всем остальным, основным аргументом в пользу права выбора является право женщины распоряжаться своим телом. Если развивающийся эмбрион или плод нежизнеспособен и мать хочет, чтобы он вышел из матки, это ее право.
Если развивающийся эмбрион или плод нежизнеспособен и мать хочет, чтобы он вышел из матки, это ее право.
Но что произойдет, когда у нас появится технология, позволяющая удалить его из нее, не убивая, и позволить беременности продолжаться в искусственной матке? Уже сейчас, когда технологии отделений интенсивной терапии отодвигают предел выживания, сроки жизнеспособности, влияющие на законность аборта, были оспорены противниками абортов. Перспектива эктогенеза может поставить проблему жизнеспособности с ног на голову, и будет интересно посмотреть, к чему это приведет.
В то время как социальные консерваторы могут быть восприимчивы к тому, что искусственная матка может сделать с парадигмой аборта, не заблуждайтесь, они, вероятно, не будут рады тому, что технология также может значительно облегчить мужчинам-гей-парам рождение детей. Все, что им нужно, это донор яйцеклеток; суррогатной матери больше не нужно брать эмбрион в свою матку и вынашивать его в течение 40 недель. Это проще для любой гей-пары с точки зрения практичности, сроков ожидания и денег. То же самое касается трансгендерного человека, желающего иметь ребенка.
То же самое касается трансгендерного человека, желающего иметь ребенка.
Наконец, из-за огромного количества искусственная матка может иметь серьезные последствия для гетеросексуальных женщин с полностью функциональной маткой. Многие, кто хочет собственных детей, могут предпочесть отказаться от беременности, но не будут нанимать суррогатную мать. Это не только дорого, но и суррогатная мать может полюбить вынашиваемый ею плод, так зачем рисковать?
С другой стороны, мышление могло бы быть совсем другим, если бы суррогатная мать была высокотехнологичной банкой. Это ваш ребенок, не беспокойтесь о конкурирующих матерях. Я не утверждаю, что все потенциальные матери выберут это, но догадка Холдейна может быть не такой уж нереалистичной, поскольку в конечном итоге она может составить значительную часть населения.
Дэвид Уормфлэш — астробиолог, врач и научный писатель. Подпишитесь на @CosmicEvolution, чтобы прочитать, что он говорит в Твиттере.
Эта статья ранее публиковалась в GLP 12 июня 2015 г. когда-либо было возможно.
когда-либо было возможно.
By
- Антонио Регаладоархив стр.
17 марта 2021 г.
Одни только фотографии рассказывают фантастическую историю — мышиный эмбрион с бьющимися сердечными клетками, головой и зачатками конечностей, живой и растущий в стеклянной банке.
По словам научной группы в Израиле, которая сделала снимок, исследователи выращивали мышей в искусственной матке в течение 11 или 12 дней, что составляет примерно половину естественного периода беременности животного.
Это рекорд развития млекопитающего вне матки, и, по мнению исследовательской группы, человеческие эмбрионы могут стать следующими, что поднимает огромные новые этические вопросы.
«Это готовит почву для других видов», — говорит Джейкоб Ханна, специалист по биологии развития из Научного института Вейцмана, возглавлявший исследовательскую группу. «Я надеюсь, что это позволит ученым выращивать человеческие эмбрионы до пятой недели».
Выращивание человеческих эмбрионов в лаборатории в течение столь долгого времени, глубоко в первом триместре, поставило бы науку на путь столкновения с дебатами об абортах. Ханна считает, что выращенные в лаборатории эмбрионы могут стать исследовательской заменой ткани, полученной в результате абортов, и, возможно, также источником тканей для лечения.
Как они это сделали
Команда Ханны удлинила эмбрионы мышей, добавляя сыворотку крови из пуповины человека, перемешивая их в стеклянных банках и накачивая смесью кислорода под давлением. Ханна сравнивает этот процесс с помещением пациента с COVID-19 на аппарат искусственной вентиляции легких.
«Это нагнетает кислород в клетки», — говорит он. «Тогда пациент намного счастливее. Вы можете видеть, что у него есть кровеносная система, и все основные системы органов работают».
На видео, снятом исследователями Института науки Вейцмана, показаны мышиные эмбрионы с бьющимся сердцем. Лаборатория расширяет возможности выращивания эмбрионов в лаборатории.
Эмбрионы мышей погибли только после того, как стали слишком большими, чтобы через них мог диффундировать кислород, поскольку у них отсутствует естественное кровоснабжение, которое может обеспечить плацента.
Работа открывает научное окно на ранний эмбрион, который обычно скрыт внутри матки. В сегодняшней публикации в журнале Nature израильская команда описывает серию экспериментов, в которых они добавляли токсины, красители, вирусы и человеческие клетки к развивающимся эмбрионам мышей, чтобы изучить, что произойдет.
«Это проявление силы — очень, очень впечатляющее», — говорит Альфонсо Мартинес Ариас, биолог развития и исследователь стволовых клеток из Университета Помпеу Фабра в Испании, который не участвовал в исследовании.
Далее: люди
Ханна говорит, что ученые захотят развивать человеческие эмбрионы таким же образом. Он признает, что изображения выращенных в лаборатории человеческих эмбрионов с примерно узнаваемой формой — головой, хвостом и зачатками конечностей — могут шокировать. Человеческий эквивалент 12-дневных мышей Ханны был бы эмбрионом первого триместра.
Человеческий эквивалент 12-дневных мышей Ханны был бы эмбрионом первого триместра.
«Я понимаю трудности. Я понимаю. Вы вступаете в область абортов», — говорит Ханна. Однако он говорит, что может рационализировать такие эксперименты, потому что исследователи уже изучают пятидневные человеческие эмбрионы из клиник ЭКО, которые также разрушаются в этом процессе.
«Поэтому я бы советовала выращивать его до 40-го дня, а затем утилизировать», — говорит Ханна. «Вместо того, чтобы получать ткань от абортов, давайте возьмем бластоцисту и вырастим ее».
Исследование является частью взрыва новых методов и идей для изучения раннего развития. Сегодня в том же номере журнала Nature две другие исследовательские группы сообщают о прорыве в создании «искусственных» человеческих эмбрионов.
Этим командам удалось уговорить обычные клетки кожи и стволовые клетки самостоятельно собраться в похожие на них ранние человеческие эмбрионы, которые они назвали «бластоиды», которые они выращивали в течение примерно 10 дней в лаборатории.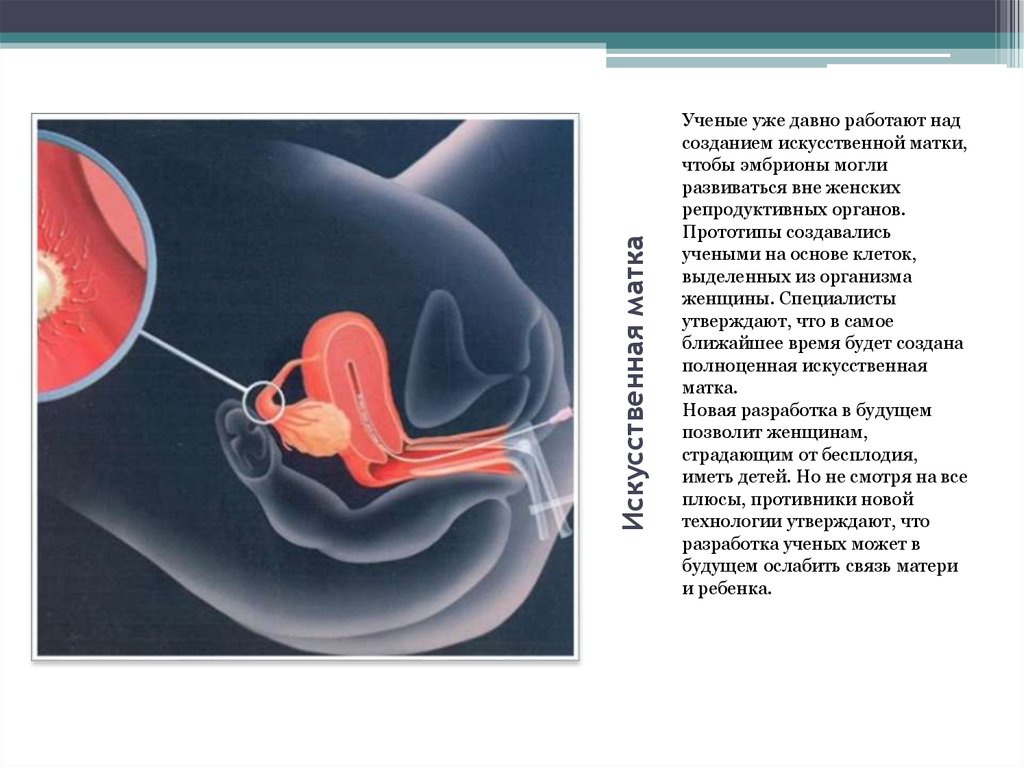 Ранее было описано несколько видов искусственных моделей эмбрионов, но те, которые описаны сегодня, являются одними из наиболее полных, поскольку они содержат клетки, необходимые для образования плаценты. Это означает, что они на шаг ближе к тому, чтобы стать жизнеспособными человеческими эмбрионами, которые могут развиваться дальше, вплоть до рождения.
Ранее было описано несколько видов искусственных моделей эмбрионов, но те, которые описаны сегодня, являются одними из наиболее полных, поскольку они содержат клетки, необходимые для образования плаценты. Это означает, что они на шаг ближе к тому, чтобы стать жизнеспособными человеческими эмбрионами, которые могут развиваться дальше, вплоть до рождения.
Ученые говорят, что они никогда не попытались бы установить беременность с помощью искусственных эмбрионов — действие, которое сегодня было бы запрещено в большинстве стран.
Вместо этого, говорит Ханна, очевидным следующим шагом было бы добавить эти модели эмбрионов в его систему вращающихся сосудов и посмотреть, насколько дальше они смогут развиваться. «Потребовалось шесть лет очень напряженной работы, чтобы довести эту систему до того состояния, в котором она находится, — говорит Ханна. «У нас есть цель сделать это и с синтетическими эмбрионами».
Первые дни
На данный момент технология искусственной матки остается «сложной и дорогой», говорит Мартинес Ариас. Он не верит, что многие другие лаборатории смогут его использовать, что ограничит его влияние в краткосрочной перспективе, и он не поддерживает выращивание человеческих эмбрионов таким образом: «Это дорого и сложно, поэтому мы должны увидеть, насколько это полезно». является.»
Он не верит, что многие другие лаборатории смогут его использовать, что ограничит его влияние в краткосрочной перспективе, и он не поддерживает выращивание человеческих эмбрионов таким образом: «Это дорого и сложно, поэтому мы должны увидеть, насколько это полезно». является.»
Технология «мышь в банке» нуждается и в других улучшениях, — говорит Ханна. Ему не удалось вырастить мышей, начиная с оплодотворенной яйцеклетки, вплоть до 12-го дня. Вместо этого он собрал 5-дневные эмбрионы беременных мышей и переместил их в систему инкубатора, где они прожили еще неделю.
Проблема в том, что в настоящее время мышиные эмбрионы развиваются правильно только в том случае, если их можно прикрепить к настоящей мышиной матке, по крайней мере, на короткое время. Команда Ханны работает над адаптацией процедуры, чтобы они могли полностью развивать мышей в лабораторных условиях.
Ханна говорит, что он не заинтересован в доведении мышей до срока в лаборатории. Его цель — наблюдать и манипулировать ранним развитием. «Я хочу посмотреть, как будет развиваться программа, — говорит он. «Мне есть чему учиться».
«Я хочу посмотреть, как будет развиваться программа, — говорит он. «Мне есть чему учиться».
Запрещено?
Долгосрочные исследования живых человеческих эмбрионов, развивающихся в лаборатории, в настоящее время запрещены в соответствии с так называемым правилом 14 дней, руководящим принципом (и законом в некоторых странах), согласно которому эмбриологам запрещается выращивать человеческие эмбрионы более две недели.
Тем не менее, ключевая научная организация, Международное общество исследований стволовых клеток, или ISSCR, планирует рекомендовать отменить запрет и позволить некоторым эмбрионам расти дольше.
Ханна говорит, что это означает, что он может выращивать человеческие эмбрионы в своем инкубаторе — до тех пор, пока израильский совет по этике подпишет его, что, по его мнению, они сделают.
«Как только правила будут обновлены, я смогу подать заявку, и она будет одобрена. Это очень важный эксперимент», — говорит Ханна. «Нам нужно увидеть, как человеческие эмбрионы гаструлируют и формируют органы, и начинают его тревожить.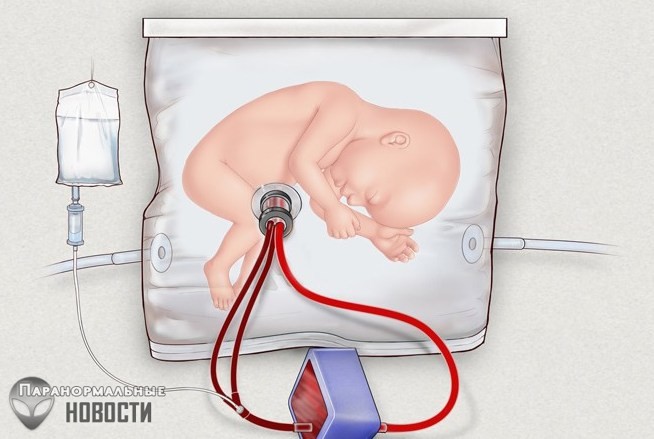 Польза от выращивания человеческих эмбрионов до третьей, четвертой и пятой недель неоценима. Я думаю, что эти эксперименты следует, по крайней мере, рассмотреть. Если мы сможем добраться до развитого человеческого эмбриона, мы сможем многому научиться».
Польза от выращивания человеческих эмбрионов до третьей, четвертой и пятой недель неоценима. Я думаю, что эти эксперименты следует, по крайней мере, рассмотреть. Если мы сможем добраться до развитого человеческого эмбриона, мы сможем многому научиться».
Система вращающихся бутылок, разработанная в Израиле, может поддерживать жизнь эмбрионов мышей вне матки. Эмбрионы подвергаются воздействию кислорода под давлением в течение нескольких дней.
Ханна говорит, что для того, чтобы сделать такие эксперименты более приемлемыми, можно изменить человеческие эмбрионы, чтобы ограничить их потенциал для полного развития. Одной из возможностей было бы установить генетические мутации в кальциевом канале, чтобы сердце никогда не билось.
Я спросил Ханну, обращался ли он за советом к специалистам по этике или религиозным деятелям. Он сказал, что нет. Вместо этого он ожидает совета своего профессионального органа и разрешения на этические вопросы в своем университете.
«ISSCR — мой раввин», — говорит он.
Выращивание человеческих эмбрионов в банках может найти неожиданное практическое применение. Уильям Херлбут, врач и биоэтик из Стэнфордского университета, говорит, что система предлагает ему способ получения примитивных органов, таких как клетки печени или поджелудочной железы, из человеческих эмбрионов первого триместра, которые затем можно выращивать дальше и использовать в трансплантационной медицине. Ханна соглашается, что это потенциальное направление развития технологии.
«Граница науки перемещается от молекул и пробирок к живым организмам», — говорит Херлбут. «Я не думаю, что извлечение органов — это так уж надуманно. В конце концов, оно могло туда попасть. Но это очень чревато, потому что граница одного человека не является границей другого человека».
Антонио Регаладо
Глубокое погружение
Биотехнологии
Оставайтесь на связи
Иллюстрация Роуз Вонг
Узнайте о специальных предложениях, главных новостях,
предстоящие события и многое другое.