Содержание
Удар для любителей нефти: два шага к новой энергетике
- Технологии
- Алексей Алексенко
Автор
Фото Getty Images
Недавние технологические разработки приблизили использование искусственного фотосинтеза для получения чистой энергии
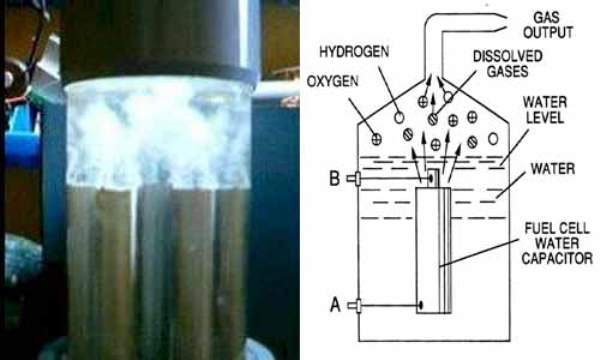
Сразу две исследовательские группы объявили о серьезных успехах на пути к искусственному фотосинтезу — процессу, при котором вода расщепляется солнечным светом с образованием водорода и кислорода. Водород и кислород при этом образуют эффективное и экологически чистое топливо: при их реакции образуется опять же вода. Немецкие исследователи разработали эффективный катализатор, обеспечивающий разложение воды. Тем временем ученые из британского Кембриджа предложили систему полуискусственного фотосинтеза с использованием отдельных элементов живых организмов.
Водород и кислород при этом образуют эффективное и экологически чистое топливо: при их реакции образуется опять же вода. Немецкие исследователи разработали эффективный катализатор, обеспечивающий разложение воды. Тем временем ученые из британского Кембриджа предложили систему полуискусственного фотосинтеза с использованием отдельных элементов живых организмов.
Закончили чтение тут
Почти вся энергия, используемая человечеством, поступает к нам от Солнца (исключение — энергия распада урана, которая идет от другого источника — давно потухших звезд). Именно энергия Солнца заключена во всех видах ископаемого топлива: ее запасли для нас живые организмы прежних эпох.
Живая природа выработала исключительно эффективный способ использовать энергию Солнца — фотосинтез. Прилетевший от Солнца фотон растения и цианобактерии используют, чтобы разбить молекулу воды на кислород и водород. Кислород они тут же выбрасывают, а водород в конечном счете используют для того, чтобы обвешать им молекулу углекислого газа, превратив ее в органику. Эту самую органику, то есть энергию химических связей между углеродом и водородом, человечество и использует, сжигая ископаемое топливо или непосредственно части растений (например, древесину).
Кислород они тут же выбрасывают, а водород в конечном счете используют для того, чтобы обвешать им молекулу углекислого газа, превратив ее в органику. Эту самую органику, то есть энергию химических связей между углеродом и водородом, человечество и использует, сжигая ископаемое топливо или непосредственно части растений (например, древесину).
Синтез органики из углекислого газа, воды и солнечного света — процесс, который удается растениям так хорошо, что людям нет никакого смысла его копировать: достаточно просто посадить побольше лесов. Однако инженеров очень привлекает другая возможность: если не доводить природный процесс до конца, а остановить его на стадии расщепления воды, можно запасать солнечную энергию в виде водорода и кислорода. Водород и кислород по отдельности выделяют многие микроорганизмы, но вот объединить эти процессы для обеспечения собственной энергетики живая природа не додумалась (она нашла для этого более изысканные и безопасные химические реакции). Между тем такой технологический процесс мог бы многократно покрыть все сегодняшние энергетические потребности человечества.
Между тем такой технологический процесс мог бы многократно покрыть все сегодняшние энергетические потребности человечества.
Йохен Фельдман и Яцек Столарчик из Мюнхена, а также Франк Вюртнер из Вюрцбурга решили важнейшую проблему: как эффективно разделить воду на водород и кислород и не дать им соединиться обратно. Их подход основан на довольно традиционной технологии использования полупроводников. После поглощения фотона в полупроводнике создается пара из электрона и положительно заряженной «дырки». Электрон используется для того, чтобы «восстановить» из воды водород. В прежних инженерных решениях «дырки» старались как можно быстрее удалить из полупроводника с помощью химических реагентов, и таким образом вторая, более медленная часть реакции — «окисление» кислорода «дыркой» — оставалась неосуществленной.
Зачем нам использовать наработки древних растений, если мы сами научимся делать то же, что и они, — только лучше?
Эту проблему и решили исследователи. В их системе две половинки реакции протекают на одной наночастице, хоть и разнесены в пространстве. Наночастицы представляют собой стержни из полупроводника, сульфата кадмия. На концы стержней нанесены частицы платины, которая служит акцептором для возбужденных электронов. Там и происходит реакция восстановления водорода. Тем временем на боковые поверхности стержней нанесен разработанный исследователями катализатор на основе рутения: он обеспечивает исключительно быструю доставку «дырок» к ионам кислорода. Скорость особенно важна, поскольку «дырки» химически активны и быстро разрушают катализатор. В итоге две части реакции катализируются одним типом наночастиц, и происходит полное расщепление воды на кислород и водород в одну стадию.
В их системе две половинки реакции протекают на одной наночастице, хоть и разнесены в пространстве. Наночастицы представляют собой стержни из полупроводника, сульфата кадмия. На концы стержней нанесены частицы платины, которая служит акцептором для возбужденных электронов. Там и происходит реакция восстановления водорода. Тем временем на боковые поверхности стержней нанесен разработанный исследователями катализатор на основе рутения: он обеспечивает исключительно быструю доставку «дырок» к ионам кислорода. Скорость особенно важна, поскольку «дырки» химически активны и быстро разрушают катализатор. В итоге две части реакции катализируются одним типом наночастиц, и происходит полное расщепление воды на кислород и водород в одну стадию.
Ученые из Кембриджа придерживались другого подхода: они объединили в одном дизайне инженерные технологии человека и компоненты природных живых систем. Получившийся в результате процесс преподнес исследователям сюрприз: он позволил использовать энергию солнечного света даже более эффективно, чем это делает природный фотосинтез в растениях.
Преимущества полуискусственного фотосинтеза в том, что для него не нужны дорогие и токсичные катализаторы, ограничивающие возможности полностью искусственных систем, вроде описанной выше. С другой стороны, полуискусственные процессы, возможно, вскоре удастся масштабировать до промышленного уровня.
Авторы использовали молекулярное оборудование природной фотосистемы II, добавив к нему фермент гидрогеназу из водорослей, восстанавливающий протоны до водорода. В природном фотосинтезе ничего подобного не происходит, так как выделяющиеся при расщеплении воды протоны сразу же вовлекаются в другие биохимические процессы. Однако исследователям удалось совместить две биологические реакции, в обычных условиях разобщенные: работу фермента гидрогеназы и расщепление воды фотосистемой II. Оба «живых» компонента фиксировали на фотоаноде, покрытом особым красителем. В результате природный процесс был оптимизирован: вместо кислорода и восстановленной из СО2 органики модифицированный фотосинтез стал давать просто кислород и водород — два вещества, на которых, возможно, будет базироваться «зеленая» энергетика будущего.
Появление на протяжении одной недели сразу двух научных работ, с разных сторон атакующих проблему искусственного фотосинтеза, свидетельствует, что этой технологии, возможно, нам не так уж долго ждать. О том, как это достижение изменит все без исключения промышленные технологии, пока можно только догадываться, но оно несомненно будет означать конец эры ископаемого топлива. Зачем нам использовать наработки древних растений, если мы сами научимся делать то же, что и они, — только лучше?
Алексей Алексенко
Автор
#альтернативная энергетика
Рассылка Forbes
Самое важное о финансах, инвестициях, бизнесе и технологиях
Почему мы до сих пор не умеем делать воду — и как научиться ее беречь
Лето — разве не идеальное время, чтобы бросить побольше льда в лимонад, наполнить бассейн и почаще принимать долгий, освежающий душ? Если коротко — то нет.
На самом деле, когда мы все наслаждаемся прекрасной погодой, легко забыть о важности экономии воды. Но разве не было бы проще, если бы мы могли просто делать воду с нуля? В конце концов, сегодня мы можем изготавливать самые разнообразные вещи — от бриллиантов до бургеров.
Н-2-О нет!
Теоретически, сделать воду должно быть легко. Надо лишь взять два атома водорода и соединить с атомом кислорода — разве это может быть сложно? Оказывается, может — и даже очень.
Просто смешав водород с кислородом, воду вы не получите — для того, чтобы их соединить, нужна энергия. Проблема с добавлением в это уравнение энергии заключается в том, что масштабная химическая реакция легковоспламеняющегося водорода и кислорода (который как раз и поддерживает горение) может привести к довольно большому взрыву. Поэтому опасности в этой затее больше, чем пользы.
- «Безглютеновая вода» и другие маркетинговые стратегии
- Питьевая вода на планете загрязнена пластиком — обзор СМИ
- Руки мыли? Правильно ли мы делаем это
Если мы не можем просто сделать воду из ее атомов, есть ли другие способы ее создать? В последнее время ученые сосредотачиваются на получении воды из воздуха и использовании для этого влажности. К сожалению, большинство таких исследований находятся на ранних стадиях и проводятся в небольших масштабах. То есть, бороться с нехваткой воды и засухой таким образом сейчас, безусловно, нельзя.
К сожалению, большинство таких исследований находятся на ранних стадиях и проводятся в небольших масштабах. То есть, бороться с нехваткой воды и засухой таким образом сейчас, безусловно, нельзя.
Настоящая жажда
Однако засуха — не единственная причина, почему мы работаем над тем, чтобы научиться делать воду. Население Земли постоянно увеличивается — и спрос на воду также растет.
Кроме того, в мире до сих пор есть места, где нет доступа к чистой воде. Хотя около 71% поверхности Земли — это вода, большая ее часть — это соленая вода, то есть не питьевая. Лишь 2% воды на Земле является пресной и безопасной для питья, и более половины ее находится в полярных ледяных шапках, откуда мы не можем ее получить. В то же время много чистой, питьевой воды мы теряем просто потому, что воспринимаем ее как должное.
Нам так легко получить воду у себя дома и на работе, что мы забываем, что это ограниченный ресурс и однажды он, вполне вероятно, закончится. По всем этим причинам поиск новых способов создания воды становится все более актуальным.
По всем этим причинам поиск новых способов создания воды становится все более актуальным.
Голубая планета №2?
Підпис до фото,
Можем ли мы добывать воду на других планетах?
Ученые заинтересованы не только в создании и сборе воды на Земле. На самом деле, их исследования распространяются на самые удаленные уголки космоса. Сейчас астронавты NASA полагаются на свою Систему восстановления воды (Water Recovery System) для переработки водорода и углекислого газа в космосе для получения воды (и метана). В космосе у них нет дождя и водоемов, которые есть здесь у нас, поэтому количество воды еще более ограничено. Было бы почти идеально, если бы мы могли брать воду из космоса — но насколько это реально?
- На Марсе нашли озеро. С водой
В прошлом году ученые обнаружили доказательства наличия льда на так называемой темной стороне Луны. Ранее подобные образования льда находили и на других планетах, например на Меркурии. Не трудно представить, как сильно это взволновало научное сообщество. Возможность брать воду с Луны и других планет не только открывает водные ресурсы за пределами Земли, но также дает возможность дальнейшего исследования космоса.
Не трудно представить, как сильно это взволновало научное сообщество. Возможность брать воду с Луны и других планет не только открывает водные ресурсы за пределами Земли, но также дает возможность дальнейшего исследования космоса.
Но лед — не единственный водный ресурс в космосе. На Марсе есть ряд возможных источников воды — нам просто нужно найти способ ее добычи. Например, воду можно было бы собирать из атмосферы, из почвы или даже добывать из полезных ископаемых — возможности бесконечны. К сожалению, наши технологии еще не настолько развиты.
А может, начать с того, чтобы беречь то, что имеем?
Поэтому, возможно, вода — это не столь ограниченный ресурс, как мы считали изначально. Но пока возможность получать воду в глобальном или даже планетарном масштабе все еще недоступна.
- Зачем люди пьют неочищенную «сырую» воду и безопасно ли это?
Так что же мы можем сделать для сохранения воды, которая уже есть? Самое главное — не воспринимать воду как должное. Вот пять полезных советов, которые помогут вам уменьшить количество потребляемой воды:
Вот пять полезных советов, которые помогут вам уменьшить количество потребляемой воды:
- Не принимайте душ слишком долго. В жаркую погоду понятно желание принимать душ чаще. Однако, когда вы его принимаете, делайте это недолго, или даже замените долгий душ частично наполненной ванной.
- Не оставляйте кран открытым, когда в этом нет необходимости. Чаще всего так происходит, когда вы чистите зубы или умываетесь — но подумайте, что вся эта вода просто стекает в канализацию!
- Используйте стиральную или посудомоечную машины только с полной загрузкой. Одна полная загрузка экономит гораздо больше воды, чем две или три частичных.
- Не поливайте газон и растения избыточно. А также поливайте их в прохладное время суток — например, вечером вода не испаряется на солнце, поэтому расходуется меньше.
- Держите бутылку с водой в холодильнике, а не ждите, пока из крана потечет холодная.

В среднем человек использует около 9 000 литров воды в год — этого достаточно для наполнения двух бензиновых цистерн! Еще страшнее думать, что, по прогнозам, к 2025 году более 60% людей будут иметь ограниченный доступ к пресной воде.
Даже самая незначительная экономия воды может иметь огромное значение — если в ней будет участвовать большое количество людей.
Следите за нашими новостями в Twitter и Telegram
Методы расщепления воды, которые могут подпитывать промышленность и города
Исследователи проекта SafeFlame используют стандартное сетевое электричество для расщепления воды на кислород и водород, а затем воссоединяют их на кончике паяльной лампы, чтобы получить пламя. Поскольку их горелка генерирует собственное топливо по требованию, она устраняет необходимость в легковоспламеняющихся газах, таких как ацетилен, которые необходимо хранить в топливных баллонах и которые опасны при транспортировке из-за их взрывоопасной природы.
Имеется много сообщений о человеческих травмах и смертях из-за небезопасной транспортировки или хранения ацетиленовых топливных баллонов, особенно при перевозке в кузове инженерного фургона. «Небольшая утечка и взрыв — газ можно воспламенить, просто открыв дверь фургона с помощью дистанционного ключа или включив двигатель», — сказал Дерек Дэвис, технический консультант проекта SafeFlame, финансируемого ЕС, который должен завершиться в конец октября. «Таких историй полно».
»
«Это новое безопасное пламя из воды, которое полностью отличается от любого из существующих методов создания пламени для коммерческого использования».
Дерек Дэвис, технический консультант, SafeFlame
раз дешевле, чем при использовании комбинации газов кислорода и ацетилена, и имеет меньшие затраты на страхование, так как исключается риск взрыва. Это означает, что технология может применяться в ряде приложений, использующих пламя, в таких различных отраслях, как кондиционирование воздуха, автомобильные компоненты, обработка стекла, железнодорожные сети и судостроение, а также в научных лабораториях.
Хорхе Уэте, председатель проектного консорциума, сказал, что они достигли «фантастических результатов и прототипов», которые принесут реальную пользу людям, работающим с пламенем.
Хотя так называемые электролизеры воды, которые расщепляют воду на газы, которые затем можно сжигать, существуют уже много лет, проблема заключалась в том, что они удерживали потоки газообразных водорода и кислорода вместе — небезопасная и потенциально взрывоопасная смесь из-за проблемы flashback’, когда пламя разгорается слишком быстро и всасывается обратно в систему подачи газа.
«Это новое более безопасное пламя из воды, которое полностью отличается от любого из существующих методов создания пламени для коммерческого использования», — сказал Дэвис.
Расщепление воды светом
В то время как SafeFlame использует электролиз для расщепления воды для создания пламени, другие проекты стремятся имитировать процесс фотосинтеза и использовать свет для расщепления воды, чтобы улавливать молекулы водорода для возобновляемых источников энергии.
«Искусственный фотосинтез предлагает стратегию замены ископаемого топлива чистыми источниками энергии», — сказал доктор Стефано Фабрис, исследователь проекта h3OSPLIT, финансируемого ЕС, в Институте материалов Итальянского национального исследовательского совета.
Конечной целью искусственного фотосинтеза является эффективное преобразование солнечной энергии в химическую энергию и сохранение ее в качестве топлива. Расщепляя воду, молекулы водорода могут быть выделены, а затем преобразованы в электричество для питания всего, от вашего холодильника до города.
Исследователи h3OSPLIT использовали синтезированную группу неорганических молекул оксидов металлов, известных как фотокатализаторы, для запуска химической реакции расщепления воды на водород и кислород под воздействием света.
Чтобы понять, как оптимизировать процесс, исследователи h3OSPLIT использовали комплексное компьютерное моделирование для имитации поведения атомов и электронов во время процесса. Проект завершился в 2013 году, и его предварительные результаты были опубликованы в Proceedings of the National Academy of Sciences .
Проект завершился в 2013 году, и его предварительные результаты были опубликованы в Proceedings of the National Academy of Sciences .
‘Эффективность фотосинтеза растений очень низкая – подумайте о времени, необходимом для выращивания дерева. Чтобы иметь смысл для нашего энергоемкого общества, эффективность искусственных фотосинтетических устройств должна быть намного выше. На данный момент мы все еще далеки от этой цели, но исследования продвигаются быстро», — сказал д-р Фабрис.
Профессор Мэтью Россеински, координатор проекта PhotoCatMOF, финансируемого ЕС, согласен с тем, что пройдет некоторое время, прежде чем эта технология сможет применяться в нашей повседневной жизни. «Только если эффективность станет достаточно высокой, а стоимость снизится до достаточно низкой, технология может быть применена на практике», — сказал он.
Проект PhotoCatMOF исследует, как металлоорганические каркасные материалы могут помочь в получении водорода из воды. Эти материалы улавливают свет, а также являются пористыми, что способствует химической реакции расщепления воды на водород и кислород. Профессор Россеинский сказал, что следующей неотложной задачей является улучшение характеристик их материалов для получения более высокой скорости генерации водорода.
Профессор Россеинский сказал, что следующей неотложной задачей является улучшение характеристик их материалов для получения более высокой скорости генерации водорода.
Хотя были созданы сотни фотокаталитических материалов, они все еще находятся на стадии лабораторных испытаний. Необходимы дальнейшие исследования в рамках проекта PhotoCatMOF и других, чтобы улучшить эти технологии, если они хотят удовлетворить будущие потребности мира в энергии.
Лучший способ получения водорода из воды
Перейти к содержимому
Изменение климата
Исследователи Калифорнийского технологического института демонстрируют чистую технику использования тепла и катализаторов для расщепления воды на водород и кислород.
By
- Kevin Bullisarchive page
19 июня 2012 г.
Экспериментальный подход к расщеплению воды может привести к относительно дешевому и чистому методу крупномасштабного производства водорода, не требующего ископаемого топлива. В процессе вода расщепляется на водород и кислород с использованием тепла и катализаторов, изготовленных из недорогих материалов.
В процессе вода расщепляется на водород и кислород с использованием тепла и катализаторов, изготовленных из недорогих материалов.
Mark E. Davis
Расщепление воды с помощью тепла является альтернативой электролизу, который является дорогостоящим и требует большого количества электроэнергии. Новый подход, разработанный профессором химического машиностроения Калифорнийского технологического института Марком Дэвисом, позволяет избежать ключевых проблем с предыдущими методами расщепления воды, основанными на тепле. Он работает при относительно низких температурах и не производит никаких токсичных или коррозионных промежуточных продуктов.
Почти весь водород, используемый в настоящее время в промышленных процессах, таких как производство бензина, получается в результате риформинга природного газа. Если автопроизводители начнут продавать большое количество автомобилей на водородных топливных элементах, как они заявили, что в конечном итоге планируют это сделать, водород для них также, вероятно, будет поступать из природного газа, если только процессы, подобные тому, что в Калифорнийском технологическом институте, не будут коммерциализированы.
Основной подход к высокотемпературному расщеплению воды заключается в нагревании окисленного металла для удаления кислорода с последующим добавлением воды. В случае Дэвиса исходным материалом является оксид марганца, и реакциям способствует перемещение ионов натрия внутрь и наружу. «Без натрия температура превышала бы 1000 °C, — говорит Дэвис. С ним реакции идут при температурах 850 °С и ниже.
Вероятно, технология далека от коммерческого использования. Для него по-прежнему требуются довольно высокие температуры — например, на пару сотен градусов выше, чем те, которые используются для привода паровых турбин на угольных и атомных электростанциях. Для получения таких температур без ископаемого топлива, вероятно, потребуется одна из двух технологий, ни одна из которых в настоящее время не используется в коммерческих целях: высокотемпературные ядерные реакторы или солнечные тепловые установки с высокой концентрацией, которые используют кольца зеркал для более интенсивной концентрации солнечного света, чем это происходит сегодня в солнечные тепловые электростанции.
Подход Калифорнийского технологического института также необходимо протестировать, чтобы убедиться, что цикл разделения воды может выполняться многократно. На данный момент исследователи показали, что одни и те же материалы можно использовать повторно пять раз, но «если вы хотите, чтобы одна из этих вещей работала по-настоящему, вам пришлось бы запускать ее в течение тысяч циклов», — говорит Дэвис. Он говорит, что такое тестирование выходит за рамки его лаборатории. «Мы довольны потенциалом для многих циклов на этом, но пока вы не сделаете это, вы не узнаете», — говорит он. «Все, что мы здесь сделали, это доказали, что химия может работать».
Также необходимо увеличить скорость производства водорода, например, за счет перехода на материалы с большей площадью поверхности. И Дэвис надеется еще больше снизить необходимые температуры. Цель состоит в том, чтобы использовать этот процесс или аналогичный для использования отработанного тепла на сталелитейных заводах и электростанциях.