Содержание
Расщепление воды – Наука – Коммерсантъ
3K
1 мин.
…
Опыт Карлайла и Николсона был простым, как все гениальное. Чуть раньше в том же 1800 году итальянец Вольта сделал первую в истории человечества химическую батарейку — вольтов столб из сложенных поочередно в столбик кружочков меди и цинка с прокладками между ними из сукна, смоченного в соленой воде. Карлайл и Николсон проводки от вольтова столба опустили в воду. На них образовались пузырьки газа, на одном проводке — водорода, а другом — кислорода.
На них образовались пузырьки газа, на одном проводке — водорода, а другом — кислорода.
Предыдущая фотография
Фото:
Henry Bone
Фото:
T. Blood
Следующая фотография
1
/
2
Фото:
Henry Bone
Фото:
T. Blood
Blood
Оценить всю глубину своего открытия Карлайл и Николсон не смогли и, соответственно, не сумели извлечь из него все крывшиеся в нем научные дивиденды. Не потому что были химиками-самоучками (Карлайл был хирургом, а Николсон и вовсе самоучкой в буквальном смысле этого слова), а потому что вряд ли кто-нибудь другой, будь он семи пядей во лбу, смог бы это сделать, уж слишком широкое поле для научных и практических приложений открыл их опыт.
Поначалу все были загипнотизированы самим фактом того, что электричество способно менять природу материи, на детали опыта всеобщий восторг не распространялся. Эти детали исследовали уже другие ученые, и в отличие от Карлайла и Николсона они остались в истории науки авторами фундаментальных открытий.
Первым был химик Хэмфри Дэви, который, неоднократно повторяя опыт и каждый раз получая из воды только водород и кислород, стал первооткрывателем химического состава воды. Он же, пропуская ток через растворы разных солей, получил на электродах химические элементы калий, натрий, магний, стронций, барий, кальций, бор и хлор. Открыл их!
Он же, пропуская ток через растворы разных солей, получил на электродах химические элементы калий, натрий, магний, стронций, барий, кальций, бор и хлор. Открыл их!
Повторяя опыт Карлайла и Николсона, Гей-Люссак открыл закон объемных отношений газов, а Авогадро — свой «закон Авогадро». В конце концов, Берцелиус окончательно определил формулу воды Н2О. А Майкл Фарадей сформулировал законы электролиза — того явления, которое открыли Карлайл и Николсон в своем опыте и без которого немыслима современная промышленность.
О них же самих сегодня никто не помнит, хотя последние лет тридцать их опыт во всевозможных вариантах со всевозможными катализаторами с упорством маньяков воспроизводят тысячи химиков по всему миру, пытаясь экономически рентабельно разложить воду на водород и кислород, чтобы создать водородный двигатель для автомобиля. А когда эта задача будет решена, о Карлайле и Николсоне опять «первооткрыватели» топлива из воды вряд ли вспомнят.
Сергей Петухов
Картина дня
Вся лента
Водород из воды: просто и дешево
Тема дня
- org/BreadcrumbList»>
Главная
Наука
08 июля, 2005, 00:00
Распечатать
Выпуск № 26, 8 июля-15 июля 2005г.
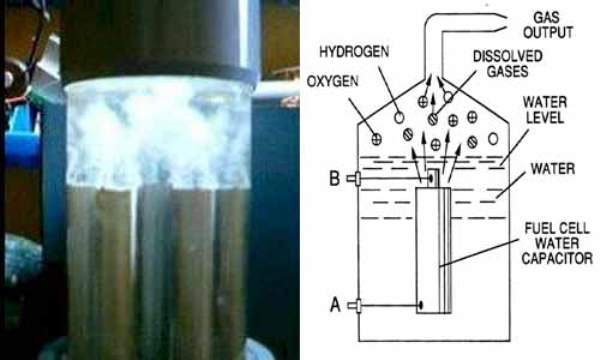
Российский исследователь сконструировал электролизер, позволяющий получать водород из воды, затрачивая на это очень мало энергии…
ЗЕРКАЛО НЕДЕЛИ, УКРАИНА
Архив номеров
|
Последние статьи<
>Временно перемещенные в Украине или за границей, но ведь не забытые
Где за границей уже можно заменить просроченный украинский паспорт или получить международное водительское удостоверение…
Опрос читателейАвторТатьяна Кириленко
Статья
26 октября 17:00
Открытая наука — второй шанс для украинской научной системы?
Правительство приняло план для Украины
Опрос читателейАвторАлександр Березко
Статья
26 октября 13:00
Почему «судьям-пятилеткам» нельзя возвращать полномочия автоматически
Топ-5 причин для блокирования законопроекта № 7698
АвторыМихаил Жернаков, Мария Глушко
Статья
26 октября 08:30
Почему у Путина с Эрдоганом ничего не получится: призрак газового хаба
России не следует рассчитывать на возвращение на газовый рынок Европы через «черный ход»
Опрос читателейАвторАлександр Харченко
Статья
25 октября 17:00
И снова не Джонсон: что обещает Украине премьерство Риши Сунака?
О новом главе правительства Великобритании и стоящих перед ним вызовах
Опрос читателейАвторВиктор Константинов
Статья
25 октября 13:36
Мопедофобия.
 Как найти опору, когда мир катится к чертям
Как найти опору, когда мир катится к чертямСоветы психолога
АвторОлег Покальчук
Статья
25 октября 08:31
- Вам также будет интересно
>
Открытая наука — второй шанс для украинской научной системы?
Опрос читателей
26.10 13:00Не просто победа Украины: зачем нужна научно-техническая деградация России
Опрос читателей
23. 10 08:30
10 08:30Аномальные температуры: будет ли зима холодной
Инфографика
Опрос читателей
15.10 08:30Куда приглашают украинских ученых во время войны
Опрос читателей
30.08 13:05Харьковских школьников встретили невероятными аплодисментами на международном турнире. Почему и как это было?
08.
 08 13:00
08 13:00Наука может стать локомотивом, который вытащит Украину из экономической пропасти
Инфографика
Опрос читателей
06.08 13:40Как оценивать украинскую науку: четыре важные вещи
Опрос читателей
02.08 13:00В чем нуждаются украинские научные работники во время войны и что они могут дать стране?
Опрос читателей
31. 07 13:00
07 13:00Война с Россией: почему Украине нужна математика
Опрос читателей
26.06 17:00Плагиат Шкарлета: почему это важно даже во время войны
► Видео
Опрос читателей
21.05 14:00Как война повлияет на украинскую науку: три риска
Опрос читателей
06. 05 17:00
05 17:00Спецоперация России в науке. Начали и сдулись
Инфографика
05.04 15:00
Последние новости
Оккупанты всю ночь обстреливали Никопольский район. Били по трем громадам из «Градов» и тяжелой артиллерии
08:32
Коррупция на границе во время войны: как излечить неприличную болезнь сильного государства
08:30
ВСУ отразили атаки в районе 13 населенных пунктов – Генштаб
08:01
Военное положение: что делать, если повестку вручили снятому с учета
08:00
Оккупанты под видом «эвакуации» просто грабят Херсонщину – Генштаб
07:28
Все новости
Добро пожаловать!
Регистрация
Восстановление пароля
Авторизуйтесь, чтобы иметь возможность комментировать материалы
Зарегистрируйтесь, чтобы иметь возможность комментировать материалы
Введите адрес электронной почты, на который была произведена регистрация и на него будет выслан пароль
Забыли пароль?
Войти
Пароль может содержать большие и маленькие буквы латинского алфавита, а также цифры
Введенный e-mail содержит ошибки
Зарегистрироваться
Имя и фамилия должны состоять из букв латинского алфавита или кирилицы
Введенный e-mail содержит ошибки
Данный e-mail уже существует
У поля Имя и фамилия нет ошибок
У поля E-mail нет ошибок
Напомнить пароль
Введенный e-mail содержит ошибки
Нет учетной записи? Зарегистрируйтесь!
Уже зарегистрированы? Войдите!
Нет учетной записи? Зарегистрируйтесь!
Метод получения кислорода из воды в условиях невесомости дает надежду на дальние космические путешествия Предоставлено: NASA
Следующее эссе перепечатано с разрешения The Conversation, интернет-издания, посвященного последним исследованиям.
Космические агентства и частные компании уже разработали планы по отправке людей на Марс в ближайшие несколько лет и, в конечном счете, его колонизации. А с растущим числом открытий похожих на Землю планет вокруг ближайших звезд дальние космические путешествия никогда не казались более захватывающими.
Однако людям нелегко выживать в космосе в течение продолжительных периодов времени. Одной из главных проблем дальних космических полетов является транспортировка достаточного количества кислорода для дыхания астронавтов и достаточного количества топлива для питания сложной электроники. К сожалению, в космосе мало кислорода, а большие расстояния затрудняют быстрое восполнение запасов.
Но теперь новое исследование, опубликованное в Nature Communications, показывает, что можно производить водород (для топлива) и кислород (для жизни) только из воды, используя полупроводниковый материал и солнечный свет (или звездный свет) в условиях невесомости, что делает устойчивые космические путешествия — реальная возможность.
Использование неограниченных ресурсов солнца для обеспечения энергией нашей повседневной жизни — одна из самых больших проблем на Земле. Поскольку мы медленно уходим от нефти к возобновляемым источникам энергии, исследователей интересует возможность использования водорода в качестве топлива. Лучший способ сделать это — разделить воду (h3O) на составляющие: водород и кислород. Это возможно с помощью процесса, известного как электролиз, который включает пропускание тока через образец воды, содержащий некоторое количество растворимого электролита. Это расщепляет воду на кислород и водород, которые выделяются отдельно на двух электродах.
Хотя этот метод технически возможен, он еще не стал доступным на Земле, поскольку нам нужна дополнительная инфраструктура, связанная с водородом, такая как станции заправки водородом, чтобы масштабировать его.
Солнечная энергия
Водород и кислород, полученные таким образом из воды , также могут использоваться в качестве топлива на космических кораблях. Запуск ракеты с водой на самом деле был бы намного безопаснее, чем запуск с дополнительным ракетным топливом и кислородом на борту, которые могут быть взрывоопасными. Оказавшись в космосе, специальная технология сможет расщепить воду на водород и кислород, которые, в свою очередь, можно будет использовать для поддержания жизни или для питания электроники с помощью топливных элементов.
Запуск ракеты с водой на самом деле был бы намного безопаснее, чем запуск с дополнительным ракетным топливом и кислородом на борту, которые могут быть взрывоопасными. Оказавшись в космосе, специальная технология сможет расщепить воду на водород и кислород, которые, в свою очередь, можно будет использовать для поддержания жизни или для питания электроники с помощью топливных элементов.
Это можно сделать двумя способами. Один из них включает электролиз, как мы делаем на Земле, с использованием электролитов и солнечных элементов , чтобы улавливать солнечный свет и преобразовывать его в ток.
Альтернативой является использование «фотокатализаторов», которые работают, поглощая частицы света — фотоны — полупроводниковым материалом, помещенным в воду. Энергия фотона поглощается электроном в материале, который затем прыгает, оставляя после себя дыру. Свободный электрон может реагировать с протонами (которые вместе с нейтронами составляют атомное ядро) в воде с образованием водорода.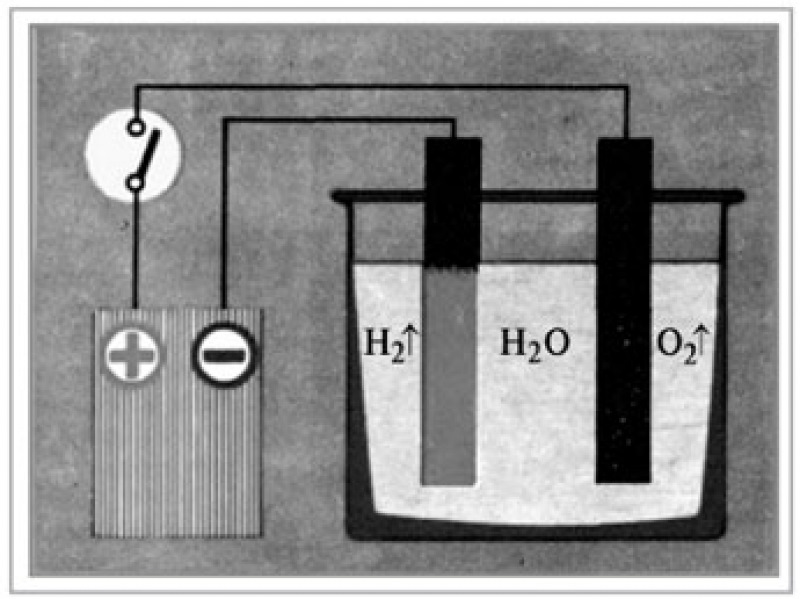 Между тем, дырка может поглощать электроны из воды с образованием протонов и кислорода.
Между тем, дырка может поглощать электроны из воды с образованием протонов и кислорода.
Процесс также может быть обратным. Водород и кислород можно объединить или «рекомбинировать» с помощью топливного элемента, возвращая солнечную энергию, полученную в результате «фотокатализа» — энергию, которую можно использовать для питания электроники. В результате рекомбинации в качестве продукта образуется только вода, а это означает, что вода также может быть использована повторно. Это ключ к дальним космическим путешествиям.
Процесс с использованием фотокатализаторов является оптимальным вариантом для космических полетов, так как оборудование весит намного меньше, чем необходимое для электролиза. По идее должно работать легко. Отчасти это связано с тем, что интенсивность солнечного света намного выше, а атмосфера Земли не поглощает его в больших количествах на пути к поверхности.
Управление пузырьками
В новом исследовании исследователи сбросили полную экспериментальную установку для фотокатализа в 120-метровую башню, создав среду, подобную микрогравитации. По мере того, как объекты ускоряются к Земле в свободном падении, эффект гравитации уменьшается, поскольку силы, действующие под действием гравитации, уравновешиваются равными и противоположными силами из-за ускорения. Это противоположно перегрузкам, которые испытывают космонавты и летчики-истребители, когда они разгоняются в своих самолетах.
По мере того, как объекты ускоряются к Земле в свободном падении, эффект гравитации уменьшается, поскольку силы, действующие под действием гравитации, уравновешиваются равными и противоположными силами из-за ускорения. Это противоположно перегрузкам, которые испытывают космонавты и летчики-истребители, когда они разгоняются в своих самолетах.
Исследователям удалось показать, что в этой среде действительно возможно разделить воду. Однако, когда вода расщепляется с образованием газа, образуются пузырьки. Избавление от пузырьков из когда-то образовавшегося материала катализатора важно, так как пузырьки мешают процессу образования газа. На Земле гравитация заставляет пузырьки автоматически всплывать на поверхность (вода у поверхности плотнее пузырьков, что делает их гибкими), освобождая место на катализаторе для образования следующего пузыря.
В условиях невесомости это невозможно, и пузырек останется на катализаторе или рядом с ним. Однако ученые скорректировали форму наночастиц в катализаторе, создав пирамидальные зоны, в которых пузырек мог легко отделиться от кончика и уплыть в среду.
Но остается одна проблема. В отсутствие гравитации пузырьки останутся в жидкости, даже если они были вытеснены из самого катализатора. Гравитация позволяет газам легко выходить из жидкости, что очень важно для использования чистого водорода и кислорода. Без гравитации никакие пузырьки газа не всплывают на поверхность и не отделяются от смеси — вместо этого весь газ остается для создания пены.
Это резко снижает эффективность процесса из-за блокировки катализаторов или электродов. Инженерные решения этой проблемы будут иметь ключевое значение для успешного внедрения технологий в космосе. Одна из возможностей — использование центробежных сил от вращения космического корабля для отделения газов от раствора.
Тем не менее, благодаря этому новому исследованию мы стали на шаг ближе к длительному космическому полету человека.
Первоначально эта статья была опубликована на The Conversation. Прочитайте оригинальную статью.
ОБ АВТОРАХ
Share on Facebook
Share on Twitter
Share on Reddit
Share on LinkedIn
Share via Email
Print
- Водонепроницаемая рабочая зона
- Помощник для взрослых
- Графит для механического карандаша (достаточно толстый, чтобы не сломаться) или деревянный карандаш и нож, чтобы ваш взрослый помощник извлек графит
- Клей
- Play-Doh или другая глина
- Два или три одноразовых пластиковых стаканчика (лучше всего подходят прозрачные пластиковые стаканчики на 18 унций).

- Ножницы
- Перманентный маркер
- Две металлические кнопки
- Дистиллированная вода
- Пищевая сода
- Аккумулятор на девять вольт
- Две прозрачные соломинки (большой размер)
- Чайная ложка
- Медицинская капельница
- Таймер
- Бумажные полотенца
- Тест-полоски для определения pH (дополнительно)
- Поваренная соль (хлорид натрия — NaCl) (по желанию)
- Ваша рабочая зона должна быть водонепроницаемой; разливы воды могут произойти во время деятельности.
- Соберите свой прочный графитовый механический карандаш. Убедитесь, что у вас есть два куска длиной около 2,5 см (один дюйм). Если вы решите использовать деревянный карандаш, попросите взрослого взять нож и извлечь из карандаша графитовый грифель. (Для этого у вас также должно получиться два куска длиной примерно 2,5 сантиметра). Это будут ваши графитовые электроды.

- Аккуратно отрежьте ножницами (или попросите взрослого обрезать) открытый конец одного пластикового стаканчика так, чтобы он был на высоте девятивольтовой батареи. В нижней части чашки прорежьте отверстие, чтобы кончик батареи (с двумя полюсами) мог пройти через него.
- Возьмите другую чашку и держите дно этой чашки поверх девятивольтовой батареи. Несмываемым маркером на внутренней стороне чашки нарисуйте две точки внизу, где чашка соприкасается с двумя полюсами батареи.
- Снимите чашку с батареи и с помощью чертежной кнопки проделайте по одному отверстию в каждой отмеченной точке на дне пластиковой чаши.
- Аккуратно вставьте два графитовых (карандашных) штифта в два отверстия, по одному в каждое. Возможно, вам придется сделать отверстия немного больше, чтобы они подходили.
- Используйте клей, чтобы запечатать вокруг графитовых штифтов на внешней стороне чашки, и дайте ему высохнуть. Это должно предотвратить просачивание воды. Убедитесь, что графитовые контакты не все покрыты клеем, иначе они больше не будут контактировать с батареей.

- Поместите разрезанную чашку открытой стороной вниз на батарею. Дно чашки и аккумулятор должны совпадать, образуя ровную поверхность, на которую можно поставить другую чашку.
- Поместите чашку с графитовыми штифтами на перевернутую обрезанную чашку сверху аккумулятора. Он должен сидеть там прочно, и каждый из графитовых штифтов должен касаться одного из полюсов батареи.
- Заклейте один конец обеих соломинок для питья пластилином или пластилином.
- Возьмите чашку с графитовыми штифтами и налейте в чашку около 300 миллилитров дистиллированной воды подальше от батареи. Убедитесь, что он не протекает. Если это так, вам может понадобиться добавить немного клея, чтобы сделать плотное соединение. Примечание. Не прикасайтесь к воде или электродам после того, как чаша будет помещена на батарею, так как вы можете почувствовать покалывание электричества в пальцах.
- Как и раньше, поместите его на перевернутую обрезанную чашку сверху батареи так, чтобы каждый из графитовых штифтов касался одного из полюсов батареи.
 Возможно, вам придется немного прижать его, чтобы установить хорошее соединение. Обратите внимание на два графитовых электрода. Что ты видишь? Что-то происходит на электродах?
Возможно, вам придется немного прижать его, чтобы установить хорошее соединение. Обратите внимание на два графитовых электрода. Что ты видишь? Что-то происходит на электродах? - Снимите чашу с дистиллированной водой с аккумулятора. Насыпьте одну чайную ложку пищевой соды и размешайте ее в дистиллированной воде, пока все не растворится. Как вы думаете, что изменит пищевая сода? Какую функцию он выполняет?
- Теперь снова поставьте чашку на батарею и соедините графитовые электроды с полюсами батареи. Что вы сейчас наблюдаете? На графитовых штифтах ничего не происходит? Как вы думаете, что является продуктом реакции? Сравните реакции, происходящие на каждом из графитовых электродов. Вы видите разницу между обеими сторонами? Есть ли один графитовый электрод, на котором реакция выражена сильнее? К какому полюсу батареи подключен этот графитовый штифт, к положительному или отрицательному?
- Засуньте нос в чашку и понюхайте продукты реакции.
 Есть запах? Если да, то как он пахнет?
Есть запах? Если да, то как он пахнет? - Снова снимите чашку с батареи. С помощью пипетки наполните обе закупоренные большие соломинки раствором пищевой соды из чашки с графитовыми штифтами. Когда они наполнятся, закройте каждую одним пальцем и переверните вверх дном. Опустите их в чашку с раствором пищевой соды и осторожно поместите их поверх графитовых штифтов (по одной соломинке на каждую), чтобы соломинки оставались полностью заполненными раствором пищевой соды. Если соломинки не стоят вертикально, вы можете прислонить их к краю чашки. Как вы думаете, что будет с соломинкой?
- После того, как соломинки будут размещены поверх графитовых штифтов, поставьте чашку обратно на батарею. Оставьте его там на 10 минут и немного нажмите на чашку, чтобы убедиться, что электроды остаются подключенными и электродные реакции происходят непрерывно в течение всего этого времени. Обратите внимание на огромные соломинки, которые вы надеваете на графитовые булавки.
 Что происходит с водой, которую вы туда налили? Вы замечаете разницу между двумя уровнями воды в обеих соломинках? Какой из них выше, какой ниже; к каким полюсам батареи подключен каждый из них?
Что происходит с водой, которую вы туда налили? Вы замечаете разницу между двумя уровнями воды в обеих соломинках? Какой из них выше, какой ниже; к каким полюсам батареи подключен каждый из них? - По истечении 10 минут отметьте уровень воды в каждой соломинке несмываемым маркером. Насколько больше воды было вытеснено продуктами реакции на отрицательном полюсе по сравнению с положительным полюсом? Одинаковые, двойные или тройные?
- Дополнительно: Если у вас есть тест-полоски для измерения pH, которые могут измерять кислотность или щелочность растворов, используйте их для измерения pH в каждой большой соломинке после того, как уровень воды упадет примерно на 50 процентов. Осторожно снимите большие соломинки с электродов и сразу же запечатайте каждую из них пальцем, как только вы оторвете ее от электродов. Убедитесь, что вы не потеряли воду, которая находится внутри, окуните тест-полоску pH внутрь. Какой цвет показывает тест-полоска и какое значение рН она представляет? Есть ли разница между растворами в двух соломинках? Чем они отличаются и почему, на ваш взгляд, это так?
- Дополнительно: Повторите эксперимент, но вместо пищевой соды в дистиллированную воду добавьте чайную ложку поваренной соли (хлорида натрия или NaCl) и дайте электролизу поработать в течение пяти минут.
 Изменяются ли электродные реакции? Что можно сказать о запахе продуктов реакции; Вы можете разобрать определенный запах на этот раз? Как вы думаете, почему это так?
Изменяются ли электродные реакции? Что можно сказать о запахе продуктов реакции; Вы можете разобрать определенный запах на этот раз? Как вы думаете, почему это так? - Дополнительно: Замените графитовые электроды металлическими кнопками. Для этого вам может понадобиться свежая чашка. Вставьте кнопки в дно чашки так, чтобы они не касались друг друга, но так, чтобы каждая из них касалась одного из полюсов батареи, как только вы поместите чашку на батарею. При использовании кнопок клеевое уплотнение не требуется. Повторите исходную процедуру, но на этот раз добавьте в дистиллированную воду одну чайную ложку поваренной соли. Наблюдайте за электродными реакциями. Что будет на этот раз? Посмотрите внимательно на контакт, который подключен к положительному полюсу аккумулятора. Вы видите другие продукты реакции, кроме газа? Как вы думаете, что произошло? Как выглядят металлические кнопки после того, как вы их снова вытащите?
Старший преподаватель энергетики Университета Суонси.
Splitting Water — Scientific American
Знаете ли вы, что воду можно разделить на два составных элемента, используя всего несколько предметов домашнего обихода? Посмотрите, из чего на самом деле состоит ваша вода, в этом занятии по разрушению молекул. Все, что нужно, это немного сока! Кредит: Джордж Рецек
Ключевые понятия
Вода
Химия
Электричество
Молекулы
Введение
Пользуешься им каждый день и без него не выживешь — нет, это не интернет, а вода! Это одно из самых важных соединений в мире, и проблема становится все более важной во всем мире. Вы, наверное, слышали, что во многих местах засуха или загрязнение воды ограничивают запасы чистой питьевой воды, и эти запасы продолжают сокращаться. Размышляя об этом, задумывались ли вы когда-нибудь, почему мы не делаем воду сами? Из чего на самом деле состоит вода? В этой научной деятельности вы будете использовать энергию в виде электричества для расщепления воды на отдельные компоненты; так что соберите все материалы и приготовьтесь узнать, что это такое, — и разделите их сами!
Размышляя об этом, задумывались ли вы когда-нибудь, почему мы не делаем воду сами? Из чего на самом деле состоит вода? В этой научной деятельности вы будете использовать энергию в виде электричества для расщепления воды на отдельные компоненты; так что соберите все материалы и приготовьтесь узнать, что это такое, — и разделите их сами!
Фон
Чтобы узнать, из чего состоит вода, полезно посмотреть на ее химическую формулу: h3O. Это в основном говорит нам о том, что молекула воды состоит из двух элементов: водорода и кислорода или, точнее, двух атомов водорода (h3) и одного атома кислорода (O). Водород и кислород являются газами при комнатной температуре. Значит ли это, что мы можем просто соединить оба газа и получить воду? Это не так просто. В уравнении отсутствует энергетическая составляющая химической реакции. Изготовление воды из ее элементов производит большое количество энергии. Химические реакции, в результате которых выделяется энергия, также называют экзотермическими реакциями. В случае водорода и кислорода выделяемая энергия настолько велика, что ее практически невозможно контролировать, и в большинстве случаев она приводит к взрыву. К счастью, эта реакция не происходит самопроизвольно, а происходит только при поджигании газовой смеси зажигалкой.
В случае водорода и кислорода выделяемая энергия настолько велика, что ее практически невозможно контролировать, и в большинстве случаев она приводит к взрыву. К счастью, эта реакция не происходит самопроизвольно, а происходит только при поджигании газовой смеси зажигалкой.
Если делать воду из ее элементов так опасно, то как насчет обратной реакции? Разделить воду на два компонента гораздо проще, и это называется электролизом воды. Получение водорода или кислорода таким способом кажется простым. Но, как вы, вероятно, подозревали, эта обратная реакция требует затрат энергии, поэтому ее также называют эндотермической реакцией. При электролизе воды источником энергии, используемой для протекания реакции, является электричество. Самый простой способ получения электричества — аккумулятор. Однако, поскольку чистая вода плохо проводит электричество, для электролиза требуется добавление электролита 9.0003, , такие как соль или кислота. Электролит растворяется в воде и разделяется на ионы (электрически заряженные частицы), которые перемещаются в растворах и таким образом способны проводить электричество. Чтобы добавить электричества в раствор, вам также понадобятся два электрических проводника, которые соприкасаются с водой. Они называются электродами и в основном представляют собой металлы или другие проводящие материалы. Когда на электроды подается электрический ток, ионы (электрически заряженные атомы) в электролите, включая положительно заряженные протоны (H + ) и отрицательно заряженные гидроксильные ионы (ОН — ), образующиеся в результате самоионизации воды, начинают двигаться к электроду с противоположным зарядом, где образуется либо водород, либо кислород. Вы можете убедиться в этом сами в этом упражнении и даже зафиксировать оба газа!
Чтобы добавить электричества в раствор, вам также понадобятся два электрических проводника, которые соприкасаются с водой. Они называются электродами и в основном представляют собой металлы или другие проводящие материалы. Когда на электроды подается электрический ток, ионы (электрически заряженные атомы) в электролите, включая положительно заряженные протоны (H + ) и отрицательно заряженные гидроксильные ионы (ОН — ), образующиеся в результате самоионизации воды, начинают двигаться к электроду с противоположным зарядом, где образуется либо водород, либо кислород. Вы можете убедиться в этом сами в этом упражнении и даже зафиксировать оба газа!
Материалы
Подготовка
Процедура
Наблюдения и результаты
Удалось ли вам разделить воду на водород и кислород? Вы видели много пузырьков на обоих графитовых штифтах? Первоначально, когда вы ставили чашку с дистиллированной водой на аккумулятор, вы, вероятно, не видели, что происходит на графитовых электродах. Это связано с тем, что дистиллированная вода не очень хорошо проводит электричество, поэтому электродные реакции отсутствуют или возможны лишь незначительные реакции. Однако, если вы добавите электролиты, такие как пищевая сода, добавленные ионы могут проводить электричество, и вы должны были увидеть пузырьки газа, появляющиеся на обоих графитовых штифтах. С одной стороны, на положительном полюсе образуется кислород, тогда как на отрицательном полюсе образуется водород.
Это связано с тем, что дистиллированная вода не очень хорошо проводит электричество, поэтому электродные реакции отсутствуют или возможны лишь незначительные реакции. Однако, если вы добавите электролиты, такие как пищевая сода, добавленные ионы могут проводить электричество, и вы должны были увидеть пузырьки газа, появляющиеся на обоих графитовых штифтах. С одной стороны, на положительном полюсе образуется кислород, тогда как на отрицательном полюсе образуется водород.
Присмотревшись, вы могли заметить, что на графитовом электроде, соединенном с отрицательным полюсом батареи, образовалось больше газа, чем на другой стороне. Сбор двух газов с помощью гигантских соломинок, вероятно, продемонстрировал это еще лучше. Через 10 минут уровень воды на отрицательном полюсе должен был быть примерно вдвое меньше, чем на положительном полюсе, а это означает, что вы собрали примерно вдвое больше газообразного водорода по сравнению с кислородом. Разница связана с тем, что на одну молекулу воды приходится два атома водорода на один атом кислорода, как объяснялось выше. Это означает, что для образования одной молекулы кислорода (O2) требуется две молекулы воды (2 ч3О). Однако в то же время из двух молекул воды (2 ч3О) можно получить две молекулы водорода (2 ч3). В то время как на электродах образуются водород и кислород, остаточными продуктами реакции из воды являются протоны (H + на стороне кислорода) и ионов гидроксила (ОН — на стороне водорода). Вы можете визуализировать это, поместив полоску pH в растворы в больших соломинках над каждым электродом. Раствор в соломинке, помещенной поверх электрода отрицательного полюса батареи, должен иметь щелочной pH (7 или выше), тогда как другой раствор должен быть кислым (pH менее 7).
Это означает, что для образования одной молекулы кислорода (O2) требуется две молекулы воды (2 ч3О). Однако в то же время из двух молекул воды (2 ч3О) можно получить две молекулы водорода (2 ч3). В то время как на электродах образуются водород и кислород, остаточными продуктами реакции из воды являются протоны (H + на стороне кислорода) и ионов гидроксила (ОН — на стороне водорода). Вы можете визуализировать это, поместив полоску pH в растворы в больших соломинках над каждым электродом. Раствор в соломинке, помещенной поверх электрода отрицательного полюса батареи, должен иметь щелочной pH (7 или выше), тогда как другой раствор должен быть кислым (pH менее 7).
Могут происходить и другие электродные реакции, если в растворе есть ионы, конкурирующие с образованием водорода или кислорода. Возможно, вы заметили, что после того, как вы добавили соль (хлорид натрия) в электролит, он начал пахнуть, как в бассейне. Вместо кислорода на положительном полюсе батареи вырабатывается хлор, который также используется для дезинфекции воды в бассейне.

 Как найти опору, когда мир катится к чертям
Как найти опору, когда мир катится к чертям 10 08:30
10 08:30 08 13:00
08 13:00 07 13:00
07 13:00 05 17:00
05 17:00

 Возможно, вам придется немного прижать его, чтобы установить хорошее соединение. Обратите внимание на два графитовых электрода. Что ты видишь? Что-то происходит на электродах?
Возможно, вам придется немного прижать его, чтобы установить хорошее соединение. Обратите внимание на два графитовых электрода. Что ты видишь? Что-то происходит на электродах?  Есть запах? Если да, то как он пахнет?
Есть запах? Если да, то как он пахнет?  Что происходит с водой, которую вы туда налили? Вы замечаете разницу между двумя уровнями воды в обеих соломинках? Какой из них выше, какой ниже; к каким полюсам батареи подключен каждый из них?
Что происходит с водой, которую вы туда налили? Вы замечаете разницу между двумя уровнями воды в обеих соломинках? Какой из них выше, какой ниже; к каким полюсам батареи подключен каждый из них?  Изменяются ли электродные реакции? Что можно сказать о запахе продуктов реакции; Вы можете разобрать определенный запах на этот раз? Как вы думаете, почему это так?
Изменяются ли электродные реакции? Что можно сказать о запахе продуктов реакции; Вы можете разобрать определенный запах на этот раз? Как вы думаете, почему это так?