Содержание
Из чего состоит все вокруг или что такое молекула?
Каждый раз, когда два атома соединяются вместе, они образуют молекулу. На самом деле все, что нас окружает – да и мы сами – состоит из триллионов различных типов молекул. Понятие молекулы было принято в 1860 году на международном съезде химиков в Карлсруэ. Согласно принятому определению молекула – это наименьшая частица химического вещества, которая обладает всеми его химическими свойствами (растворимость, вкус, способность вступать в соединения и пр). Введение понятия молекулы подтолкнуло развитие физики, химии и других естественных наук. В более общем понимании молекулой называют частицу, образованную из двух или более атомов, соединенных между собой ковалентными связями.
Молекула воды содержит 1 атом кислорода и 2 атома водорода
Атом – мельчайшая частица вещества, которая обладает всеми его физическими свойствами (цвет, твердость, плотность и пр.)
Когда атомы различных типов элементов соединяются вместе, они образуют молекулы, называемые соединениями. Так, вода состоит из сложных молекул, состоящих из 2 атомов водорода и 1 атома кислорода. Вот почему она называется h3O: у молекулы воды всегда будет в 2 раза больше атомов водорода, чем атомов кислорода. Существует чуть более 100 типов атомов, но типов различных веществ миллионы. Причина такого неравенства кроется в том, что они состоят из различных типов молекул.
Так, вода состоит из сложных молекул, состоящих из 2 атомов водорода и 1 атома кислорода. Вот почему она называется h3O: у молекулы воды всегда будет в 2 раза больше атомов водорода, чем атомов кислорода. Существует чуть более 100 типов атомов, но типов различных веществ миллионы. Причина такого неравенства кроется в том, что они состоят из различных типов молекул.
Важно понимать, что молекулы состоят не только из различных типов атомов, но и из различных соотношений. Как и в приведенном выше примере с водой, молекула воды состоит из двух атома водорода и одного атома кислорода, что записывается как h3O. Другими примерами являются углекислый газ (C02), аммиак (Nh4) и сахар или глюкоза (C6h22O6). Некоторые молекулярные формулы могут получиться довольно длинными и сложными. Давайте посмотрим на молекулу сахара:
- С6 — 6 атомов углерода
- h22 — 12 атомов водорода
- Атом кислорода O6 — 6
Чтобы она получилась, нужны определенные атомы в определенном количестве. Но молекулы могут быть гораздо больше. Одна молекула витамина С состоит из 20 атомов (6 атомов углерода, 8 атомов водорода и 6 атомов кислорода – C6H8O6). Если взять эти 20 атомов витамина С и смешать, соединяя их вместе в другом порядке, то получится совершенно другая молекула, которая не только выглядит по-другому, но и действует иначе.
Но молекулы могут быть гораздо больше. Одна молекула витамина С состоит из 20 атомов (6 атомов углерода, 8 атомов водорода и 6 атомов кислорода – C6H8O6). Если взять эти 20 атомов витамина С и смешать, соединяя их вместе в другом порядке, то получится совершенно другая молекула, которая не только выглядит по-другому, но и действует иначе.
Молекула витамина С выглядит так
Читайте также: Обнаружены новые химические соединения, способные объяснить возникновение жизни на Земле.
Некоторые молекулы, особенно некоторые белки, содержат сотни или даже тысячи атомов, которые соединяются вместе в цепи, которые могут достигать значительной длины. Жидкости, содержащие такие молекулы, иногда ведут себя странно. Например, жидкость может продолжать вытекать из колбы, из которой была вылита некоторая ее часть, даже после того, как колба будет возвращена в вертикальное положение.
Факты о молекулах
- Газообразный кислород обычно представляет собой молекулу O2, но это может быть и O3, который мы называем озоном.

- Молекулы могут иметь различную форму. Некоторые из них представляют собой длинные спирали, а другие могут иметь форму пирамиды.
- Идеальный алмаз — это единственная молекула, состоящая из атомов углерода.
- ДНК – это сверхдлинная молекула, которая обладает информацией, описывающей каждого человека.
- 66% массы человеческого тела состоит из атомов кислорода
Чтобы всегда быть в курсе последних научных открытий, подписывайтесь на наш новостной канал в Telegram
Химические связи
Молекулы и соединения удерживаются вместе силами, называемыми химическими связями. Существует четыре типа химических связей, которые удерживают большинство соединений вместе: ковалентные связи, ионные связи, водородные и металлические, однако в качестве основных выделяют ковалентные и ионные, так как они связаны с электронами. Как известно, электроны вращаются вокруг атомов в оболочках. Эти оболочки хотят быть «полными» электронов. Когда они не заполнены, то будут пытаться соединиться с другими атомами, чтобы получить нужное количество электронов и заполнить их оболочки.
Ковалентные связи делят электроны между атомами. Это происходит, когда получается, что атомы делятся своими электронами, чтобы заполнить свои внешние оболочки. В свою очередь ионные связи образуются, когда один электрон передается другому. Это происходит, когда один атом отдает электрон другому, чтобы сформировать баланс и, следовательно, молекулу или соединение.
Еще больше увлекательных статей о том, как ученые дробят реальность на атомы, читайте на нашем канале в Яндекс.Дзен. Там выходят статьи, которых нет на сайте!
Знания о свойствах и строении молекул легли в основу современной науки и нашего понимания Вселенной
Немаловажным также является тот факт, что молекулы всегда находятся в движении. В твердых телах и жидкостях они находятся очень близко друг к другу, а их движение можно сравнить с быстрой вибрацией. В жидкостях молекулы могут свободно перемещаться между собой, как бы скользя. В газе плотность молекул обычно меньше, чем в жидкости или твердом теле того же химического соединения, а потому молекулы движутся даже более свободно, чем в жидкости. Для конкретного соединения в данном состоянии (твердом, жидком или газообразном) скорость молекулярного движения возрастает с увеличением абсолютной температуры.
Для конкретного соединения в данном состоянии (твердом, жидком или газообразном) скорость молекулярного движения возрастает с увеличением абсолютной температуры.
БиологияНаука физика
Для отправки комментария вы должны или
Опровергнута самая популярная теория строения воды
Учёные СФУ совместно с коллегами из Королевского института технологий Швеции опровергли самую популярную ныне кластерную теорию строения воды. В ходе работы исследователи предложили новую теорию, согласующуюся с результатами их эксперимента. Работа опубликована в журнале Nature Communications. Исследования поддержаны грантом Российского научного фонда.
Вода — одно из самых распространённых, но в то же время необычных веществ на Земле. Она обладает рядом нетипичных свойств, объясняемых её особой структурой, например, высокой теплоёмкостью и низкой электропроводностью. Общепринято, что вода состоит из молекул Н2О, объединённых в группы так называемыми водородными связями. Их наличие обусловлено притяжением между положительно заряженными атомами водорода и отрицательно заряженными атомами кислорода. Свободные, не входящие в кластеры (группы молекул, связанных водородными связями) молекулы присутствуют лишь в небольшом количестве. Многие учёные считают, что вода — постоянно изменяющаяся смесь кластеров лёгкого и тяжёлого типов. В первом молекулы связаны друг с другом (как во льду), а во втором связи нарушены, благодаря чему такие системы более плотные. Наличие этих фаз можно обнаружить при помощи резонансного неупругого рассеяния рентгеновских фотонов водой. При этом виден переход, в котором электрон с занятой молекулярной орбитали заполняет дырку, на месте которой был выбитый ранее фотоном электрон. Эксперимент с жидкой водой показывает расщепление резонанса на два пика. В научной литературе получившийся дублет приписывается кластерам лёгкого и тяжёлого типов.
Их наличие обусловлено притяжением между положительно заряженными атомами водорода и отрицательно заряженными атомами кислорода. Свободные, не входящие в кластеры (группы молекул, связанных водородными связями) молекулы присутствуют лишь в небольшом количестве. Многие учёные считают, что вода — постоянно изменяющаяся смесь кластеров лёгкого и тяжёлого типов. В первом молекулы связаны друг с другом (как во льду), а во втором связи нарушены, благодаря чему такие системы более плотные. Наличие этих фаз можно обнаружить при помощи резонансного неупругого рассеяния рентгеновских фотонов водой. При этом виден переход, в котором электрон с занятой молекулярной орбитали заполняет дырку, на месте которой был выбитый ранее фотоном электрон. Эксперимент с жидкой водой показывает расщепление резонанса на два пика. В научной литературе получившийся дублет приписывается кластерам лёгкого и тяжёлого типов.
Чтобы пролить свет на эту фундаментальную проблему, авторы работы провели эксперимент с парами воды, где нет водородных связей. В ходе исследования они измерили спектр резонансного неупругого рассеяния изолированной молекулы. Эксперименты привели к неожиданному результату и показали, что точно такое же расщепление резонанса на два пика присутствует в рентгеновских спектрах рассеяний молекул воды в газовой фазе. Более того, выполненные теоретические расчёты однозначно объясняют расщепление на спектре сверхбыстрым распадом (диссоциацией) молекулы воды на ионы Н+ и ОН-. Таким образом, исследование свидетельствует о динамической природе расщепления резонанса и опровергает структурный механизм, тем самым демонстрируя, что структура воды однородна.
В ходе исследования они измерили спектр резонансного неупругого рассеяния изолированной молекулы. Эксперименты привели к неожиданному результату и показали, что точно такое же расщепление резонанса на два пика присутствует в рентгеновских спектрах рассеяний молекул воды в газовой фазе. Более того, выполненные теоретические расчёты однозначно объясняют расщепление на спектре сверхбыстрым распадом (диссоциацией) молекулы воды на ионы Н+ и ОН-. Таким образом, исследование свидетельствует о динамической природе расщепления резонанса и опровергает структурный механизм, тем самым демонстрируя, что структура воды однородна.
Второй не менее важный результат этой работы — получение детальной структурной информации о том, как влияют водородные связи на силу OH-связи. Колебательная инфракрасная (ИК) спектроскопия — общепринятый инструмент для исследования водородных связей в жидкостях. Но в них ИК-спектроскопия показывает лишь наиболее интенсивный переход в состояние с минимальной энергией колебаний, которое «слабо чувствует» межмолекулярное взаимодействие. Спектроскопия резонансного неупругого рассеяния воды качественно отличается от ИК-спектроскопии тем, что, получив энергию от рентгеновского фотона, электрон кислорода переходит с самой глубокой орбитали на первую незанятую. В результате молекула воды быстро диссоциирует. В процессе возбуждённый электрон переходит обратно на самый глубокий уровень, испуская рентгеновский фотон. Частота колебаний испущенного фотона отличается от возбуждающего фотона, так как при этом переходе электрон попадает на уровни с большей энергией. Таким образом, в отличие от ИК-спектра, спектр резонансного неупругого рассеяния состоит из протяжённого набора колебательных пиков. Чем выше колебательное состояние, тем дальше атомы водорода удаляются от кислорода в процессе колебаний связи между О и Н и тем сильнее это колебание чувствует взаимодействие с ближайшей молекулой воды, а именно водородную связь. Резонансное неупругое рассеяние даёт уникальную возможность исследовать водородные связи, в частности определить на основании спектра, как влияют соседние молекулы через водородную связь на потенциал взаимодействия OH-связи.
Спектроскопия резонансного неупругого рассеяния воды качественно отличается от ИК-спектроскопии тем, что, получив энергию от рентгеновского фотона, электрон кислорода переходит с самой глубокой орбитали на первую незанятую. В результате молекула воды быстро диссоциирует. В процессе возбуждённый электрон переходит обратно на самый глубокий уровень, испуская рентгеновский фотон. Частота колебаний испущенного фотона отличается от возбуждающего фотона, так как при этом переходе электрон попадает на уровни с большей энергией. Таким образом, в отличие от ИК-спектра, спектр резонансного неупругого рассеяния состоит из протяжённого набора колебательных пиков. Чем выше колебательное состояние, тем дальше атомы водорода удаляются от кислорода в процессе колебаний связи между О и Н и тем сильнее это колебание чувствует взаимодействие с ближайшей молекулой воды, а именно водородную связь. Резонансное неупругое рассеяние даёт уникальную возможность исследовать водородные связи, в частности определить на основании спектра, как влияют соседние молекулы через водородную связь на потенциал взаимодействия OH-связи.
«Важно отметить, что, в отличие от изолированной молекулы воды с одной энергией взаимодействия О и Н, в жидкости имеется набор (распределение) таких энергий в силу многообразия ближайшего окружения молекулы воды. Таким образом, второй результат работы — измерение распределения OH-потенциалов в сети постоянно изменяющихся водородных связей. На следующем этапе исследований необходимо выяснить, возможно ли из спектров резонансного неупругого рассеяния воды определить такой важный структурный параметр, как среднее число связей молекулы. Он определяет энергию взаимодействия последней с её окружением, а значит, и такие свойства, как скорость звука в воде и её теплоёмкость»,— дополняет Фарис Гельмуханов, доктор физико-математических наук, профессор Королевского технологического института (Стокгольм, Швеция), старший научный сотрудник Сибирского федерального университета.
В работе также приняли участие учёные из Университета Потсдама (Германия), Университета Цюриха (Швейцария) и Университета Турку (Финляндия).
Рисунки
- A) Молекула воды, поглотив фотон, возбуждается из основного состояния (0) в высоковозбуждённое диссоциативное состояние (с), где атом водорода быстро покидает точку равновесия. В процессе диссоциации возбуждённая молекула возвращается в основное (0) или конечное состояние (f) испуская другой фотон и формируя спектр вблизи 535 эВ и 526 эВ, соответственно.
- Б) рентгеновский спектр поглощения воды.
- B) Спектры испускания c→f и c→0 вблизи 526 эВ и 535 эВ, соответственно. Эмиссионный спектр c→f вблизи 525 эВ показывает динамическое формирование (в процессе диссоциации) дублета с расщеплением Δ (см. панель A). При возвращении молекулы в основное состояние c→0 в процессе диссоциации заселяются высокие колебательные уровни, что формирует протяжённую колебательную прогрессию в районе 535 эВ.
- Г) В работе решена обратная задача восстановления из колебательной прогрессии распределения OH-потенциалов воды в жидкой фазе.
Как выглядят молекулы? — новости
Молекула представляет собой группу атомов, связанных вместе. Молекулы составляют почти все вокруг вас — вашу кожу, ваш стул и даже вашу еду.
Молекулы составляют почти все вокруг вас — вашу кожу, ваш стул и даже вашу еду.
Они различаются по размеру, но очень малы. Вы не можете увидеть отдельную молекулу своими глазами или даже микроскопом. Они в 100 000 раз меньше ширины волоса.
Самая маленькая молекула состоит из двух слипшихся атомов, а большая молекула может состоять из 100 000 или более атомов. Молекула может быть повторением одного и того же атома, например молекулы кислорода, которым мы дышим, или может состоять из множества атомов, например молекула сахара, состоящая из углерода, кислорода и водорода.
Но как выглядят молекулы? Все начинается с их строительных блоков: атомов.
Атом золота имеет плотный центр, состоящий из 79 протонов и 118 нейтронов, с более густым облаком из 79 электронов вокруг него. Иллюстрация создана Galarza Creador.
Противоположности притягиваются
Частицы вещества, из которых состоит атом, не одинаковы. Они могут иметь положительный заряд, отрицательный заряд или не иметь заряда. Ученые называют их протонами, электронами и нейтронами.
Ученые называют их протонами, электронами и нейтронами.
Незаряженные нейтроны и положительно заряженные протоны образуют тяжелый центр атома. Отрицательно заряженные электроны окружают этот небольшой центр.
Когда атомы приближаются друг к другу, чтобы потенциально соединиться и образовать молекулы, отрицательные электроны в одном атоме притягиваются к положительным протонам в другом, и наоборот. Оба атома приспосабливаются соответственно.
Когда атом один, отрицательные электроны, окружающие его центр, симметричны. При сближении двух атомов отрицательные электроны одного атома движутся к положительному центру другого атома. Кристин Хелмс, CC BY-SA
Это можно сравнить с попыткой выбрать место в классе. Есть некоторые правила. Например, вы должны оставаться в классе и не можете сидеть на ком-то сверху. Следуя этим правилам, вы можете попытаться сесть рядом со своими друзьями и подальше от врагов. Поиск идеального положения, чтобы все в классе были счастливы, похоже на поиск идеального положения атомов в молекуле.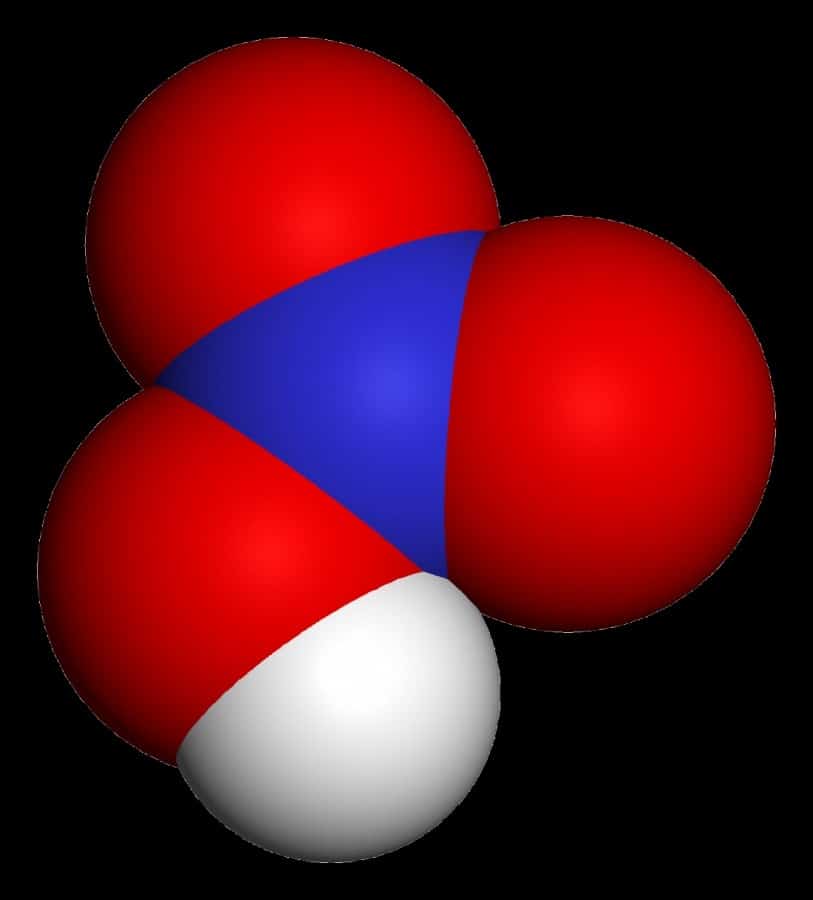 Иногда атомы не могут найти удачное расположение, и молекулы не образуются.
Иногда атомы не могут найти удачное расположение, и молекулы не образуются.
Увидеть невидимое
Если молекулы слишком малы, чтобы увидеть их невооруженным глазом или даже мощным микроскопом, как их видят ученые? Ответ заключается в том, что они разработали для этого специальные инструменты.
В одном инструменте используются рентгеновские лучи, о которых вы, возможно, знаете, поскольку врачи используют их, чтобы увидеть кости в теле. Рентгеновские лучи — это тип света, который человеческий глаз не может видеть, например, ультрафиолетовый или инфракрасный свет.
Когда ученые направляют рентгеновские лучи на молекулы, некоторые из них отражаются. Ученые могут записывать эти отраженные рентгеновские лучи и использовать их модели, чтобы выяснить, как выглядят отдельные молекулы.
Рентгеновские лучи, отражающиеся от атомов белковой молекулы, образуют черные точки на изображении выше. Расположение этих точек говорит ученым, как атомы расположены в молекуле. Del45/Wikimedia Commons, CC BY
Del45/Wikimedia Commons, CC BY
В 1912 году одной из первых молекул, замеченных таким образом, была соль (NaCl) — молекула, которая составляет ингредиент, который мы все знаем и любим в картофеле фри.
Ученые изобрели и другие методы наблюдения за молекулами. Подобно тому, как электроны меняют свое поведение, когда два атома сближаются, центр атома также может изменить свое поведение. Метод, называемый ядерным магнитным резонансом, обнаруживает эти изменения в центре атома и использует их в качестве подсказки, чтобы определить, какие атомы находятся поблизости.
Атомно-силовой микроскоп работает как хлипкая доска для прыжков в воду, которая трясется, когда вы идете и прыгаете по ней. Но этот трамплин чрезвычайно мал, настолько мал, что отрицательный заряд на его конце изгибает его к положительному центру атома. Перемещая этот трамплин и наблюдая, как он изгибается, можно показать расположение атомов в молекуле.
Анимация, показывающая, как работает атомно-силовой микроскоп.
Еще один метод, который ученые разработали для наблюдения за молекулами, называется криоэлектронной микроскопией. Во-первых, ученые замораживают молекулы до температуры, намного более низкой, чем температура снега или льда. Затем они стреляют электронами в молекулу и собирают те, которые проходят, чтобы создать изображение. Этот метод получил Нобелевскую премию по химии в 2017 г.
Схемы атомов, составляющих молекулы бензола (слева) и фуллерена (справа). Jynto (слева) Benjah-bmm27 (справа)/Wikimedia Commons
Каждая молекула уникальна — некоторые действительно разные. Например, бензол плоский, как блин, а фуллерен – круглый, как шар. Penguinone можно нарисовать похожим на пингвина, в то время как другие молекулы кажутся совершенно случайными. Но положение атомов в молекуле никогда не бывает случайным.
Хотя ученым известно, как выглядят многие молекулы, некоторые из них мы все еще пытаемся выяснить. Знание этих ответов может привести к изобретениям новых материалов и лекарств.
Автором этой статьи является Кристин Хелмс, доцент кафедры физики Ричмондского университета.
Эта статья переиздана из The Conversation под лицензией Creative Commons. Прочитайте оригинальную статью.
Как выглядят молекулы?
Любопытные дети — серия для детей всех возрастов. Если у вас есть вопрос, на который вы хотели бы получить ответ от эксперта, отправьте его на адрес любопытного[email protected].
Как выглядят молекулы? – Джастис Б., 6 лет, Уимберли, Техас
Молекула представляет собой группу атомов, связанных вместе. Молекулы составляют почти все вокруг вас — вашу кожу, ваш стул и даже вашу еду.
Они различаются по размеру, но очень малы. Вы не можете увидеть отдельную молекулу своими глазами или даже микроскопом. Они в 100 000 раз меньше ширины волоса.
Самая маленькая молекула состоит из двух слипшихся атомов, а большая молекула может состоять из 100 000 или более атомов. Молекула может быть повторением одного и того же атома, например молекулы кислорода, которым мы дышим, или может состоять из множества атомов, например молекула сахара, состоящая из углерода, кислорода и водорода.
Молекула может быть повторением одного и того же атома, например молекулы кислорода, которым мы дышим, или может состоять из множества атомов, например молекула сахара, состоящая из углерода, кислорода и водорода.
Но как выглядят молекулы? Все начинается с их строительных блоков: атомов.
Противоположности притягиваются
Частицы вещества, из которых состоит атом, не одинаковы. Они могут иметь положительный заряд, отрицательный заряд или не иметь заряда. Ученые называют их протонами, электронами и нейтронами.
Атом золота имеет плотный центр, состоящий из 79 протонов и 118 нейтронов, с более густым облаком из 79 электронов вокруг него. Иллюстрация создана Galarza Creador.
Незаряженные нейтроны и положительно заряженные протоны образуют тяжелый центр атома. Отрицательно заряженные электроны окружают этот небольшой центр.
Когда атомы приближаются друг к другу, чтобы потенциально соединиться и образовать молекулы, отрицательные электроны в одном атоме притягиваются к положительным протонам в другом, и наоборот. Оба атома приспосабливаются соответственно.
Оба атома приспосабливаются соответственно.
Когда атом один, отрицательные электроны, окружающие его центр, симметричны. При сближении двух атомов отрицательные электроны одного атома движутся к положительному центру другого атома.
Кристин Хелмс, CC BY-SA
Это можно сравнить с попыткой выбрать место в классе. Есть некоторые правила. Например, вы должны оставаться в классе и не можете сидеть на ком-то сверху. Следуя этим правилам, вы можете попытаться сесть рядом со своими друзьями и подальше от врагов. Поиск идеального положения, чтобы все в классе были счастливы, похоже на поиск идеального положения атомов в молекуле. Иногда атомы не могут найти удачное расположение, и молекулы не образуются.
Увидеть невидимое
Если молекулы слишком малы, чтобы увидеть их невооруженным глазом или даже мощным микроскопом, как их видят ученые? Ответ заключается в том, что они разработали для этого специальные инструменты.
В одном инструменте используются рентгеновские лучи, о которых вы, возможно, знаете, поскольку врачи используют их, чтобы увидеть кости в теле. Рентгеновские лучи — это тип света, который человеческий глаз не может видеть, например, ультрафиолетовый или инфракрасный свет.
Рентгеновские лучи — это тип света, который человеческий глаз не может видеть, например, ультрафиолетовый или инфракрасный свет.
Когда ученые направляют рентгеновские лучи на молекулы, некоторые из них отражаются. Ученые могут записывать эти отраженные рентгеновские лучи и использовать их модели, чтобы выяснить, как выглядят отдельные молекулы.
Рентгеновские лучи, отражающиеся от атомов белковой молекулы, образуют черные точки на изображении выше. Расположение этих точек говорит ученым, как атомы расположены в молекуле.
Del45/Wikimedia Commons, CC BY
В 1912 году одной из первых молекул, увиденных таким образом, была соль (NaCl) — молекула, которая составляет ингредиент, который мы все знаем и любим в картофеле фри.
Ученые изобрели и другие методы наблюдения за молекулами. Подобно тому, как электроны меняют свое поведение, когда два атома сближаются, центр атома также может изменить свое поведение. Метод, называемый ядерным магнитным резонансом, обнаруживает эти изменения в центре атома и использует их в качестве подсказки, чтобы определить, какие атомы находятся поблизости.
Атомно-силовой микроскоп работает как хлипкая доска для прыжков в воду, которая трясется, когда вы идете и прыгаете по ней. Но этот трамплин чрезвычайно мал, настолько мал, что отрицательный заряд на его конце изгибает его к положительному центру атома. Перемещая этот трамплин и наблюдая, как он изгибается, можно показать расположение атомов в молекуле.
Анимация, показывающая, как работает атомно-силовой микроскоп.
Еще один метод, который ученые разработали для наблюдения за молекулами, называется криоэлектронной микроскопией. Во-первых, ученые замораживают молекулы до температуры, намного более низкой, чем температура снега или льда. Затем они стреляют электронами в молекулу и собирают те, которые проходят, чтобы создать изображение. Этот метод получил Нобелевскую премию по химии в 2017 г.
Все формы и размеры
Так как же выглядят молекулы? Они представляют собой группу атомов, центр которой содержит большую часть материала, а остальная часть представляет собой в основном пустое пространство. У каждого атома есть определенное положение, в котором он счастлив, как и ученики в этом классе.
У каждого атома есть определенное положение, в котором он счастлив, как и ученики в этом классе.
Схемы атомов, составляющих молекулы бензола (слева) и фуллерена (справа).
Джинто (слева) Бенджа-bmm27 (справа)/Wikimedia Commons
Каждая молекула уникальна, некоторые действительно разные. Например, бензол плоский, как блин, а фуллерен – круглый, как шар. Penguinone можно нарисовать похожим на пингвина, в то время как другие молекулы кажутся совершенно случайными. Но положение атомов в молекуле никогда не бывает случайным.
Хотя ученым известно, как выглядят многие молекулы, некоторые из них мы все еще пытаемся выяснить. Знание этих ответов может привести к изобретениям новых материалов и лекарств.
Привет, любознательные дети! У вас есть вопрос, на который вы хотели бы получить ответ от эксперта? Попросите взрослого отправить ваш вопрос по адресу [email protected]. Пожалуйста, сообщите нам ваше имя, возраст и город, в котором вы живете.