Содержание
Инженерные фаги против устойчивых бактерий
09.10.2019
09.10.2019
Подготовила
Елена Фетисова
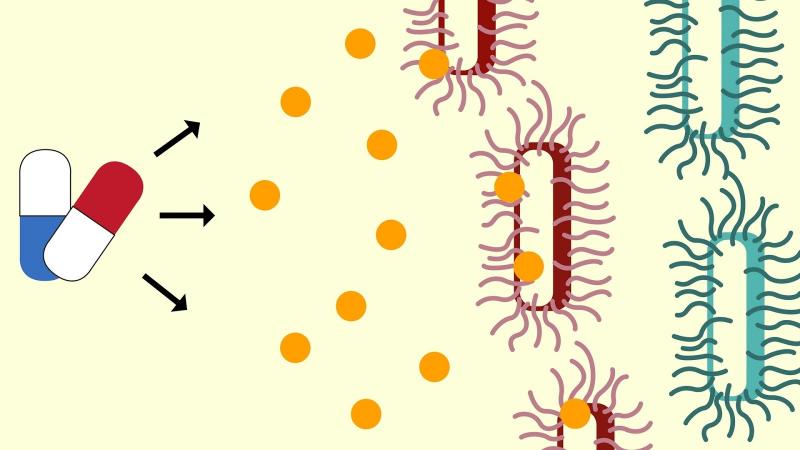
Ученые из Массачусетского технологического института разработали подход, позволяющий быстро изменять специфичность бактериофагов к клеткам-хозяевам. Инженерные фаги, полученные в ходе исследования, подавляли рост бактерий in vitro и in vivo, а также замедляли развитие резистентности.
Подготовила
Елена Фетисова
Развитие бактериальной устойчивости к антибиотикам пробуждает все больший интерес к препаратам на основе бактериофагов. Важным преимуществом фаговой терапии является селективность к бактериальным штаммам, основанная на взаимодействии с определенными молекулами на поверхности клеток — фагоспецифическими рецепторами. Однако мутации в генах, отвечающих за синтез этих рецепторов, могут способствовать развитию резистентности.
Однако мутации в генах, отвечающих за синтез этих рецепторов, могут способствовать развитию резистентности.
Для повышения эффективности терапии используют смесь фагов, действующих на несколько рецепторов, однако такая стратегия усложняет изучение свойств препарата. Авторы исследования, опубликованного в Cell, разработали подход, который позволяет менять специфичность фагов к клеткам-хозяевам в краткие сроки.
Первоначальное взаимодействие фага с клеткой происходит за счет его хвостовых фибрилл. При изучении коэволюции штамма E.coli и фага T3 ученые обнаружили участок на дистальном конце фибрилл, определяющий диапазон клеток-хозяев. Участок состоит из бета-листов, соединенных вариабельными петлями длиной 4–9 аминокислотных остатков. Мутации в этих участках практически не сказываются на структуре белка, но существенно влияют на взаимодействие с бактерией.
Ген фибриллы клонировали в плазмиду и амплифицировали с применением вырожденных праймеров, чтобы создать мутантные версии гена. Библиотеку плазмид использовали для трансформации бактерий, которых затем инфицировали фагом T3. В результате ученые получили библиотеки фагов, содержащих мутации в различных петлях за счет рекомбинации с плазмидой.
Библиотеку плазмид использовали для трансформации бактерий, которых затем инфицировали фагом T3. В результате ученые получили библиотеки фагов, содержащих мутации в различных петлях за счет рекомбинации с плазмидой.
Для скрининга штаммы бактерий с редуцированными поверхностными липополисахаридами, устойчивые к фагу T3 дикого типа, инфицировали фагами из полученных библиотек. Исследование показало, что мутации в определенных петлях способствуют связыванию с более разнообразными клетками-хозяевами и мутантные фаги подавляют рост устойчивых штаммов. Кроме того, смесь мутантных бактериофагов препятствует развитию резистентности существенно дольше, чем исходный T3 (который также способен мутировать вслед за бактерией). Эффективность инженерных бактериофагов была подтверждена на мышиной модели раневой инфекции.
Авторы исследования подчеркивают, что на создание данного подхода их вдохновила инженерия антител, направленная на тонкую настройку специфичности и селективности за счет изменений в вариабельных фрагментах. Поэтому для своих инженерных фагов они предложили название «фаготела» (от англ. «phagebodies»). Ученые предполагают, что их подход может быть применен для борьбы с другими патогенными бактериями, имеющими иные механизмы устойчивости.
Поэтому для своих инженерных фагов они предложили название «фаготела» (от англ. «phagebodies»). Ученые предполагают, что их подход может быть применен для борьбы с другими патогенными бактериями, имеющими иные механизмы устойчивости.
Источник
Kevin Yehl, et al. // Engineering Phage Host-Range and Suppressing Bacterial Resistance through Phage Tail Fiber Mutagenesis. // Cell, 2019; DOI:
10.1016/j.cell.2019.09.015
Новые препараты Вирусология Бактериология Молбиология Методология эксперимента Новые концепции
Добавить в избранное
Подписаться
Вариант гена, связанный с детской эпилепсией, сохраняется в популяции 800 лет
Медицинские генетики стран Евразии объединяются
Шанс попасть во вторую волну эпидемии довольно велик в Москве, но этот исход не выглядит неизбежным
Завлабы
Александр Филатов: «Длинные пустые коридоры, а на полу лежит “лунная” пыль»
Мицелиальный гриб помог увеличить синтез лекарства для лечения болезней печени
7 сентября, 2022 13:23
Источник:
Naked Science
Российские ученые предложили микробиологический метод, позволяющий эффективно синтезировать урсодезоксихолевую кислоту — препарат, который широко используется при лечении различных заболеваний печени. Традиционно ее получают в процессе сложных химических реакций, которые малоэффективны и экологически небезопасны. Авторы «научили» мицелиальный гриб, способный вызывать болезни зерновых культур, синтезировать урсодезоксихолевую кислоту из вещества-предшественника с выходом до 88%. Такой подход позволит упростить и удешевить производство важного для медицины соединения.
Традиционно ее получают в процессе сложных химических реакций, которые малоэффективны и экологически небезопасны. Авторы «научили» мицелиальный гриб, способный вызывать болезни зерновых культур, синтезировать урсодезоксихолевую кислоту из вещества-предшественника с выходом до 88%. Такой подход позволит упростить и удешевить производство важного для медицины соединения.
Поделиться
Регенерация протопластов Gibberella zeae без обработки ультрафиолетом (а) и после обработки в течение двух, трех, пяти и шести минут (b, c, d, e) / ©Kollerov V. and Donova M. / AMB Express, 2022
Результаты исследования, поддержанного грантом Российского научного фонда (РНФ), опубликованы в журнале AMB Express. Урсодезоксихолевая кислота — лекарственное средство, используемое в современной медицине для лечения и профилактики хронических, воспалительных заболеваний печени, к которым относятся гепатит и цирроз, а также для растворения камней в желчном пузыре. Кроме того, препарат предотвращает развитие рака толстой кишки.
Кроме того, препарат предотвращает развитие рака толстой кишки.
На сегодняшний день урсодезоксихолевую кислоту в промышленных масштабах производят химически, но этот процесс сложен, экологически небезопасен и малоэффективен — лишь 30% вещества-предшественника превращается в нужное соединение. Ученые разрабатывают альтернативные способы получения урсодезоксихолевой кислоты, и наиболее перспективно с этой точки зрения использование микроорганизмов-продуцентов, которые способны ее синтезировать.
Микрофотографии гриба Gibberella zeae / ©Kollerov V. and Donova M. / AMB Express, 2022
Ранее биотехнологи из Института биохимии и физиологии микроорганизмов имени Г. К. Скрябина Пущинского научного центра биологических исследований РАН (Пущино) исследовали способность различных микроскопических грибов синтезировать урсодезоксихолевую кислоту из вещества-предшественника (литохолевой кислоты) и выявили наиболее перспективный штамм гриба Gibberella zeae, также известного как фузариум злаковый, обладающий высокой активностью фермента, необходимого для такого превращения. Использование этого штамма позволяет получать целевой продукт в одну биотехнологическую стадию с двукратным увеличением выхода по сравнению с химическим синтезом.
Использование этого штамма позволяет получать целевой продукт в одну биотехнологическую стадию с двукратным увеличением выхода по сравнению с химическим синтезом.
В новой работе авторам удалось повысить продуктивность грибной культуры в синтезе урсодезоксихолевой кислоты до 88%. Для этого исследователи получили мутантные штаммы с повышенной активностью. Ученые разработали оригинальную процедуру получения протопластов — клеток гриба, не имеющих клеточной стенки. Активно растущий мицелий, или тело гриба, на подходящей питательной среде обработали специальными ферментами, разрушающими клеточную стенку.
Это было необходимо для последующего мутагенеза с помощью ультрафиолетового облучения и для получения мутантных клонов с большим числом случайных мутаций, среди которых оказалась бы нужная. В результате эксперимента авторы выявили 27 клонов, три из которых синтезировали на 10-30% больше урсодезоксихолевой кислоты, чем исходные клетки родительского штамма.
«Мы определили оптимальные условия для роста и получения протопластов грибной культуры Gibberella zeae и их мутагенеза.Это позволило значительно повысить эффективность микробиологического синтеза урсодезоксихолевой кислоты. В дальнейшем мы планируем определить ген, ответственный за синтез фермента, катализирующего ключевую реакцию этого процесса. Это позволит изучить его молекулярные механизмы, а также условия, способствующие дальнейшему увеличению продуктивности грибной культуры», — рассказывает руководитель проекта, поддержанного грантом РНФ, Марина Донова, доктор биологических наук, профессор, главный научный сотрудник Института биохимии и физиологии микроорганизмов имени Г. К. Скрябина Пущинского научного центра биологических исследований РАН.
Если вы хотите стать героем публикации и рассказать о своем исследовании, заполните форму на сайте РНФ.
Теги
Биология, Спецпроект
Бактерии идут на смертельный риск, чтобы выжить — ScienceDaily
Science News
от исследовательских организаций
- Дата:
- 2 мая 2017 г.

- Источник:
- КУ Левен
- Резюме:
- Бактерии нуждаются в мутациях — изменениях в их коде ДНК — чтобы выжить в сложных условиях. При необходимости они могут даже мутировать с разной скоростью. Полученные результаты открывают новые возможности для исследований, начиная от более эффективных методов производства биотоплива и заканчивая более эффективным лечением бактериальных инфекций и рака.
- Поделиться:
ПОЛНАЯ ИСТОРИЯ
Бактерии нуждаются в мутациях — изменениях в их коде ДНК — чтобы выжить в трудных обстоятельствах. При необходимости они могут даже мутировать с разной скоростью. Это показано в недавнем исследовании Центра микробной и растительной генетики KU Leuven (Лёвенский университет), Бельгия. Полученные результаты открывают новые возможности для исследований, начиная от более эффективных методов производства биотоплива и заканчивая более эффективным лечением бактериальных инфекций и рака.
реклама
Когда они находятся в состоянии стресса, бактерии начинают мутировать, чтобы произвести один или несколько вариантов ДНК, которые позволяют бактериям выживать и размножаться. Но мутация опасна при нормальных обстоятельствах, поскольку она ослабляет бактерии. Таким образом, хитрость заключается в том, чтобы найти баланс между слишком большим количеством и слишком малым количеством мутаций. Потеря этого баланса означает гипермутацию: клетка мутирует гораздо быстрее, чем обычно, что в конечном итоге приводит к гибели.
Но мутация опасна при нормальных обстоятельствах, поскольку она ослабляет бактерии. Таким образом, хитрость заключается в том, чтобы найти баланс между слишком большим количеством и слишком малым количеством мутаций. Потеря этого баланса означает гипермутацию: клетка мутирует гораздо быстрее, чем обычно, что в конечном итоге приводит к гибели.
Поскольку научные знания о роли гипермутации все еще ограничены, исследователи из Калифорнийского университета в Лёвене изучили ее основной механизм в кишечных бактериях Кишечная палочка . « E.coli является печально известной причиной диареи, но большинство штаммов E.coli на самом деле являются безвредными кишечными бактериями, обнаруженными у людей и животных», — говорит профессор Ян Михилс. «Воздействие высоких, почти смертельных концентраций этанола вызывает гипермутацию в E.coli . Мы были удивлены, обнаружив, что скорость гипермутации у бактерий может быстро изменяться: бактерии мутируют быстрее при более высоких концентрациях этанола и медленнее, когда стресс от этанола снимается. Как только опасность минует, бактерии нажимают на тормоз и пытаются вернуться в свое нормальное состояние без гипермутации».
Как только опасность минует, бактерии нажимают на тормоз и пытаются вернуться в свое нормальное состояние без гипермутации».
Гипермутация позволила бактериям пережить стресс от этанола и позволила исследователям выбрать мутанты E. coli, которые очень устойчивы к этанолу. Это открывает новые перспективы для исследований в области производства биотоплива. «В процессе производства биотоплива сахар получают из растительных остатков и подобных отходов. Этот сахар, в свою очередь, превращается в этанол. Для этой цели можно использовать бактерии E.coli : они могут превращать сахара в этанол, но этанол, который они производят. Гипермутация позволила нам получить варианты, которые менее восприимчивы к этанолу и быстро растут. Это означает, что мы могли бы использовать их для более эффективного производства биотоплива».
«Другое применение — борьба с устойчивостью бактерий к антибиотикам и устойчивостью раковых клеток к химиотерапии», — добавляет докторант Тун Свингс. «Антибиотики представляют смертельную угрозу для бактерий. Бактерии защищают себя, мутируя, и в результате у них развивается устойчивость к антибиотикам. То же самое относится и к раковым клеткам после лечения. Поэтому блокирование гипермутации может стать возможным лечением или, возможно, даже новым котерапия».
Бактерии защищают себя, мутируя, и в результате у них развивается устойчивость к антибиотикам. То же самое относится и к раковым клеткам после лечения. Поэтому блокирование гипермутации может стать возможным лечением или, возможно, даже новым котерапия».
изменить мир к лучшему: спонсируемая возможность
Источник истории:
Материалы предоставлены KU Leuven . Примечание. Содержимое можно редактировать по стилю и длине.
Ссылка на журнал :
- Toon Swings, Брэм Ван ден Берг, Сандер Вуйтс, Элин Ойен, Карин Вурдекерс, Кевин Дж. Верстрепен, Мартен Фоварт, Натали Верстратен, Ян Михилс. Адаптивная настройка частоты мутаций позволяет быстро реагировать на летальный стресс у Escherichia coli . eLife , 2017; 6 DOI: 10.7554/eLife.22939
Цитировать эту страницу :
- MLA
- АПА
- Чикаго
КУ Левен.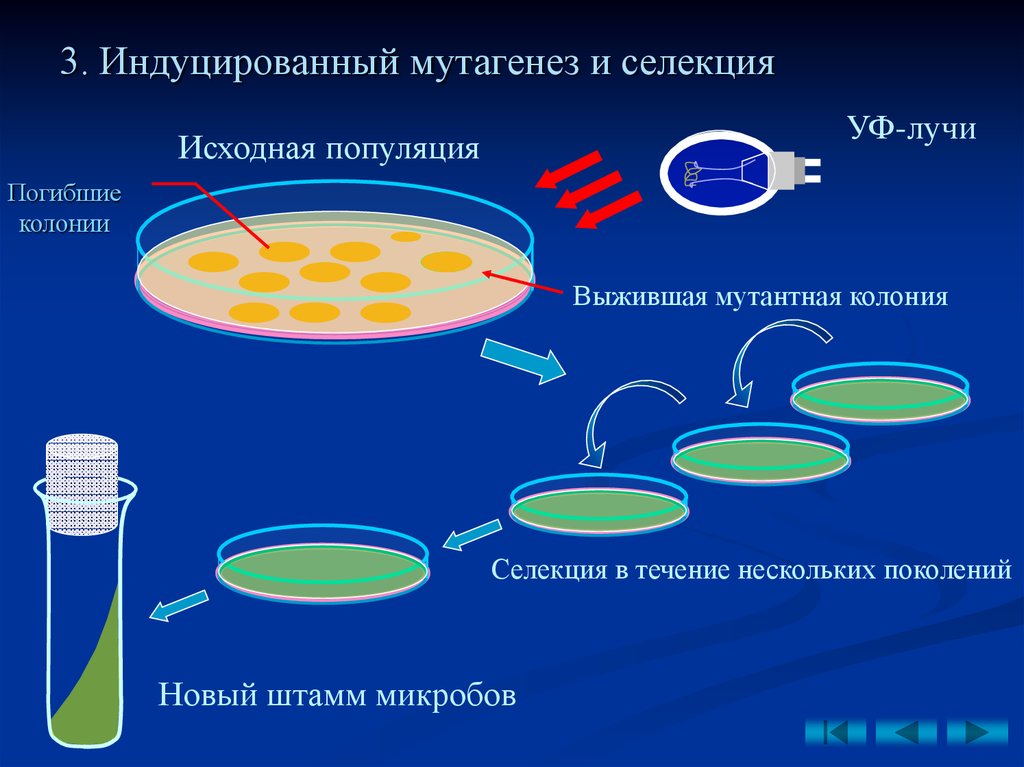 «Бактерии идут на смертельный риск, чтобы выжить». ScienceDaily. ScienceDaily, 2 мая 2017 г.
«Бактерии идут на смертельный риск, чтобы выжить». ScienceDaily. ScienceDaily, 2 мая 2017 г.
КУ Левен. (2017, 2 мая). Бактерии идут на смертельный риск, чтобы выжить. ScienceDaily . Получено 30 октября 2022 г. с сайта www.sciencedaily.com/releases/2017/05/170502112545.htm
КУ Левен. «Бактерии идут на смертельный риск, чтобы выжить». ScienceDaily. www.sciencedaily.com/releases/2017/05/170502112545.htm (по состоянию на 30 октября 2022 г.).
реклама
Бактерии, устойчивые к антибиотикам — Better Health Channel
Резюме
Читать полный информационный бюллетень
- Устойчивость к антибиотикам является серьезной проблемой общественного здравоохранения.
- Некоторые бактерии, способные вызывать серьезные заболевания, становятся устойчивыми к наиболее распространенным антибиотикам.

- Устойчивые к антибиотикам бактерии могут передаваться от человека к человеку в обществе или от пациента к пациенту в больнице.
- Тщательные процедуры инфекционного контроля могут свести к минимуму распространение этих бактерий в больницах.
- Надлежащая личная гигиена может свести к минимуму распространение этих бактерий в обществе.
- Тщательное назначение антибиотиков сведет к минимуму развитие более устойчивых к антибиотикам штаммов бактерий.
Антибиотики используются для уничтожения бактерий, которые могут вызывать заболевания. Они внесли большой вклад в здоровье человека. Многие болезни, которые когда-то убивали людей, теперь можно эффективно лечить с помощью антибиотиков. Однако некоторые бактерии стали устойчивыми к обычно используемым антибиотикам.
Бактерии, устойчивые к антибиотикам, — это бактерии, которые не контролируются и не уничтожаются антибиотиками. Они способны выживать и даже размножаться в присутствии антибиотика. Большинство инфекционных бактерий могут стать устойчивыми по крайней мере к некоторым антибиотикам. Бактерии, устойчивые ко многим антибиотикам, известны как полирезистентные организмы (MRO).
Они способны выживать и даже размножаться в присутствии антибиотика. Большинство инфекционных бактерий могут стать устойчивыми по крайней мере к некоторым антибиотикам. Бактерии, устойчивые ко многим антибиотикам, известны как полирезистентные организмы (MRO).
Устойчивость к антибиотикам является серьезной проблемой общественного здравоохранения. Его можно предотвратить, сводя к минимуму ненужное назначение и чрезмерное назначение антибиотиков, правильно используя назначенные антибиотики, а также соблюдая правила гигиены и инфекционного контроля.
Некоторые бактерии естественным образом устойчивы к некоторым антибиотикам. Например, бензилпенициллин очень слабо влияет на большинство микроорганизмов, обитающих в пищеварительной системе человека (кишечнике).
Бактерии, устойчивые к антибиотикам
Некоторые бактерии выработали устойчивость к антибиотикам, которые когда-то широко использовались для их лечения. Например, Staphylococcus aureus («золотой стафилококк» или MRSA) и Neisseria gonorrhoeae (возбудитель гонореи) в настоящее время почти всегда устойчивы к бензилпенициллину.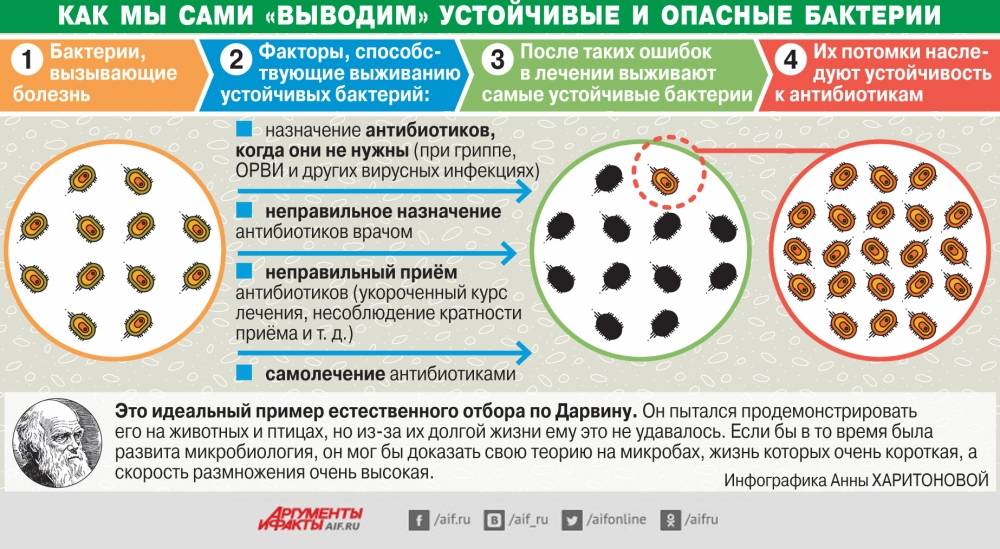 В прошлом эти инфекции обычно контролировались пенициллином.
В прошлом эти инфекции обычно контролировались пенициллином.
Самая серьезная проблема с устойчивостью к антибиотикам заключается в том, что некоторые бактерии стали устойчивыми почти ко всем легкодоступным антибиотикам. Эти бактерии способны вызывать серьезные заболевания, и это является серьезной проблемой общественного здравоохранения. Важные примеры:
- метициллин-резистентный Staphylococcus aureus (MRSA)
- ванкомицин-резистентный Enterococcus (VRE)
- мультирезистентный Mycobacterium tuberculosis (MDR-TB)
- устойчивый к карбапенемам Enterobacteriaceae (9CRE) кишечные бактерии0075
Способы предотвращения устойчивости к антибиотикам
Наиболее важными способами предотвращения устойчивости к антибиотикам являются:
- Минимизация ненужного и чрезмерного назначения антибиотиков. Это происходит, когда люди ожидают, что врачи пропишут антибиотики при вирусном заболевании (антибиотики не действуют против вирусов) или когда антибиотики назначают при состояниях, которые в них не нуждаются.

- Пройдите весь курс любого назначенного антибиотика, чтобы он был полностью эффективным и не вызывал резистентности.
- Соблюдайте правила гигиены, такие как мытье рук, и используйте соответствующие процедуры инфекционного контроля.
Передача устойчивых к антибиотикам бактерий в больницах
Распространенные пути передачи бактерий от человека к человеку включают:
- контакт с загрязненными руками персонала больницы
- контакт с загрязненными поверхностями, такими как дверные ручки, прикроватные тумбочки и звонки
- контакт с загрязненным оборудованием, таким как стетоскопы и манжеты для измерения артериального давления.
Инфекционный контроль в больницах
Стандартные меры предосторожности в больницах — это методы работы, обеспечивающие базовый уровень инфекционного контроля для всех людей, независимо от их диагноза или предполагаемого инфекционного статуса.
Эти меры предосторожности должны соблюдаться во всех больницах и медицинских учреждениях и включают:
- надлежащую личную гигиену, такую как мытье рук до и после контакта с пациентом и надлежащее использование растворов для обработки рук на спиртовой основе
- использование барьерного оборудования, такого как перчатки, халаты, маски и защитные очки
- надлежащее обращение с острыми предметами (например, иглами) и медицинскими отходами (отходы, образующиеся во время ухода за пациентами) и их утилизация
- асептические (стерильные) методы.

Соблюдение стандартных мер предосторожности сводит к минимуму риск передачи инфекции от человека к человеку даже в ситуациях высокого риска.
Дополнительные меры предосторожности в отношении устойчивых к антибиотикам бактерий
Дополнительные меры предосторожности используются при уходе за людьми, которые, как известно или подозреваются, инфицированы или колонизированы высокоинфекционными патогенами (микроорганизмами, вызывающими заболевания).
Микроорганизмы могут быть классифицированы как «высокий риск», если:
- их путь передачи делает их более заразными – они могут распространяться контактным или воздушно-капельным путем
- они вызываются устойчивыми к антибиотикам бактериями
- они устойчивы к стандартным процедурам стерилизации.
Дополнительные меры предосторожности адаптированы к конкретному возбудителю и пути передачи. Дополнительные меры предосторожности могут включать:
- использование отдельной палаты с ванными комнатами или отдельным туалетом
- специальное оборудование для ухода за этим человеком
- ограничение передвижения человека и его медицинских работников.

Устойчивые к антибиотикам бактерии также могут передаваться от человека к человеку внутри сообщества. Это становится все более распространенным явлением.
Способы предотвращения передачи микроорганизмов, в том числе устойчивых к антибиотикам бактерий, следующие:
- Мыть руки до и после обработки пищевых продуктов, посещения туалета и смены подгузников.
- Прикрывайте нос и рот при кашле и чихании.
- Используйте салфетки, чтобы высморкаться или вытереть нос.
- Выбрасывайте салфетки надлежащим образом: в мусор или в туалет.
- Не плюйся.
- Оставайтесь дома, если вы плохо себя чувствуете и не можете справиться с обычными повседневными делами.
- Не отдавайте детей в детский сад, детский сад или школу, если они плохо себя чувствуют.
- Если вам прописали антибиотики, пройдите весь курс — не останавливайтесь, потому что вы чувствуете себя лучше.
- Если вы по-прежнему плохо себя чувствуете, обратитесь к врачу.


 Это позволило значительно повысить эффективность микробиологического синтеза урсодезоксихолевой кислоты. В дальнейшем мы планируем определить ген, ответственный за синтез фермента, катализирующего ключевую реакцию этого процесса. Это позволит изучить его молекулярные механизмы, а также условия, способствующие дальнейшему увеличению продуктивности грибной культуры», — рассказывает руководитель проекта, поддержанного грантом РНФ, Марина Донова, доктор биологических наук, профессор, главный научный сотрудник Института биохимии и физиологии микроорганизмов имени Г. К. Скрябина Пущинского научного центра биологических исследований РАН.
Это позволило значительно повысить эффективность микробиологического синтеза урсодезоксихолевой кислоты. В дальнейшем мы планируем определить ген, ответственный за синтез фермента, катализирующего ключевую реакцию этого процесса. Это позволит изучить его молекулярные механизмы, а также условия, способствующие дальнейшему увеличению продуктивности грибной культуры», — рассказывает руководитель проекта, поддержанного грантом РНФ, Марина Донова, доктор биологических наук, профессор, главный научный сотрудник Института биохимии и физиологии микроорганизмов имени Г. К. Скрябина Пущинского научного центра биологических исследований РАН.