Содержание
Неинвазивная стимуляция мозга | Официальный сайт Научного центра неврологии
В отделении нейрореабилитации и физиотерапии используются следующие методы неинвазивной стимуляции мозга:
Транскраниальная магнитная стимуляция (ТМС) — это метод, основанный на стимуляции нейронов головного мозга переменным магнитным полем без инвазивного вмешательства.
Метод ТМС используется для:
определения возбудимости моторной коры и проведения по кортикоспинальным трактам;
картирования (определения локализации) моторных и немоторных функций в коре головного мозга;
направленного влияния на возбудимость коры и нейропластичность (ритмическая ТМС)
Системы навигационной ТМС учитывают индивидуальную анатомию конкретного человека позволяют наносить стимул целенаправленно и локально, c опорой на МРТ-данные. Одной из таких систем является система навигационной транскраниальной магнитной стимуляции мозга (нТМС) — NBS eXimia Nexstim (Nexstim Ltd. , Хельсинки, Финляндия), использующаяся в нашем отделении.
, Хельсинки, Финляндия), использующаяся в нашем отделении.
Ритмическая ТМС – метод ТМС, использующийся для лечения или реабилитации пациентов с заболеваниями нервной системы. Ритмическая ТМС по результатам крупных международных исследований обладает доказанной эффективностью при ряде заболеваний. В нашем отделении при отсутствии противопоказаний ритмическая ТМС применяется при следующих состояниях:
- депрессия
- нейропатическая боль
- постинсультный гемипарез (после 3 месяцев от НМК)
- невралгия тройничного нерва
- спинальная спастичность при рассеянном склерозе
- речевые нарушения (афазия)
- болезнь Паркинсона
- шум в ушах
Определение показаний и противопоказаний к ТМС, продолжительности курса терапии возможно при очной консультации сотрудника отделения.
Проведение транскраниальной магнитной стимуляции также возможно в рамках научных исследований.
Транскраниальная электрическая стимуляция (ТЭС) – метод неинвазивной стимуляции мозга, основанный на воздействии на кору головного мозга слабым электрическим полем. ТЭС используется для направленного изменения активности регионов коры головного мозга.
ТЭС используется для направленного изменения активности регионов коры головного мозга.
Проведенные исследования показали потенциал для применения этого метода при депрессии, болевых синдромах, фибромиалгии, двигательных, речевых и зрительных нарушениях после инсульта, паркинсонизме и ряде других заболеваний. В нашем отделении при отсутствии противопоказаний ТЭС применяется при следующих состояниях:
- постинсультный гемипарез (после 3 месяцев от НМК)
- фибромиалгия
- хронические болевые синдромы
Определение показаний и противопоказаний к ТЭС, продолжительности курса терапии возможно при очной консультации сотрудника отделения.
Проведение транскраниальной электрической стимуляции также возможно в рамках научных исследований.
Репортажи в СМИ:
https://www.neurology.ru/videosyuzhety/reabilitaciya-posle-insulta-progr…
https://www.neurology.ru/video-lekcii-legostaevoy-l-kak-uchyonye-issledu…
https://www.neurology. ru/videosyuzhety/programma-tk-doktor-kliniki-rossi…
ru/videosyuzhety/programma-tk-doktor-kliniki-rossi…
https://www.neurology.ru/videosyuzhety/diagnostika-hronicheskih-narushen…
https://www.neurology.ru/moskovskie-vrachi-razrabotali-tehnologiyu-po-vo…
https://www.neurology.ru/videosyuzhety/syuzhet-o-rabote-nauchnogo-centra…
Основные публикации сотрудников отделения по неинвазивной стимуляции мозга:
1. Sinitsyn D. O., Chernyavskiy A. Y., Poydasheva A. G., Bakulin I. S., Suponeva N. A., Piradov M. A. Optimization of the navigated tms mapping algorithm for accurate estimation of cortical muscle representation characteristics. BRAIN SCIENCES 2019; 9(4): 1–21.
2. Korzhova J., Bakulin I., Sinitsyn D., Poydasheva A., Suponeva N., Zakharova M., Piradov M. High-frequency rtms and itbs for spasticity management in secondary-progressive multiple sclerosis. European Journal of Neurology 2019; 26(4): 680-e44.
3. Пойдашева А. Г., Бакулин И. С., Легостаева Л. А., Супонева Н. А., Пирадов М. А. Метод ТМС-ЭЭГ: возможности и перспективы. Журнал высшей нервной деятельности им. И. П. Павлова 2019: 69(3): 267–279.
А. Метод ТМС-ЭЭГ: возможности и перспективы. Журнал высшей нервной деятельности им. И. П. Павлова 2019: 69(3): 267–279.
4. Бакулин И. С., Пойдашева А. Г., Павлов Н. А., Супонева Н. А., Пирадов М. А., Афтанас Л. И. Транскраниальная электрическая стимуляция в улучшении функции руки при инсульте. Успехи физиологических наук 2019: 50(1): 90–104.
5. Chervyakov Alexander V., Poydasheva Alexandra G., Lyukmanov Roman H., Suponeva Natalia A., Chernikova Ludmila A., Piradov Michael A., Ustinova Ksenia I. Effects of Navigated Repetitive Transcranial Magnetic Stimulation After Stroke // Journal of Clinical Neurophysiology, 2018. 35(2): p. 166-172
6. Korzhova J., Sinitsyn D., Chervyakov A., Poydasheva A., Zakharova M., Suponeva N., Chernikova L., Piradov M. Transcranial and spinal cord magnetic stimulation in treatment of spasticity. A literature review and meta-analysis // European Journal of Physical and Rehabilitation Medicine 2018; 54(1): 75-84.
7. Супонева Н.А., Бакулин И. С., Пойдашева А.Г., Пирадов М.А., Безопасность транскраниальной магнитной стимуляции: обзор международных рекомендаций и новые данные // Нервно-мышечные болезни, 2017. 7(2): с. 21-36
С., Пойдашева А.Г., Пирадов М.А., Безопасность транскраниальной магнитной стимуляции: обзор международных рекомендаций и новые данные // Нервно-мышечные болезни, 2017. 7(2): с. 21-36
8. Пойдашева А.Г., Азиатская Г.А., Чернявский А.Ю., Люкманов Р.Х., Мокиенко О.А., Черникова Л.А., Супонева Н.А., Фролов А.А., Пирадов М.А. Динамика коркового моторного представительства общего разгибателя пальцев на фоне обучения представлению движений с помощью интерфейса мозг-компьютер: контролируемое исследование // Журнал высшей нервной деятельности им. И. П. Павлова, 2017. 67(4): с. 473-484
9. Пойдашева А.Г., Бакулин И.С., Чернявский А.Ю., Супонева Н.А., Пирадов М.А., Картирование корковых представительств мышц с помощью навигационной транскраниальной магнитной стимуляции: возможности применения в клинической практике // Медицинский алфавит, 2017. 2(22): с. 21-25
10. Chervyakov A.V., Belopasova A.V., Poydasheva A.G., Chernikova L.A., Kadykov A.S., Suponeva N.A., Piradov M.A. Transcranial magnetic stimulation for the treatment of central post-stroke pain // Human Physiology, 2016. 42(8): p. 844-849
42(8): p. 844-849
11. Коржова Ю.Е., Червяков А.В., Пойдашева А.Г., Кочергин И.А., Переседова А.В., Захарова М.Н., Супонева Н.А., Черникова Л.А., Пирадов М.А. Применение транскраниальной магнитной стимуляции в лечении синдрома спастичности при вторично-прогредиентном рассеянном склерозе // Вопросы курортологии, физиотерапии и лечебной физической культуры, 2016. 93(5): с. 8-13
12. Chervyakov A., Sinitsyn D., Chernyavsky A., Piradov, M. Possible mechanisms underlying the therapeutic effects of transcranial magnetic stimulation. Frontiers in Human Neuroscience 2015; 9: 303.
13. Червяков А. В., Пойдашева А. Г., Коржова Ю. Е., Супонева Н. А., Черникова Л. А., Пирадов М. А. Ритмическая транскраниальная магнитная стимуляция в неврологии и психиатрии. Журнал неврологии и психиатрии им. С.С.Корсакова 2015; 12: 7-18.
14. Chervyakov A. V., Bakulin I. S., Savitskaya N. G., Arkhipov I. V., Gavrilov A. V., Zakharova M. N., Piradov M. A. Navigated transcranial magnetic stimulation in amyotrophic lateral sclerosis. Muscle and Nerve 2015; 51(1): 125–131.
Muscle and Nerve 2015; 51(1): 125–131.
Магнитная стимуляция
Магнитная стимуляция
Уникальная методика диагностики и лечения стала доступна во Владивостоке и успешно применяется в Институте вертеброневрологии и мануальной медицины, где есть собственный аппарат «Нейро-МС/Д» с максимальным уровнем функциональности.
Специалисты нашей клиники с помощью этого прибора способны диагностировать весь спектр отклонений в работе нервной системы и готовы использовать весь потенциал стимулятора для реализации любых диагностических и терапевтических программ.
Что такое магнитная стимуляция?
Лечебная ритмическая магнитная стимуляция – это неинвазивная безболезненная методика, не имеющая побочных эффектов и один из немногих доступных способов в реальном времени, без применения лекарств, активировать пострадавшие участки головного, спинного мозга и периферических нервов.
Мощный магнитный импульс приводит к возникновению электрического тока в тканях. Индуцируемое электрическим током магнитное поле вызывает тормозящий или возбуждающий эффект. Стимуляция с низкой частотой 1 Гц и меньше обычно обладает тормозящим действием, а стимуляция с высокой частотой повышает возбудимость мотонейронов.
Индуцируемое электрическим током магнитное поле вызывает тормозящий или возбуждающий эффект. Стимуляция с низкой частотой 1 Гц и меньше обычно обладает тормозящим действием, а стимуляция с высокой частотой повышает возбудимость мотонейронов.
Магнитная стимуляция совершенно безопасна при частоте ниже 10 Гц даже при продолжительных стимуляциях до 6-8 недель.
Самое большое преимущество магнитной стимуляции по сравнению с электрической стимуляцией является то, что она может проникать через препятствия, такие как кость. К тому же процедура магнитной стимуляции действует одновременно более эффективно на нервные стволы и нервные окончания, кровеносные сосуды и мышцы в области воздействия, что в физиотерапии редко и можно определить как 3 в 1.
Как действует магнитная стимуляция?
Магнитная стимуляция способствует восстановлению нервных связей головного мозга с телом, «пробуждает» неактивные участки коры головного мозга, активирует скрытые ресурсы мозга и периферической нервной системы.
После стимуляции можно заметить увеличение силы мышц конечностей при параличах и парезах, уменьшение спастичности, улучшение трофики, чувствительности, памяти, внимания, уменьшение боли. Эффект обычно виден и ощутим сразу после первой же процедуры.
Как выполняется стимуляция?
Это безболезненная и легко переносимая процедура, хотя в процессе стимуляции и возможны некоторые своеобразные ощущения. К поверхности тела (это может быть голова или другая поверхность) прикладывается электромагнитная катушка (койл), подключенный к основному блоку магнитного стимулятора. Койл в течение 15-30 минут генерирует электромагнитные импульсы, ощущаемые в виде «пробегания тока».
Магнитная стимуляция
Мы используем 2 типа процедур:
1. рТМС — транскраниальная магнитная стимуляция:
Стимуляция головного мозга. Используется в восстановительном периоде заболеваний, травм и хирургического лечения головного и спинного мозга, последствиях ишемического инсульта. Показания: спастичность, нарушение равновесия, нарушения речи (афазия, дизартрия), расстройство памяти, депрессия, головная боль, неврастения, фобические состояния.
2. рПМС — Периферическая магнитная стимуляция:
Заболевания периферической нервной системы очень распространены, достаточно мучительны для больных и плохо поддаются лечению, что приводит к длительной нетрудоспособности и высокому проценту инвалидизации.
В нашей клинике широко и эффективно применяется лечение ритмической магнитной стимуляцией таких заболеваний, как остеохондроз с болевым синдромом, грыжи межпозвоночных дисков, состояние после операций на позвоночнике и травм, нейропатии (в том числе диабетические), посттравматические, ревматоидные, послеоперационные; невропатии лицевого и тройничного нервов, невропатии плечевого сплетения, локтевого, лучевого, срединного нервов, малоберцового, большеберцового, седалищного нервов, а также плечелопаточный болевой синдром и заболевания суставов.
Магнитная стимуляция способствует восстановлению иннервации тканей, улучшению кровотока, устраняет межтканевые отеки (что зачастую является причиной сдавления нервов), которые ведут к нарушению чувствительности, онемению и болевому синдрому; восстанавливает посттравматическую и послеоперационную иннервацию.
После ритмической магнитной стимуляции восстанавливается сила мышц конечностей при параличах и парезах, уменьшается спастика, улучшается трофика, чувствительность, и достаточно быстро уходит болевой синдром. По нашим наблюдениям, при регулярном выполнении курсов магнитной стимуляции (3-4 раза в год) грыжи межпозвоночных дисков нередко исчезают и отпадает необходимость в оперативном вмешательстве.
а) Стимуляция периферических нервов и сплетений.
Показания: боль, расстройство чувствительности, периферический парез или паралич. Обычно нам приходится иметь дело с невропатией плечевого сплетения и нервов: локтевого, лучевого, срединного, малоберцового, большеберцового, седалищного, остеохондрозом, плече-лопаточным периартритом.
б) Стимуляция тройничного и лицевого нервов при их заболеваниях и повреждениях приводит к более быстрому и более полному восстановлению мимики и чувствительности лица, уменьшению боли.
Эффективность лечения обострений заболеваний нервной системы при совмещении традиционной терапии с курсом магнитной стимуляции значительно выше, чем при изолированном применении стандартной медикаментозной терапии.
Какие имеются противопоказания для проведения процедур?
Противопоказаниями к применению методики являются:
1. Эпилепсия и эпилептические приступы в анамнезе;
2. Онкологические заболевания мозга, перенесенные нейрохирургические операции на головном мозге,;
3. Наличие искусственного водителя ритма сердца — кардиостимулятора;
4. Тяжелые нарушения ритма сердца;
5. Инсулиновая помпа;
6. Беременность;
7. Наличие вживленных имплантов и металлоконструкций из магнитных материалов в зоне предполагаемой стимуляции. Зубные металлопротезы допустимы.
Сколько необходимо процедур для лечения и куда обратиться для записи?
Курс лечения — 10 — 15 процедур. Эффект от лечения продолжительный и зависит от соблюдения пациентом рекомендаций врача. Выраженное обезболивающее действие обычно проявляется уже после первой процедуры.
При первичном посещении клиники желательно иметь на руках результаты обследования. Если исследования выполнены не были и Вы не посещали невролога, возможно пройти осмотр в нашей клинике, что позволит избежать лишних исследований и сэкономить средства.
Будем рады помочь Вам!
Записаться на прием можно по телефону +7(423) 245-62-28
ИНСТИТУТ ВЕРТЕБРОНЕВРОЛОГИИ И МАНУЛЬНОЙ МЕДИЦИНЫ
г. Владивосток, ул. Амурская, 84
Неинвазивная стимуляция мозга в реабилитации пациентов с постинсультной афазией
Афазии разной степени выраженности являются одним из наиболее частых осложнений инсульта. Они развиваются у 25—38% больных и требуют длительной реабилитации [1—3]. Учитывая ежегодное развитие в нашей стране около 500 тыс. инсультов, ожидаемая частота афазий составляет не менее 100—120 тыс. случаев в год. Утрата способности говорить и понимать обращенную речь, невозможность письма, чтения и счета приводят к затруднению контакта пациента с окружающими его людьми, осложняют личную, семейную и социальную жизнь в целом. По данным последних исследований, тяжелые формы афазии ухудшают качество жизни и приводят к развитию депрессии чаще, чем при болезни Альцгеймера или онкологических заболеваниях [4].
Реабилитация речевых нарушений является одним из наименее изученных направлений восстановительной неврологии. В то время как для восстановления движений ежегодно предлагаются новейшие механизированные системы, основанные на роботизированных технологиях, в области речевой реабилитации логопедические занятия остаются практически единственным инструментом помощи больным. Появление неинвазивных методов реабилитации, таких как транскраниальная магнитная стимуляция (ТМС, англ. TMS — Transcranial Magnetic Stimulation) и транскраниальная стимуляция постоянным током (ТЭС, англ. tDCS — transcranial Direct Current Stimulation) стало многообещающим в отношении модификации нейропластических процессов и повышения эффективности классических логопедических подходов. Уточнение оптимальных параметров интенсивности и длительности стимуляции, их клиническая апробация — необходимые требования для внедрения стимуляционных методов в программы лечения пациентов с афазией.
В то время как для восстановления движений ежегодно предлагаются новейшие механизированные системы, основанные на роботизированных технологиях, в области речевой реабилитации логопедические занятия остаются практически единственным инструментом помощи больным. Появление неинвазивных методов реабилитации, таких как транскраниальная магнитная стимуляция (ТМС, англ. TMS — Transcranial Magnetic Stimulation) и транскраниальная стимуляция постоянным током (ТЭС, англ. tDCS — transcranial Direct Current Stimulation) стало многообещающим в отношении модификации нейропластических процессов и повышения эффективности классических логопедических подходов. Уточнение оптимальных параметров интенсивности и длительности стимуляции, их клиническая апробация — необходимые требования для внедрения стимуляционных методов в программы лечения пациентов с афазией.
Методы неинвазивной стимуляции мозга
Метод ритмической ТМС (рТМС) в последние годы достаточно хорошо зарекомендовал себя как эффективный инструмент в лечении постинсультной спастичности, когнитивных и речевых нарушений. Под воздействием магнитного поля возникает деполяризация мембраны нервных клеток коры головного мозга с формированием потенциала действия и дальнейшим антеградным распространением возбуждения. Меняя параметры рТМС, можно оказывать локальное стимулирующее или ингибирующее влияние на отдельные участки коры, изменяя, таким образом, их функциональную активность и взаимодействие с другими структурами головного мозга [5].
Под воздействием магнитного поля возникает деполяризация мембраны нервных клеток коры головного мозга с формированием потенциала действия и дальнейшим антеградным распространением возбуждения. Меняя параметры рТМС, можно оказывать локальное стимулирующее или ингибирующее влияние на отдельные участки коры, изменяя, таким образом, их функциональную активность и взаимодействие с другими структурами головного мозга [5].
В первых исследованиях М. Naeser и соавт. [6] с использованием рТМС выявили значительное улучшение речевых возможностей пациентов с хронической афазией под влиянием ингибиторной стимуляции частотой 1 Гц на гомолог зоны Брока в правом полушарии, что в дальнейшем было подтверждено во многих рандомизированных клинических испытаниях. В настоящее время методика pТМС применяется в крупных неврологических и реабилитационных клиниках. Однако высокая стоимость оборудования и его обслуживания, вероятность развития эпилептических приступов [7, 8] обосновывают поиск более доступных и безопасных методов нейромодуляции.
В начале 2000-х годов параллельно с изучением воздействия магнитного поля были возобновлены исследования по влиянию низкочастотного постоянного тока на нейропластичность у пациентов, перенесших инсульт [9]. Методика нейрональной стимуляции постоянным током малой мощности (до 1 мА) известна в нашей стране как транскраниальная микрополяризация (ТЭС-терапия). В конце 1970-х годов ее разработкой занимались сотрудники Физиологического отдела им. И.П. Павлова НИИ экспериментальной медицины АМН СССР (Ленинград) под руководством проф. Г.А. Вартаняна [10—12]. В ходе проведения экспериментальных работ по изучению механизмов памяти было отмечено положительное влияние малым постоянным током на различные структуры головного мозга. Установлено, что при микрополяризации происходят изменения возбудимости и импульсной активности нервных клеток не только под электродами, но и в дистанционно расположенных структурах. Результаты исследований показали связь активации структур со сдвигами мембранного потенциала клеток и распространением возбуждения по кортикофугальным и транссинаптическим связям [13]. Возбуждению нейронов предшествовали биохимические процессы с ультраструктурной перестройкой синаптических мембран. Благодаря полученным результатам были заложены теоретические основы синаптогенеза как ключевого механизма нейропластичности и обосновано использование ТЭС-терапии в нейрореабилитации.
Возбуждению нейронов предшествовали биохимические процессы с ультраструктурной перестройкой синаптических мембран. Благодаря полученным результатам были заложены теоретические основы синаптогенеза как ключевого механизма нейропластичности и обосновано использование ТЭС-терапии в нейрореабилитации.
Синаптогенез и механизмы его индукции слабыми токами
Синаптогенез — один из механизмов нейропластичности, лежащий в основе обучения, формирования памяти, восстановления утраченных функций [14]. Создание новых синаптических контактов между клетками, а в дальнейшем сетей взаимодействующих между собой групп нейронов является неотъемлемым процессом при запоминании и хранении информации, овладевании навыками. Индукция синаптогенеза посредством усиления эффективности существующих межклеточных контактов и возникновения новых связано прежде всего с глутаматными NMDA-рецепторами, а также изменением состояния потенциал-зависимых кальциевых каналов [9, 15, 16], что обеспечивает развитие феноменов долговременной потенциации и долговременной депрессии [17].
В соответствии с результатами экспериментальных исследований слабый постоянный электрический ток является адекватным и физиологичным способом стимуляции синаптогенеза [18, 19]. При ТЭС-терапии посредством 2 электродов (анода и катода), расположенных в проекции значимых для восстановления функциональных зон, наблюдается транскраниальное воздействие на кору головного мозга, результатом которого становится изменение уровня потенциала покоя мембраны и возбудимости нейронов [20]. Анодная ТЭС вызывает долгосрочное потенцирование путем модуляции ГАМКергических и глутаматергических синапсов [21, 22], тогда как катодная ТЭС — длительное ингибирование путем снижения глутаматергической активности [23].
Среди механизмов индуцированного ТЭС синаптогенеза рассматривается влияние постоянного тока на астроциты. Данный тип глии обеспечивает многофункциональную связь между нейронами и эндотелием, являясь важным элементом основной структурно-функциональной единицы мозга — нейроваскулярной единицы [24—27]. Установлено, что при глутаматной или АТФазной нейрональной активации в астроцитах повышается концентрация Ca2+, что приводит к выработке вазоактивных веществ — простагландинов, оксида азота (NO) [28] и других, вазодилатации и увеличению регионарного кровотока [29, 30] в условиях возрастающей синаптической активности [24]. Вышеописанный принцип нейроваскулярного взаимодействия составляет основу метода функционального картирования головного мозга с помощью МРТ (фМРТ), который хорошо зарекомендовал себя в фундаментальных и клинических нейронауках для изучения процессов организации и перестройки функциональных систем мозга, в том числе речевой, в физиологических и патологических условиях [31, 32].
Установлено, что при глутаматной или АТФазной нейрональной активации в астроцитах повышается концентрация Ca2+, что приводит к выработке вазоактивных веществ — простагландинов, оксида азота (NO) [28] и других, вазодилатации и увеличению регионарного кровотока [29, 30] в условиях возрастающей синаптической активности [24]. Вышеописанный принцип нейроваскулярного взаимодействия составляет основу метода функционального картирования головного мозга с помощью МРТ (фМРТ), который хорошо зарекомендовал себя в фундаментальных и клинических нейронауках для изучения процессов организации и перестройки функциональных систем мозга, в том числе речевой, в физиологических и патологических условиях [31, 32].
Роль фМРТ
На основании проведенных в течение последних лет фМРТ-исследований установлено, что реорганизация речевой системы после перенесенного ишемического инсульта осуществляется за счет вовлечения прилежащих к зоне инфаркта мозга областей доминантного по речи полушария [33—35], а также компенсаторной активации гомологов основных речевых зон субдоминантного полушария [36—38]. На интенсивность и очередность нейропластических процессов в головном мозге, равно как и на степень восстановления речи, оказывают влияние расположение и распространенность инфаркта мозга [39, 40]. У пациентов с небольшими очагами чаще наблюдается активация периинфарктных речевых зон, при обширных инфарктах переключение идет главным образом на гомологичные области в правом полушарии [40—42]. Значение структур правого полушария в восстановлении речи остается неоднозначным. Согласно существующим представлениям, активация правосторонних гомологов может играть положительную роль в восстановлении речи, носить компенсаторный характер [38, 43] или быть неэффективной из-за сдерживающего влияния на реализацию процессов нейропластичности левополушарной сети [44]. Высказывается мнение, что вследствие уменьшения ингибирующего транскаллозального воздействия со стороны пораженного полушария происходит избыточная активация в гомологичных зонах правого полушария. Ее негативным эффектом является тормозящее влияние на околоочаговые области в левом полушарии и соответственно темпы и объем восстановления функции [42, 45—49].
На интенсивность и очередность нейропластических процессов в головном мозге, равно как и на степень восстановления речи, оказывают влияние расположение и распространенность инфаркта мозга [39, 40]. У пациентов с небольшими очагами чаще наблюдается активация периинфарктных речевых зон, при обширных инфарктах переключение идет главным образом на гомологичные области в правом полушарии [40—42]. Значение структур правого полушария в восстановлении речи остается неоднозначным. Согласно существующим представлениям, активация правосторонних гомологов может играть положительную роль в восстановлении речи, носить компенсаторный характер [38, 43] или быть неэффективной из-за сдерживающего влияния на реализацию процессов нейропластичности левополушарной сети [44]. Высказывается мнение, что вследствие уменьшения ингибирующего транскаллозального воздействия со стороны пораженного полушария происходит избыточная активация в гомологичных зонах правого полушария. Ее негативным эффектом является тормозящее влияние на околоочаговые области в левом полушарии и соответственно темпы и объем восстановления функции [42, 45—49].
Представленные механизмы межполушарного взаимодействия, уточненные с помощью функциональной МРТ, явились обоснованием возможности модуляции нейропластических процессов с помощью технологий неинвазивной стимуляции мозга, в частности электростимуляции постоянным током.
ТЭС-терапия
Несмотря на многочисленные исследования с применением ТЭС-терапии в процессе реабилитации постинсультных речевых нарушений [50], универсальный протокол стимуляции до сих пор не разработан. Остаются открытыми вопросы выбора оптимальной зоны, сроков, интенсивности и длительности электрического воздействия.
Протокол стимуляции. В отличие от ТМС во время терапии постоянным током возможно применение стимулирующих протоколов в проекции основных речевых зон. Это доступно из-за использования тока низкой интенсивности (до 2 мА), что уменьшает вероятность появления эпилептиформной активности и развития судорожных приступов. Метаанализы последних лет, суммирующие результаты 19 исследований восстановления речи с помощью ТЭС, показали, что в зависимости от ведущего речевого дефекта (моторного или сенсорного) предпочтение отдается анодной стимуляции в проекции основных речевых зон Брока или Вернике соответственно [51—55]. Воздействие на периинфарктные зоны — височно-теменную [55], дорсолатеральную префронтальную кору [56], способствует улучшению понимания и беглости речи. Использование анодной стимуляции правой половины мозжечка ассоциировано с улучшением написания слов [57], тогда как катодное ингибирование той же зоны — с улучшением генерации глаголов [58].
Воздействие на периинфарктные зоны — височно-теменную [55], дорсолатеральную префронтальную кору [56], способствует улучшению понимания и беглости речи. Использование анодной стимуляции правой половины мозжечка ассоциировано с улучшением написания слов [57], тогда как катодное ингибирование той же зоны — с улучшением генерации глаголов [58].
Зоны стимуляции. Выбор зон стимуляции может осуществляться с опорой на: 1) данные фМРТ с использованием речевой парадигмы для выявления паттерна реорганизации речевой системы и зоны предполагаемого воздействия [59]; 2) локализацию моторных артикуляционных и речевых зон, найденных с помощью навигационной ТМС [49]. Однако большинство исследователей используют в качестве ориентира для расположения анода международную систему монтажа электродов при ЭЭГ — 10—20 (например, зоне Брока соответствует точка F5, зоне Вернике — CP5), при этом возвратный/референсный электрод в большинстве протоколов устанавливается на контралатеральную орбито-фронтальную область.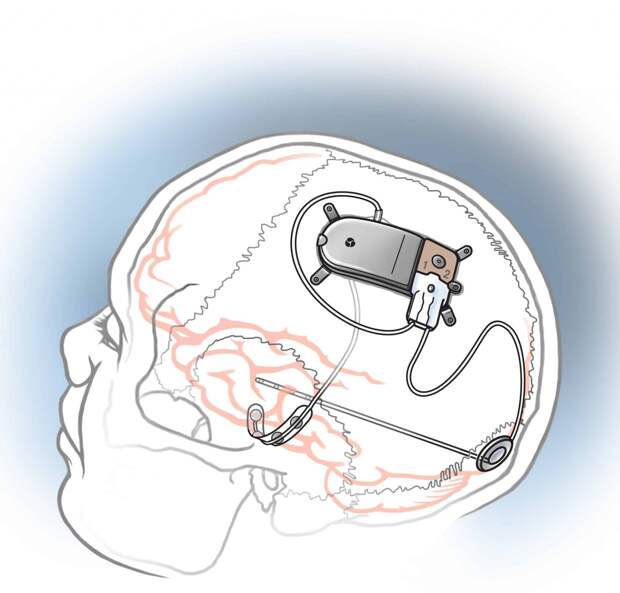 В случае двусторонней стимуляции анод и катод устанавливают в проекции речевых зон и их гомологов [60].
В случае двусторонней стимуляции анод и катод устанавливают в проекции речевых зон и их гомологов [60].
Параметры стимуляции. Рекомендованная длительность одного сеанса стимуляции составляет от 10 до 30 мин, в среднем 20 мин. Эффективная интенсивность постоянного тока может варьировать от 1 до 2 мА, ее подбирают индивидуально, ориентируясь на ощущения пациента. В течение курса параметры могут постепенно увеличиваться при каждой последующей процедуре. Воздействие интенсивностью 1—1,5 мА практически не ощутимо пациентом. В диапазоне тока от 1,5 до 2 мА возможно некоторое покалывание или жжение под электродом.
Многие исследователи указывают на дозозависимый эффект транскраниальной стимуляции. Рекомендуется проведение ежедневных сеансов на протяжении не менее 10—15 дней [61]. Наиболее эффективна комбинация ТЭС-терапии с логопедическими занятиями, направленными на восстановление ведущего речевого дефекта во время или сразу после сеанса [5].
Сроки проведения стимуляции
В большинстве исследований эксперты рекомендуют использовать методику стимуляции постоянным током в сроки от 3 до 12 мес после перенесенного инсульта [62]. При применении ТЭС-терапии у пациентов в острой или подострой стадии инсульта не выявлено достоверного улучшения речевой функции по сравнению с пациентами, которым стимуляция была начата в более поздние сроки [63]. Высказано предположение, что в раннем постинфарктном периоде анодная стимуляция является дополнительным стрессом, оказывающим отрицательное влияние на репаративные процессы и механизмы нейропластичности, снижающим позитивный эффект стимуляции [64]. Результаты недавнего исследования K. Spielmann и соавт. [62], основанные на проведении анодной стимуляции левой нижней лобной извилины у пациентов в период от 3 нед до 3 мес после ишемического инсульта с оценкой эффективности восстановления речи по Бостонскому тесту, показали отсутствие улучшения речи по сравнению с группой плацебо, что согласуется с полученными ранее данными [64]. В то же время D. You и соавт. [65] установлено, что катодное ингибирование гомолога зоны Вернике в период 16—38 дней после острого нарушения мозгового кровообращения влияет на улучшение понимания речи.
При применении ТЭС-терапии у пациентов в острой или подострой стадии инсульта не выявлено достоверного улучшения речевой функции по сравнению с пациентами, которым стимуляция была начата в более поздние сроки [63]. Высказано предположение, что в раннем постинфарктном периоде анодная стимуляция является дополнительным стрессом, оказывающим отрицательное влияние на репаративные процессы и механизмы нейропластичности, снижающим позитивный эффект стимуляции [64]. Результаты недавнего исследования K. Spielmann и соавт. [62], основанные на проведении анодной стимуляции левой нижней лобной извилины у пациентов в период от 3 нед до 3 мес после ишемического инсульта с оценкой эффективности восстановления речи по Бостонскому тесту, показали отсутствие улучшения речи по сравнению с группой плацебо, что согласуется с полученными ранее данными [64]. В то же время D. You и соавт. [65] установлено, что катодное ингибирование гомолога зоны Вернике в период 16—38 дней после острого нарушения мозгового кровообращения влияет на улучшение понимания речи.
Оценка результатов
Учитывая отсутствие общепринятых стандартов проведения ТЭС, особое значение при оценке ее эффективности приобретает стандартизированная оценка речевого статуса до и после проведения лечебных процедур. За рубежом, кроме ранее упоминаемого Бостонского теста, используются шкалы речевых нарушений Boston Diagnostic Aphasia Examination (BDAE), Aachen Aphasia Test (AAT), Western Aphasia Battery (WAB) или диагностические задания, например называние картинок [50]. В России общепризнанной среди логопедов и неврологов является методика А.Р. Лурия в модификации Л.С. Цветковой [66], которая позволяет провести качественную и количественную оценку основных параметров речевой функции.
Заключение
Проведенные исследования показали возможность включения методов неинвазивной стимуляции мозга в программу реабилитации больных с постинсультной афазией. Обоснованием для их использования являются данные о влиянии неинвазивной стимуляции мозга на синаптогенез и нейрональную сетевую перестройку. Использование ТЭС, вероятно, более перспективно для клинической практики из-за доступности и безопасности метода. Однако необходимы рандомизированные контролируемые исследования для уточнения оптимальных параметров стимуляции со стандартизированной оценкой эффективности проводимого лечения и использования метода в качестве адьювантного с целью повышения эффективности занятий с афазиологом. Представляется целесообразным использование фМРТ с релевантными тестами на разные виды афазий для определения прогностических нейрональных коррелятов эффективности нейромодуляции и выбора зон стимуляции мозга.
Использование ТЭС, вероятно, более перспективно для клинической практики из-за доступности и безопасности метода. Однако необходимы рандомизированные контролируемые исследования для уточнения оптимальных параметров стимуляции со стандартизированной оценкой эффективности проводимого лечения и использования метода в качестве адьювантного с целью повышения эффективности занятий с афазиологом. Представляется целесообразным использование фМРТ с релевантными тестами на разные виды афазий для определения прогностических нейрональных коррелятов эффективности нейромодуляции и выбора зон стимуляции мозга.
Авторы заявляют об отсутствии конфликта интересов.
The authors declare no conflicts of interest.
Сведения об авторах
Белопасова А.В. — https://orcid.org/0000-0003-3124-2443; e-mail: [email protected]
Добрынина Л.А. — https://orcid.org/ 0000-0003-3124-2443; e-mail: [email protected]
Кадыков А. С. — https://orcid.org/ 0000-0001-7491-7215; e-mail: [email protected]
С. — https://orcid.org/ 0000-0001-7491-7215; e-mail: [email protected]
Бердникович Е.С. — https://orcid.org/ 0000-0002-7608-2255; e-mail:[email protected].
Бергельсон Т.М. — https://orcid.org/0000-0002-6085-2964; e-mail: [email protected]
Цыпуштанова М.М. — https://orcid.org/0000-0002-4231-3895; e-mail: [email protected]
Автор, ответственный за переписку: Белопасова Анастасия Владимировна — e-mail: [email protected]
NIMH » Мозговая стимуляция
Обзор
Терапия стимуляции мозга может играть определенную роль в лечении некоторых психических расстройств. Терапия стимуляции мозга включает в себя активацию или торможение мозга непосредственно с помощью электричества. Электричество может подаваться непосредственно через электроды, имплантированные в мозг, или неинвазивно через электроды, размещенные на коже головы. Электричество также можно индуцировать с помощью магнитных полей, воздействующих на голову. Хотя эти виды терапии используются реже, чем лекарства и психотерапия, они обещают лечение определенных психических расстройств, которые не поддаются другим методам лечения.
Хотя эти виды терапии используются реже, чем лекарства и психотерапия, они обещают лечение определенных психических расстройств, которые не поддаются другим методам лечения.
Электросудорожная терапия является наиболее изученной терапией стимуляции мозга и имеет самую долгую историю использования. Другие методы стимуляции, обсуждаемые здесь, являются более новыми, а в некоторых случаях все еще экспериментальными методами. К ним относятся:
- стимуляция блуждающего нерва (ВНС)
- повторная транскраниальная магнитная стимуляция (рТМС)
- магнитно-судорожная терапия (МСТ)
- глубокая стимуляция мозга (DBS)
План лечения может также включать медикаментозное лечение и психотерапию . Выбор правильного плана лечения должен основываться на индивидуальных потребностях человека и медицинской ситуации, а также под наблюдением врача.
Электросудорожная терапия
Электросудорожная терапия (ЭСТ) использует электрический ток для лечения серьезных психических расстройств. Этот тип терапии обычно рассматривается только в том случае, если состояние пациента не улучшилось после применения других методов лечения (таких как прием антидепрессантов или психотерапия) или в случаях, когда требуется быстрый ответ (например, в случае суицидального риска и кататонии). ).
Этот тип терапии обычно рассматривается только в том случае, если состояние пациента не улучшилось после применения других методов лечения (таких как прием антидепрессантов или психотерапия) или в случаях, когда требуется быстрый ответ (например, в случае суицидального риска и кататонии). ).
ЭШТ: зачем это делается
ЭСТ чаще всего используется для лечения тяжелой, резистентной к лечению депрессии, но она также может быть показана с медицинской точки зрения при других психических расстройствах, таких как биполярное расстройство или шизофрения. Его также можно использовать при опасных для жизни обстоятельствах, например, когда пациент не может двигаться или реагировать на внешний мир (например, кататония), склонен к суициду или недоедает в результате тяжелой депрессии.
ЭСТ может эффективно снижать вероятность рецидива, когда пациенты проходят последующее лечение. Два основных преимущества ЭСТ перед лекарствами заключаются в том, что ЭСТ начинает действовать быстрее, часто начиная с первой недели, и пожилые люди реагируют особенно быстро.
ЭСТ: как это работает
Перед проведением ЭСТ человеку вводят успокоительное с помощью общей анестезии и дают лекарство, называемое миорелаксантом, для предотвращения движения во время процедуры. Анестезиолог контролирует дыхание, частоту сердечных сокращений и артериальное давление в течение всей процедуры, которую проводит обученная медицинская бригада, включая врачей и медсестер. Во время процедуры:
- Электроды размещаются в определенных местах на голове.
- Через электроды через мозг проходит электрический ток, вызывая припадок, который обычно длится менее одной минуты. Поскольку пациент находится под наркозом и принял миорелаксант, это не болезненно, и пациент не может чувствовать электрические импульсы.
- Через пять-десять минут после окончания процедуры пациент просыпается. Сначала он или она может чувствовать себя вялым, когда действие анестезии проходит. Но примерно через час пациент обычно приходит в себя и может возобновить нормальную деятельность.

Типичный курс ЭСТ проводится примерно три раза в неделю, пока депрессия пациента не улучшится (обычно от 6 до 12 процедур). После этого иногда требуется поддерживающая ЭСТ, чтобы снизить вероятность возвращения симптомов. Поддерживающее лечение ЭСТ варьируется в зависимости от потребностей человека и может варьироваться от одного сеанса в неделю до одного сеанса каждые несколько месяцев. Часто человек, который подвергается ЭСТ, также принимает антидепрессанты или лекарства, стабилизирующие настроение.
Побочные эффекты ЭСТ
Наиболее распространенные побочные эффекты, связанные с ЭСТ, включают:
- головную боль
- расстройство желудка
- мышечные боли
- потеря памяти
У некоторых людей могут возникать проблемы с памятью, особенно во время лечения. Иногда проблемы с памятью более серьезные, но обычно они улучшаются в течение нескольких дней и недель после окончания курса ЭСТ.
Исследования показали, что проблемы с памятью, по-видимому, в большей степени связаны с традиционным типом ЭСТ, называемым двусторонним ЭСТ, при котором электроды располагаются с обеих сторон головы.
При односторонней ЭСТ электроды размещают только на одной стороне головы — обычно на правой стороне, поскольку она находится напротив областей обучения и памяти. Было обнаружено, что односторонняя ЭСТ с меньшей вероятностью вызывает проблемы с памятью, и поэтому многие врачи, пациенты и семьи предпочитают ее.
Стимуляция блуждающего нерва
Стимуляция блуждающего нерва (ВНС) работает с помощью устройства, имплантированного под кожу, которое посылает электрические импульсы через левый блуждающий нерв, половину заметной пары нервов, идущих от ствола мозга через шею и вниз к каждой стороне грудной клетки и живота. . Блуждающие нервы передают сообщения от мозга к основным органам тела (например, к сердцу, легким и кишечнику) и к областям мозга, которые контролируют настроение, сон и другие функции.
ВНС: Почему это делается
ВНС изначально разрабатывался для лечения эпилепсии. Однако ученые заметили, что он также благоприятно влияет на настроение, особенно на депрессивные симптомы. Используя сканирование мозга, ученые обнаружили, что устройство воздействовало на участки мозга, участвующие в регуляции настроения. Импульсы, по-видимому, изменяют уровни определенных нейротрансмиттеров (химических веществ мозга), связанных с настроением, включая серотонин, норадреналин, ГАМК и глутамат.
Используя сканирование мозга, ученые обнаружили, что устройство воздействовало на участки мозга, участвующие в регуляции настроения. Импульсы, по-видимому, изменяют уровни определенных нейротрансмиттеров (химических веществ мозга), связанных с настроением, включая серотонин, норадреналин, ГАМК и глутамат.
В 2005 г. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) одобрило использование ВНС для лечения резистентной к терапии депрессии при определенных обстоятельствах:
- Если пациенту 18 лет и старше; и
- Если болезнь длится два года и более; и
- , если заболевание тяжелое или рецидивирующее; и
- , если депрессия не уменьшилась после применения не менее четырех других методов лечения
По данным FDA, он не предназначен для лечения первой линии даже у пациентов с тяжелой депрессией. И, несмотря на одобрение FDA, VNS остается редко используемым, потому что результаты ранних исследований, проверяющих его эффективность при большой депрессии, были неоднозначными. Но более новое исследование, в котором были объединены результаты только контролируемых клинических испытаний, показало, что 32% людей с депрессией реагировали на VSN, а у 14% наблюдалась полная ремиссия симптомов после лечения в течение почти 2 лет.
Но более новое исследование, в котором были объединены результаты только контролируемых клинических испытаний, показало, что 32% людей с депрессией реагировали на VSN, а у 14% наблюдалась полная ремиссия симптомов после лечения в течение почти 2 лет.
VNS: Как это работает
Устройство, называемое генератором импульсов, размером примерно с секундомер, имплантировано хирургическим путем в верхнюю левую часть грудной клетки. К генератору импульсов подсоединен электрический провод, который идет от генератора к левому блуждающему нерву.
Обычно 30-секундные электрические импульсы посылаются примерно каждые пять минут от генератора к блуждающему нерву. Длительность и частота импульсов могут варьироваться в зависимости от того, как запрограммирован генератор. Блуждающий нерв, в свою очередь, доставляет эти сигналы в мозг. Генератор импульсов, работающий непрерывно, питается от батареи, срок службы которой составляет около 10 лет, после чего ее необходимо заменить. В норме люди не чувствуют боли или каких-либо других ощущений во время работы устройства.
Устройство также можно временно отключить, поместив магнит на грудную клетку, где имплантирован генератор импульсов. Человек может захотеть деактивировать его, если побочные эффекты становятся невыносимыми, или перед тем, как приступить к напряженной деятельности или упражнениям, потому что это может мешать дыханию. Устройство снова активируется, когда магнит удаляется.
Обратите внимание: VNS должен назначаться и контролироваться только врачами, имеющими специальную подготовку и опыт в лечении резистентной депрессии и использовании этого устройства.
Лечение ВНС предназначено для уменьшения симптомов депрессии. Может пройти несколько месяцев, прежде чем пациент заметит какие-либо преимущества, и не все пациенты реагируют на VNS. Важно помнить, что VNS предназначен для применения вместе с другими традиционными методами лечения, такими как лекарства, и пациенты не должны ожидать прекращения этих других методов лечения, даже если устройство находится на месте.
ВНС: побочные эффекты
ВНС не без риска. Могут быть осложнения, такие как инфекция после операции по имплантации, или устройство может расшататься, сместиться или выйти из строя, что может потребовать дополнительной операции для исправления. У некоторых пациентов симптомы не улучшаются, а некоторые даже ухудшаются.
Другие возможные побочные эффекты включают:
- Изменение голоса или охриплость
- Кашель или боль в горле
- Боль в шее
- Дискомфорт или покалывание в области имплантации устройства
- Проблемы с дыханием, особенно во время физической нагрузки
- Затрудненное глотание
Долгосрочные побочные эффекты неизвестны.
Повторяющаяся транскраниальная магнитная стимуляция
Повторяющаяся транскраниальная магнитная стимуляция (rTMS) использует магнит для активации мозга. Впервые разработан в 1985, рТМС изучалась как средство для лечения депрессии, психоза, тревоги и других расстройств.
В отличие от ЭСТ, при которой электрическая стимуляция носит более общий характер, рТМС может быть нацелена на конкретный участок мозга. Ученые считают, что сосредоточение внимания на определенном участке мозга снижает вероятность побочных эффектов, связанных с ЭСТ. Но мнения о том, какой сайт лучше, расходятся.
rTMS: Почему это делается
В 2008 году rTMS была одобрена FDA для лечения большой депрессии у пациентов, которые не реагируют на хотя бы один антидепрессант в текущем эпизоде. Он также используется в других странах для лечения депрессии у пациентов, которые не реагировали на лекарства и которые в противном случае могли бы быть рассмотрены для ЭСТ.
Доказательства, поддерживающие рТМС при депрессии, были неоднозначными до тех пор, пока в 2010 году не было опубликовано первое крупное клиническое исследование, финансируемое NIMH. Исследование показало, что 14% пациентов достигли ремиссии с помощью рТМС по сравнению с 5% при неактивном (фиктивном) лечении. После окончания испытания пациенты могли перейти ко второй фазе, на которой всем, включая тех, кто ранее получал фиктивное лечение, давали рТМС. Показатели ремиссии во время второй фазы поднялись почти до 30%. Имитация лечения похожа на плацебо, но это не неактивная таблетка, а неактивная процедура, имитирующая настоящую рТМС.
После окончания испытания пациенты могли перейти ко второй фазе, на которой всем, включая тех, кто ранее получал фиктивное лечение, давали рТМС. Показатели ремиссии во время второй фазы поднялись почти до 30%. Имитация лечения похожа на плацебо, но это не неактивная таблетка, а неактивная процедура, имитирующая настоящую рТМС.
rTMS: как это работает
Типичный сеанс rTMS длится от 30 до 60 минут и не требует анестезии.
Во время процедуры:
- Электромагнитная катушка прикладывается ко лбу рядом с областью мозга, которая, как считается, участвует в регуляции настроения.
- Затем через катушку подаются короткие электромагнитные импульсы. Магнитные импульсы легко проходят через череп и вызывают небольшие электрические токи, которые стимулируют нервные клетки в целевой области мозга.
Поскольку этот тип импульса обычно не проникает в мозг дальше, чем на два дюйма, ученые могут выбирать, какие части мозга будут затронуты, а какие нет. Сила магнитного поля примерно такая же, как у магнитно-резонансной томографии (МРТ). Как правило, человек чувствует легкий стук или постукивание по голове при подаче импульсов.
Сила магнитного поля примерно такая же, как у магнитно-резонансной томографии (МРТ). Как правило, человек чувствует легкий стук или постукивание по голове при подаче импульсов.
Не все ученые согласны с тем, как лучше расположить магнит на голове пациента или подавать электромагнитные импульсы. Они также еще не знают, работает ли рТМС лучше всего, когда применяется отдельно или в сочетании с лекарствами и/или психотерапией. В настоящее время проводятся дополнительные исследования, чтобы определить наиболее безопасные и эффективные способы использования rTMS.
rTMS: побочные эффекты
Иногда человек может чувствовать дискомфорт в месте на голове, где находится магнит. Мышцы скальпа, челюсти или лица могут сокращаться или ощущаться покалывание во время процедуры. Могут возникнуть легкие головные боли или кратковременное головокружение. Также возможно, что процедура может вызвать припадок, хотя задокументированные случаи этого нечасты. Два крупномасштабных исследования безопасности рТМС показали, что большинство побочных эффектов, таких как головные боли или дискомфорт кожи головы, были легкими или умеренными, а судорог не было. Поскольку лечение является относительно новым, долгосрочные побочные эффекты неизвестны.
Поскольку лечение является относительно новым, долгосрочные побочные эффекты неизвестны.
Магнитная судорожная терапия
МСТ: как это работает
Магнитно-судорожная терапия (МСТ) заимствует некоторые аспекты как из ЭСТ, так и из рТМС. Как и rTMS, MST использует магнитные импульсы вместо электричества, чтобы стимулировать точную цель в мозгу. Однако, в отличие от рТМС, МСТ направлена на то, чтобы вызвать припадок, как и ЭСТ. Таким образом, импульсы подаются с более высокой частотой, чем та, которая используется в rTMS. Поэтому, как и при ЭСТ, пациент должен быть анестезирован и ему должны дать миорелаксант, чтобы предотвратить движение. Цель MST — сохранить эффективность ЭСТ при одновременном снижении ее когнитивных побочных эффектов.
MST находится на ранних стадиях тестирования на психические расстройства, но первые результаты обнадеживают. В недавней обзорной статье, в которой изучались данные восьми клинических исследований, было обнаружено, что МСТ вызывает ремиссию большой депрессии или биполярного расстройства у 30-40% людей.
МСТ: побочные эффекты
Как и ЭСТ, МСТ сопряжена с риском побочных эффектов, которые могут быть вызваны воздействием анестезии и индуцированием припадка. Исследования как на животных, так и на людях показали, что MST производит
- меньше побочных эффектов памяти
- более короткие припадки
- обеспечивает более короткое время восстановления, чем ECT
Глубокая стимуляция мозга
Глубокая стимуляция мозга (DBS) была впервые разработана для лечения болезни Паркинсона для уменьшения тремора, скованности, проблем с ходьбой и неконтролируемых движений. В DBS пара электродов имплантируется в мозг и управляется генератором, имплантированным в грудную клетку. Стимуляция непрерывна, а ее частота и уровень индивидуальны.
DBS изучался как средство для лечения депрессии или обсессивно-компульсивного расстройства (ОКР). В настоящее время существует освобождение от использования гуманитарных устройств для использования DBS для лечения ОКР, но его использование при депрессии остается только на экспериментальной основе. Обзор всех 22 опубликованных исследований по тестированию DBS на депрессию показал, что только три из них были высокого качества, потому что в них была не только группа лечения, но и контрольная группа, которая не получала DBS. Обзор показал, что в ходе исследований у 40-50% людей после DBS наблюдалось улучшение более чем на 50%.
Обзор всех 22 опубликованных исследований по тестированию DBS на депрессию показал, что только три из них были высокого качества, потому что в них была не только группа лечения, но и контрольная группа, которая не получала DBS. Обзор показал, что в ходе исследований у 40-50% людей после DBS наблюдалось улучшение более чем на 50%.
DBS: как это работает
DBS требует операции на головном мозге. Голову бреют, а затем прикрепляют винтами к прочной раме, которая предотвращает движение головы во время операции. Проводятся сканы головы и головного мозга с помощью МРТ. Хирург использует эти изображения в качестве руководства во время операции. Пациенты находятся в сознании во время процедуры, чтобы дать хирургу обратную связь, но они не чувствуют боли, потому что голова обезболена местной анестезией, а сам мозг не регистрирует боль.
После подготовки к операции в голове просверливаются два отверстия. Оттуда хирург вводит тонкую трубку в мозг, чтобы разместить электроды с каждой стороны определенной области мозга. В случае депрессии первая область мозга, на которую нацелена DBS, называется областью 25 или субгенуальной поясной корой. Было обнаружено, что эта область гиперактивна при депрессии и других расстройствах настроения. Но более поздние исследования были направлены на несколько других областей мозга, пораженных депрессией. Таким образом, DBS теперь нацелен на несколько областей мозга для лечения депрессии. В случае обсессивно-компульсивного расстройства электроды помещают в область мозга (вентральная капсула/вентральное полосатое тело), которая, как считается, связана с расстройством.
В случае депрессии первая область мозга, на которую нацелена DBS, называется областью 25 или субгенуальной поясной корой. Было обнаружено, что эта область гиперактивна при депрессии и других расстройствах настроения. Но более поздние исследования были направлены на несколько других областей мозга, пораженных депрессией. Таким образом, DBS теперь нацелен на несколько областей мозга для лечения депрессии. В случае обсессивно-компульсивного расстройства электроды помещают в область мозга (вентральная капсула/вентральное полосатое тело), которая, как считается, связана с расстройством.
После имплантации электродов и отзыва пациента об их размещении пациент подвергается общей анестезии. Затем электроды прикрепляются к проводам, которые проходят внутри тела от головы до груди, где имплантируется пара генераторов с батарейным питанием. Отсюда электрические импульсы непрерывно доставляются по проводам к электродам в мозгу. Хотя неясно, как именно работает устройство, чтобы уменьшить депрессию или обсессивно-компульсивное расстройство, ученые считают, что импульсы помогают «перезагрузить» неисправную область мозга, чтобы она снова работала нормально.
Побочные эффекты DBS
DBS несет в себе риски, связанные с любым типом операции на головном мозге. Например, процедура может привести к:
- Кровоизлиянию в мозг или инсульту
- Инфекция
- Дезориентация или спутанность сознания
- Нежелательные изменения настроения
- Двигательные расстройства
- Головокружение
- Проблемы со сном
Поскольку процедура все еще изучается, возможны другие побочные эффекты, которые еще не выявлены. Долгосрочные преимущества и побочные эффекты неизвестны.
Дополнительные ресурсы
Federal Resources
- Электросудорожная терапия: Медицинская энциклопедия MedlinePlus
- Глубокая стимуляция мозга: Медицинская энциклопедия MedlinePlus
Клинические испытания
- Присоединиться к исследованию: терапия стимуляцией мозга
- Присоединяйтесь к исследованию: депрессия — взрослые
Исследования
- Журнальные статьи: Ссылки и выдержки из MEDLINE/PubMed (Национальная медицинская библиотека).

Последняя проверка: Июнь 2016 г.
Если не указано иное, информация и публикации NIMH являются общественным достоянием и доступны для бесплатного использования. Цитирование NIMH приветствуется. Дополнительную информацию см. на странице со ссылкой на информацию и публикации NIMH .
Глубокая стимуляция мозга | Johns Hopkins Medicine
Что такое глубокая стимуляция мозга?
Глубокая стимуляция мозга (DBS) — это нейрохирургическая процедура, в которой используются имплантированные электроды и электрическая стимуляция для лечения двигательных расстройств, связанных с болезнью Паркинсона (БП), эссенциальным тремором, дистонией и другими неврологическими состояниями.
Врачи могут использовать DBS при двигательных расстройствах или нервно-психических состояниях, когда лекарства стали менее эффективными или если их побочные эффекты мешают повседневной деятельности человека.
Как работает глубокая стимуляция мозга?
Связанные с движением симптомы болезни Паркинсона и других неврологических состояний вызваны дезорганизованными электрическими сигналами в областях мозга, которые контролируют движения. В случае успеха DBS прерывает нерегулярные сигналы, вызывающие тремор и другие двигательные симптомы.
В случае успеха DBS прерывает нерегулярные сигналы, вызывающие тремор и другие двигательные симптомы.
После серии тестов, определяющих оптимальное размещение, нейрохирурги имплантируют один или несколько проводов, называемых «отведениями», внутрь мозга. Отведения соединены изолированным удлинителем провода с очень маленьким нейростимулятором (электрическим генератором), имплантированным под ключицу человека, подобно кардиостимулятору. Непрерывные импульсы электрического тока от нейростимулятора проходят через отведения в мозг.
Через несколько недель после установки нейростимулятора врач программирует его на подачу электрического сигнала. Этот процесс программирования может занять более одного посещения в течение нескольких недель или месяцев, чтобы убедиться, что ток правильно отрегулирован и дает эффективные результаты. При настройке устройства врач ищет оптимальный баланс между улучшением контроля симптомов и ограничением побочных эффектов.
Кто является кандидатом на глубокую стимуляцию мозга?
DBS — это больше, чем просто хирургическая процедура. Он включает в себя серию оценок, процедур и консультаций до и после фактической операции, поэтому люди, заинтересованные в лечении с помощью DBS, должны быть готовы посвятить время этому процессу.
Он включает в себя серию оценок, процедур и консультаций до и после фактической операции, поэтому люди, заинтересованные в лечении с помощью DBS, должны быть готовы посвятить время этому процессу.
Например, тем, кто не живет близко к медицинскому центру, предлагающему операцию DBS, может потребоваться значительное время на поездки туда и обратно на приемы.
Процедура, а также предоперационная оценка и послеоперационное наблюдение могут быть дорогостоящими в зависимости от страхового покрытия пациента. Хирургия DBS — это одобренный FDA метод лечения болезни Паркинсона, и Medicare и большинство частных страховых компаний покрывают эту процедуру, но степень покрытия будет зависеть от индивидуального полиса каждого человека.
Потенциальные пациенты должны иметь реалистичные ожидания относительно результатов DBS. Хотя DBS может улучшить двигательные симптомы болезни Паркинсона и значительно улучшить качество жизни правильно отобранных пациентов, вряд ли он вернет кому-либо идеальное здоровье.
Болезнь Паркинсона
Три типа пациентов с БП обычно получают пользу от DBS:
Пациенты с неконтролируемым тремором, у которых лекарства оказались неэффективными.
Пациенты с симптомами, которые хорошо реагируют на лекарства, но у которых после прекращения действия лекарств возникают серьезные двигательные флуктуации и дискинезии, несмотря на корректировку лекарств.
Пациенты, у которых двигательные симптомы могут реагировать на более высокие или более частые дозы лекарств, но которые ограничены в этом из-за побочных эффектов.
Эссенциальный тремор
Эссенциальный тремор является наиболее распространенным двигательным расстройством, и DBS может быть эффективной терапией, особенно в тяжелых случаях, когда дрожь может привести к инвалидности, ограничивая выполнение повседневных задач, таких как одевание, бритье, прием пищи или питье. Поскольку тремор является единственным симптомом эссенциального тремора, DBS может улучшить жизнь людей с этим заболеванием и помочь им нормально функционировать.
Дистония
Дистония — относительно редкое двигательное расстройство, но его симптомы — ненормальные позы и скручивающие движения — могут реагировать на DBS, когда лекарства не обеспечивают адекватного облегчения. Индивидуальная реакция на DBS зависит от основной причины дистонии — генетической, лекарственной или другого фактора. Если причина неизвестна, врач, скорее всего, проведет дополнительные тесты в рамках обследования DBS.
Психиатрические заболевания
Некоторые недавние исследования показали, что людям, живущим с депрессией, обсессивно-компульсивным расстройством (ОКР) или синдромом Туретта, может помочь хирургия DBS. Необходимы дополнительные исследования, чтобы определить, эффективен ли DBS при лечении психических расстройств и перевешивают ли какие-либо преимущества риски и побочные эффекты.
Выбор операции по глубокой стимуляции мозга
Операция DBS не рекомендуется всем людям, страдающим болезнью Паркинсона или другими двигательными расстройствами. Разговор с неврологом, который специализируется на двигательных расстройствах, может определить, является ли человек хорошим кандидатом на DBS.
Разговор с неврологом, который специализируется на двигательных расстройствах, может определить, является ли человек хорошим кандидатом на DBS.
Почему врач может (или не может) выбрать глубокую стимуляцию мозга
По данным Национального фонда Паркинсона, идеальным кандидатом на операцию DBS при болезни Паркинсона является:
Симптомы болезни Паркинсона, которые мешают повседневной жизни.
Колебания подвижности из-за лекарств для ПД («феномен «включено-выключено») с дискинезией или без нее (непроизвольные подергивания, особенно в руках и голове).
Постоянный хороший ответ на лекарства для ПД, даже если эффекты лекарств могут исчезнуть раньше, чем в прошлом.
История приема нескольких различных комбинаций лекарств от БП под наблюдением невролога, специализирующегося на двигательных расстройствах.
Эти факторы* могут сделать человека менее чем идеальным кандидатом на операцию DBS:
Трудности с равновесием, ходьбой или «замирание» как основной инвалидизирующий симптом.

Первичный симптом затруднения речи.
Постоянная спутанность сознания и проблемы с памятью и мышлением.
Психиатрическое состояние, такое как депрессия или тревога, которое не улучшилось или не стабилизировалось с помощью другого лечения.
Еще одно состояние, повышающее риск хирургических осложнений.
*Некоторые из этих факторов поддаются лечению. Наличие одного или нескольких не лишает человека права на будущую операцию DBS, но врач может порекомендовать более агрессивную терапию, ориентированную на эти проблемы, до операции.
Тестирование перед глубокой стимуляцией мозга
Для пациентов с болезнью Паркинсона врач должен подтвердить, что ПД чувствителен к леводопа, и определить, какие симптомы с наибольшей вероятностью реагируют на DBS, и обсудить их с пациентом.
Для достижения этих двух целей невролог, занимающийся двигательными расстройствами, обследует пациента в отсутствие его или ее лекарств от ПД, а затем еще раз после их приема. Наблюдение за влиянием препаратов ПД на двигательные и немоторные симптомы помогает врачу и пациенту определить хорошие целевые симптомы для DBS.
Наблюдение за влиянием препаратов ПД на двигательные и немоторные симптомы помогает врачу и пациенту определить хорошие целевые симптомы для DBS.
Когнитивная оценка может помочь определить способность человека участвовать в процедуре, которая включает в себя обратную связь с врачом во время операции и в процессе настройки нейростимулятора. Эта оценка также информирует команду о риске ухудшения спутанности сознания или когнитивных проблем после процедуры.
В некоторых больницах также проводят осмотр по трудотерапии или оценку речи, языка и глотания. Психиатр может осмотреть человека, чтобы определить, требует ли лечения такое состояние, как депрессия или тревога, перед процедурой DBS.
Процедура глубокой стимуляции мозга
В некоторых случаях хирург вводит и электрод, и нейростимулятор; в других случаях две операции могут выполняться отдельно, с имплантацией нейростимулятора через несколько дней или недель после установки электрода.
Стереотаксическая DBS в сравнении с интервенционной DBS под визуальным контролем
Стереотаксическая DBS хирургия требует, чтобы пациент прекратил прием лекарств. Во время процедуры рама стабилизирует голову и предоставляет координаты, помогающие хирургам направить электрод в правильное место в мозгу. Пациент получает местную анестезию (обезболивающее лекарство), чтобы ему было комфортно на каждом этапе, а также мягкое седативное средство, помогающее расслабиться.
Во время процедуры рама стабилизирует голову и предоставляет координаты, помогающие хирургам направить электрод в правильное место в мозгу. Пациент получает местную анестезию (обезболивающее лекарство), чтобы ему было комфортно на каждом этапе, а также мягкое седативное средство, помогающее расслабиться.
Во время операции DBS под визуальным контролем, например, при интервенционной МРТ (iMRI) или КТ, пациент часто спит под общей анестезией, в то время как хирург использует изображения головного мозга, чтобы направить электрод к цели.
Некоторые передовые центры предлагают как стереотаксическую, так и под контролем iMRI хирургию DBS. В этом случае врач и пациент обсудят, какая процедура лучше, исходя из ряда факторов.
Например, врач может порекомендовать процедуру под визуальным контролем детям, пациентам с тяжелыми симптомами, тем, кто испытывает особую тревогу или страх, или тем, чьи электроды проходят в определенные части мозга.
Как правило, операция DBS следует следующему процессу:
Имплантация электродов
Человек снимает одежду, украшения или другие предметы, которые могут помешать проведению процедуры.

После сбривания небольшого количества волос за линией роста волос бригада хирургов вводит местную анестезию (обезболивающее лекарство) в кожу головы для размещения каркаса головы.
Каркас головы (или «ореол») крепится к черепу с помощью винтов и остается на месте в течение всей процедуры, чтобы удерживать голову в правильном положении.
Затем команда использует компьютерную томографию или магнитно-резонансную томографию, чтобы точно определить целевое место в мозгу, куда будет направляться электрод.
После еще одного обезболивающего нейрохирург просверливает маленькое отверстие в черепе, чтобы вставить электрод.
Команда записывает процесс прохождения электрода через мозговую ткань, чтобы обеспечить точное размещение электрода. Человека могут попросить пошевелить лицом, рукой или ногой в определенное время во время записи.

После установки электрода к нему присоединяется внешний нейростимулятор. Электрическая стимуляция, проводимая через электрод в течение короткого периода времени, помогает врачам увидеть, улучшаются ли симптомы или появляются побочные эффекты (такие как мышечные сокращения или зрительные явления).
Удлинительный провод прикрепляется к электроду и помещается под кожу головы, соединяя электрод с нейростимулятором.
Отверстие в черепе закрывается пластиковой крышкой и швами.
Микроэлектродная запись
Микроэлектродная запись (MER) использует электрический ток (5-100 мкА) очень высокой частоты (300 Гц) для точного определения хирургического участка для имплантации глубокого стимулятора мозга (DBS). Этот метод был впервые применен в Университете Джона Хопкинса и одобрен Целевой группой по хирургии болезни Паркинсона Американской академии неврологии, Комитетом по оценке терапии и технологий.
Поскольку структура мозга каждого человека различается, информация, полученная с помощью MER, дает точную цель для окончательного размещения DBS. Микроэлектрод позволяет хирургической бригаде визуализировать и слышать активность нейронов из разных областей мозга, чтобы идентифицировать определенные структуры на основе уникальных паттернов активности нейронов. Пациент должен быть в сознании (не под общей анестезией), чтобы MER мог дать высококачественную информацию.
Размещение нейростимулятора
Эта процедура проводится под общим наркозом, поэтому человек спит. Хирургическая бригада вводит нейростимулятор под внешние слои кожи, обычно прямо под ключицей, но иногда в грудь или живот. Удлинительный провод от электрода присоединяется к нейростимулятору.
После операции по глубокой стимуляции мозга
В больнице
Как правило, пребывание в больнице после операции DBS составляет 24 часа, но может быть дольше в зависимости от того, насколько быстро пациент выздоровеет и будет готов вернуться домой. Врач посетит, убедится, что человек готов к отъезду, и даст инструкции по уходу на дому.
Врач посетит, убедится, что человек готов к отъезду, и даст инструкции по уходу на дому.
Дома
Дома важно, чтобы разрезы были чистыми и сухими. Врач предоставит пациенту подробную информацию о том, как принимать ванну, пока место операции заживает. Если есть швы, их снимут во время последующего визита в клинику. Клейкие полоски, если они есть, должны оставаться сухими и обычно отпадают в течение нескольких дней.
Пациенту будет выдан магнит, который можно использовать для включения или выключения нейростимулятора в соответствии с условиями, предписанными врачом.
Программирование нейростимулятора
После того, как провод(а) DBS и нейростимулятор будут на месте, пациент вернется к врачу, чтобы запрограммировать нейростимулятор для оптимальной электрической стимуляции. Программирование обычно начинается через несколько недель после процедуры DBS, хотя некоторые врачи активируют нейростимулятор перед выпиской пациента из больницы после операции.
Программирование требует времени и может потребовать нескольких встреч для настройки параметров нейростимулятора. В то же время врачи рассмотрят лекарства и дозировки пациента, чтобы лекарства эффективно работали с электрической стимуляцией для контроля симптомов.
Даже после регулировки пациенту необходимо будет периодически возвращаться для осмотра. Врач определяет частоту повторных приемов в зависимости от конкретной ситуации каждого пациента.
Нейростимулятор работает от батареи, которой обычно хватает на три-пять лет. Когда батарея начинает изнашиваться, врачи могут заменить нейростимулятор в амбулаторных условиях. Есть также перезаряжаемые нейростимуляторы, которые работают дольше, но требуют регулярной подзарядки.
Долгосрочные эффекты глубокой стимуляции мозга
Операция DBS может помочь людям с болезнью Паркинсона улучшить симптомы тремора, скованности, медлительности и дискинезии. Это также может уменьшить дозу лекарств, необходимых пациенту для лечения болезни Паркинсона.
Исследователи, которые наблюдали за пациентами после DBS, обнаружили, что многие пациенты продолжают улучшать свои симптомы в течение нескольких лет после процедуры и могут есть, пользоваться туалетом и принимать пищу самостоятельно. Пациенты, получающие лечение с помощью DBS по поводу двигательных расстройств, могут испытывать или не испытывать изменения в памяти, мышлении или настроении.
В настоящее время болезнь Паркинсона представляет собой прогрессирующее заболевание, которое невозможно полностью остановить. Даже в то время как DBS продолжает воздействовать на тремор, скованность и медлительность, могут все еще появляться другие симптомы, такие как плохая осанка, нарушение речи, замирание походки, проблемы с равновесием и слабоумие.
Особые меры предосторожности после глубокой стимуляции мозга
Как правило, людям, перенесшим операцию DBS, следует:
Всегда носите с собой удостоверение личности, в котором указано, что у них есть нейростимулятор DBS. Кроме того, они могут захотеть носить медицинский идентификационный браслет с указанием этой информации.
Кроме того, они могут захотеть носить медицинский идентификационный браслет с указанием этой информации.
Люди с нейростимулятором должны сообщить об этом сотрудникам службы безопасности аэропорта, прежде чем проходить через детекторы аэропорта. Многие детекторы в аэропортах безопасны для кардиостимуляторов, но небольшое количество металла в нейростимуляторе может вызвать срабатывание сигнализации. Пациенты, отобранные для дополнительного скрининга с помощью ручных детекторных устройств, должны вежливо напомнить специалистам, проводящим скрининг, о том, что детекторную палочку нельзя держать над нейростимулятором дольше нескольких секунд, поскольку эти устройства содержат магниты, которые могут повлиять на работу или программирование нейростимулятора.
Пациенты с электродами и нейростимуляторами могут не проходить определенные процедуры МРТ. Пациенты должны всегда консультироваться со своим врачом перед любым типом МРТ, хотя при определенных обстоятельствах DBS может быть совместима с MRI. Им следует избегать мест с сильными магнитными полями, таких как электрогенераторы и автомобильные свалки, где используются большие магниты.
Им следует избегать мест с сильными магнитными полями, таких как электрогенераторы и автомобильные свалки, где используются большие магниты.
Пациентам, перенесшим операцию DBS, следует избегать использования тепла в физиотерапии для лечения мышц.
Им также следует избегать высоковольтных или радарных машин, таких как радио- или телевизионные передатчики, электродуговые сварочные аппараты, высоковольтные провода, радарные установки или плавильные печи.
Если пациентам назначена хирургическая процедура, они должны заранее сообщить своему хирургу, что у них есть нейростимулятор . Важно проконсультироваться по поводу особых мер предосторожности до и во время операции, поскольку такое оборудование, как электрокоагулятор, который останавливает кровотечение, может мешать работе нейростимулятора.
При участии в физических, развлекательных или спортивных мероприятиях пациенты должны защищать область нейростимулятора от травм. Удар в грудь рядом с кардиостимулятором может повлиять на его работу и требует обращения к врачу.
Удар в грудь рядом с кардиостимулятором может повлиять на его работу и требует обращения к врачу.
Глубокая стимуляция мозга – преимущества, риски и условия лечения
Глубокая стимуляция мозга (DBS) — это плановая хирургическая процедура, при которой электроды имплантируются в определенные области мозга. Эти электроды или отведения генерируют электрические импульсы, которые контролируют аномальную активность мозга. Электрические импульсы также могут приспосабливаться к химическому дисбалансу в мозге, вызывающему различные состояния. Стимуляция областей мозга контролируется программируемым генератором, который помещается под кожу в верхней части грудной клетки.
Система DBS состоит из трех отдельных компонентов:
- Электрод, или электрод, представляет собой тонкий изолированный провод, вставленный через небольшое отверстие в черепе и имплантированный в определенную область мозга.
- Удлинительный провод также изолирован и пропущен под кожу головы, шеи и плеча, соединяя электрод с внутренним генератором импульсов (ВГИ).

- IPG является третьей частью системы и обычно имплантируется под кожу в верхнюю часть грудной клетки.
Состояния, которые лечат с помощью DBS:
- Дистония
- Эпилепсия
- Эссенциальный тремор
- Обсессивно-компульсивное расстройство
- Болезнь Паркинсона
DBS — это хирургическое вмешательство, используемое для лечения пациентов с двигательными расстройствами, такими как эссенциальный тремор, болезнь Паркинсона и дистония. Его также можно использовать для контроля симптомов обсессивно-компульсивного расстройства и эпилепсии. Эта процедура используется, когда лекарства больше не эффективны для пациентов, поддерживающих хорошее качество жизни.
Эти заболевания поражают сотни тысяч людей во всем мире. DBS использовался для лечения более 160 000 человек с различными неврологическими заболеваниями.
Каждый тип заболевания имеет множество симптомов, которые могут возникнуть у пациентов. Наиболее распространенными являются:
Дистония
- Непроизвольные сокращения мышц, возникающие во время определенных действий (например, при письме)
- Мышечные сокращения усиливаются при стрессе, усталости или тревоге
Эпилепсия
- Временная путаница
- Заклинание пристального взгляда
- Потеря сознания
- Неконтролируемые подергивания рук или ног
- Эмоциональные реакции, такие как страх, тревога или дежавю
Эссенциальный тремор
- Тремор, возникающий во время повседневной деятельности, такой как письмо или питье
Обсессивно-компульсивное расстройство
- Боязнь микробов или заражения
- Агрессивные мысли по отношению к другим или к себе
- Иметь вещи симметрично или в идеальном порядке
- Чрезмерная уборка или мытье рук
- Навязчивый счет
- Многократная проверка вещей (например, духовка выключена, дверца заперта и т.
 д.)
д.)
Болезнь Паркинсона
- Тремор
- Брадикинезия – замедление движений
- Жесткость
- Аномальная ходьба
DBS используется, когда лекарства больше не эффективны для пациентов, поддерживающих хорошее качество жизни. Обратитесь к врачу, если какой-либо из вышеперечисленных симптомов сохраняется в течение длительного периода, чтобы обсудить, является ли DBS правильным лечением.
За пациентами может ухаживать многопрофильная команда профессионалов, в которую входят невролог, нейрохирург, нейропсихолог и психиатр. Часто пациенты с болезнью Паркинсона или тремором могут пройти тестирование двигательных симптомов при приеме и отсутствии лекарств для оценки тяжести заболевания. Тестирование на эпилепсию может включать электроэнцефалографию, включая более сложные тесты. Некоторым пациентам во время обследования может быть проведена нейропсихологическая оценка. Пациенты с обсессивно-компульсивным расстройством должны пройти тестирование по обсессивно-компульсивной шкале Йеля-Брауна (YBOC).
Перед операцией пациенты проходят:
- Анализы крови и мочи
- Это помогает выявить токсины и аномалии
- МРТ и/или компьютерная томография
- Визуализация может помочь врачам воздействовать на нужную область мозга для облегчения симптомов.
- Медицинское освидетельствование
Кандидаты на DBS соответствуют следующим критериям:
- Симптомы существенно снижают качество жизни.
- Симптомы не поддаются контролю, несмотря на прием подходящей дозы лекарств.
- Побочные эффекты, вызванные текущими лекарствами, недопустимы
Перед рассмотрением вопроса о хирургическом вмешательстве, таком как DBS, врачи могут рассмотреть любое из следующих методов лечения.
- Лекарства
- Физиотерапия
- Может выполняться на одной или обеих сторонах мозга, в зависимости от симптомов.
- Эффекты обратимы и могут быть настроены индивидуально для каждого клинического состояния пациента.

- Настройки стимуляции можно изменить, чтобы уменьшить потенциальные побочные эффекты и повысить эффективность с течением времени.
- Устройство обеспечивает непрерывный контроль симптомов 24 часа в сутки.
- Пациенты, перенесшие DBS, могут участвовать в других видах лечения, таких как стволовые клетки или генная терапия, когда они станут доступны.
У правильно отобранных пациентов DBS безопасен и эффективен. Риски и потенциальные побочные эффекты существуют, но они, как правило, легкие и обратимые.
Риски могут включать:
- 1% риск кровоизлияния в мозг, включая инсульт
- Инфекция
- Неисправность устройства
- Отсутствие пользы при определенных симптомах
- Головная боль
- Ухудшение психического или эмоционального состояния
Во время стимуляции побочные эффекты могут включать:
- Временное покалывание лица или конечностей
- Ощущение напряжения в мышцах
- Проблемы с речью или зрением
- Потеря равновесия
- Чарльз, Д.
 , Толлесон, К., Дэвис, Т.Л., Гилл, К.Е., Молинари, А.Л., Блитон, М.Дж., … Конрад, П.Е. (2012). Пилотное исследование, оценивающее возможность применения двусторонней глубокой стимуляции субталамического ядра на очень ранней стадии болезни Паркинсона: дизайн и обоснование исследования. Журнал болезни Паркинсона, 2(3), 215–223. doi: 10.3233/JPD-2012-012095. В этом пилотном исследовании, проведенном в Университете Вандербильта, изучается применение DBS у пациентов с болезнью Паркинсона на ранней стадии. Они надеются использовать этот набор данных для поддержки и разработки многоцентрового исследования фазы III.
, Толлесон, К., Дэвис, Т.Л., Гилл, К.Е., Молинари, А.Л., Блитон, М.Дж., … Конрад, П.Е. (2012). Пилотное исследование, оценивающее возможность применения двусторонней глубокой стимуляции субталамического ядра на очень ранней стадии болезни Паркинсона: дизайн и обоснование исследования. Журнал болезни Паркинсона, 2(3), 215–223. doi: 10.3233/JPD-2012-012095. В этом пилотном исследовании, проведенном в Университете Вандербильта, изучается применение DBS у пациентов с болезнью Паркинсона на ранней стадии. Они надеются использовать этот набор данных для поддержки и разработки многоцентрового исследования фазы III. - Хамани, К., Пилицис, Дж., Ругани, А.И., Розенов, Дж.М., Патил, П.Г., Славин, К.С., … Калканис, С. (2014). Глубокая стимуляция мозга при обсессивно-компульсивном расстройстве. Нейрохирургия, 75 (4), 327–333. doi: 10.1227/neu.0000000000000499
В этой статье установлены основанные на фактических данных рекомендации по DBS при лечении пациентов с ОКР. Авторы пришли к выводу, что из существующих исследований в одном двойном слепом рандомизированном контролируемом исследовании класса I и двух класса II было сообщено, что двусторонний DBS более эффективен в улучшении симптомов ОКР, чем ложное лечение.
- Саланова, В., Витт, Т., Уорт, Р., Генри, Т. Р., Гросс, Р. Э., Наззаро, Дж. М., … Исследовательская группа SANTE (2015). Долгосрочная эффективность и безопасность таламической стимуляции при лекарственно-резистентной парциальной эпилепсии. Неврология, 84(10), 1017–1025. doi:10.1212/WNL.0000000000001334. Это исследование было направлено на сообщение о долгосрочной эффективности и результатах исследования SANTE, в котором изучалась DBS переднего ядра таламуса для лечения эпилепсии. Они обнаружили, что долгосрочное наблюдение за ANT DBS сохраняло эффективность и безопасность у пациентов, которые сопротивлялись предшествующему лечению.
- Фоллетт, К. А., Уивер, Ф. М., Стерн, М., Хур, К., Харрис, К. Л., Луо, П., … Реда, Д. Дж. (2010). Паллидальная и субталамическая стимуляция глубокого мозга при болезни Паркинсона. Медицинский журнал Новой Англии, 362 (22), 2077–2091. дои: 10.1056/nejmoa0
3. Это исследование проводилось как многоцентровое клиническое исследование пациентов с идиопатической болезнью Паркинсона. Пациентов рандомизировали для стимуляции либо внутреннего бледного шара, либо субталамического ядра. Авторы пришли к выводу, что все пациенты имели сопоставимое улучшение двигательной функции после любого типа стимуляции.
Пациентов рандомизировали для стимуляции либо внутреннего бледного шара, либо субталамического ядра. Авторы пришли к выводу, что все пациенты имели сопоставимое улучшение двигательной функции после любого типа стимуляции. - Уивер, Ф. М., Фоллетт, К. А., Стерн, М., Луо, П., Харрис, К. Л., Хур, К., … Реда, Д. Дж. (2012). Рандомизированное исследование глубокой стимуляции мозга при болезни Паркинсона: результаты за тридцать шесть месяцев. Неврология, 79(1), 55–65. doi: 10.1212/WNL.0b013e31825dcdc1. Это исследование было проведено для сравнения долгосрочных результатов у пациентов, получавших DBS, нацеленных либо на внутренний бледный шар, либо на субталамическое ядро. Авторы пришли к выводу, что исследование предоставило доказательства класса III о том, что в течение трех лет улучшение двигательных симптомов БП остается стабильным и не зависит от хирургической цели.
- Хирургический вариант, способный изменить жизнь пациентов с ОКР: прочтите и посмотрите историю Эрин, энергичной 21-летней женщины, которая боролась с ОКР.
 В этой статье исследуется, как глубокая стимуляция мозга вернула Эрин жизнь. Эта процедура была первой в своем роде, проведенной в медицинском центре Олбани — единственном учреждении, предлагающем такое лечение между Нью-Йорком и Бостоном. По словам самой Эрин: «Теперь я могу быть тем, кто я есть на самом деле, и рассказывать людям свою историю и, надеюсь, вдохновлять людей и помогать им на этом пути».
В этой статье исследуется, как глубокая стимуляция мозга вернула Эрин жизнь. Эта процедура была первой в своем роде, проведенной в медицинском центре Олбани — единственном учреждении, предлагающем такое лечение между Нью-Йорком и Бостоном. По словам самой Эрин: «Теперь я могу быть тем, кто я есть на самом деле, и рассказывать людям свою историю и, надеюсь, вдохновлять людей и помогать им на этом пути». - История Карен и Джима: общее путешествие жизни, любви и DBS: прочтите о Карен и Джиме. У каждого из них был диагностирован болезнь Паркинсона до того, как они встретились. Следуйте за ними в их путешествии, когда они влюбляются после встречи друг с другом из онлайн-группы поддержки. Посмотрите, как они обнимали друг друга и DBS.
- История Кей — пациентка с болезнью Паркинсона: прочитайте о Кей, 68-летней женщине, страдающей болезнью Паркинсона. В статье и видео рассказывается, как DBS помог ей вернуться к жизни. По словам самой Кей: «Как будто меня снова возбудили. Это было похоже на чудо».

Электроды и электрические системы, обеспечивающие стимуляцию, как правило, очень хорошо переносятся и не вызывают значительных изменений в окружающих тканях головного мозга. Может произойти смещение электрода с исходного места имплантации. Также может наблюдаться временное усиление тремора при прекращении стимуляции. Риск хирургического вмешательства возрастает у людей в возрасте 70 лет и старше, а также у людей с другими заболеваниями, такими как цереброваскулярные заболевания и высокое кровяное давление. Преимущества хирургического вмешательства всегда следует тщательно сопоставлять с его рисками. Хотя большой процент пациентов сообщает о значительном улучшении после операции DBS, нет гарантии, что операция поможет каждому человеку.
Страницы пациентов создаются профессиональными нейрохирургами с целью предоставления полезной информации общественности.
Julie G Pilitsis, MD, PhD, FAANS
Кафедра нейробиологии и экспериментальной терапии
Профессор нейрохирургии и нейробиологии и экспериментальной терапии
Медицинский колледж Олбани
Доктор Пилицис специализируется на нейромодуляции и занимается исследованиями в области лечения двигательных расстройств и хронической боли.



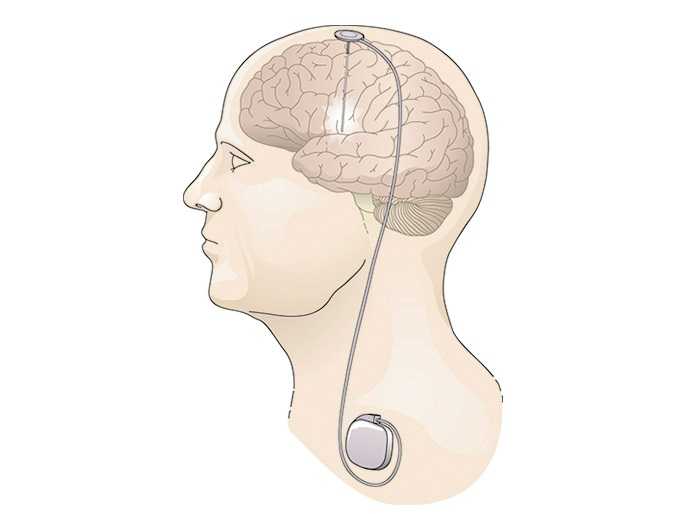


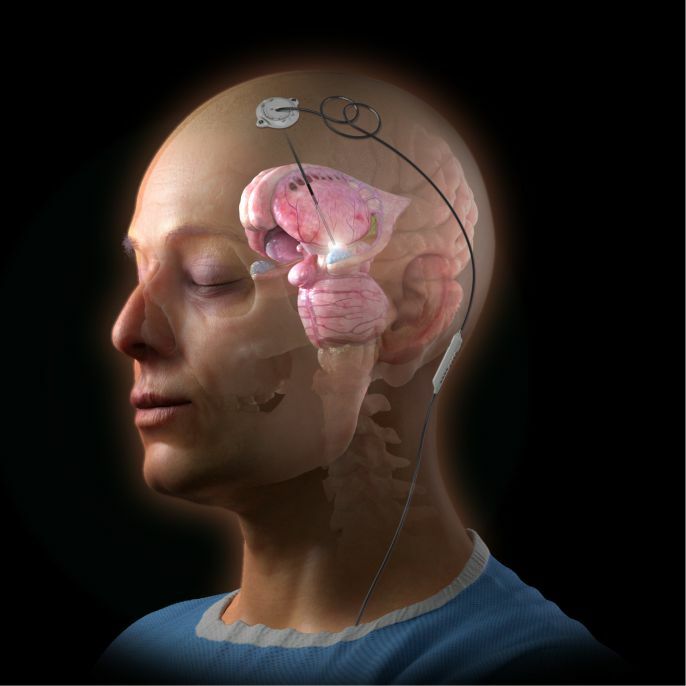 д.)
д.)
 , Толлесон, К., Дэвис, Т.Л., Гилл, К.Е., Молинари, А.Л., Блитон, М.Дж., … Конрад, П.Е. (2012). Пилотное исследование, оценивающее возможность применения двусторонней глубокой стимуляции субталамического ядра на очень ранней стадии болезни Паркинсона: дизайн и обоснование исследования. Журнал болезни Паркинсона, 2(3), 215–223. doi: 10.3233/JPD-2012-012095. В этом пилотном исследовании, проведенном в Университете Вандербильта, изучается применение DBS у пациентов с болезнью Паркинсона на ранней стадии. Они надеются использовать этот набор данных для поддержки и разработки многоцентрового исследования фазы III.
, Толлесон, К., Дэвис, Т.Л., Гилл, К.Е., Молинари, А.Л., Блитон, М.Дж., … Конрад, П.Е. (2012). Пилотное исследование, оценивающее возможность применения двусторонней глубокой стимуляции субталамического ядра на очень ранней стадии болезни Паркинсона: дизайн и обоснование исследования. Журнал болезни Паркинсона, 2(3), 215–223. doi: 10.3233/JPD-2012-012095. В этом пилотном исследовании, проведенном в Университете Вандербильта, изучается применение DBS у пациентов с болезнью Паркинсона на ранней стадии. Они надеются использовать этот набор данных для поддержки и разработки многоцентрового исследования фазы III.
 Пациентов рандомизировали для стимуляции либо внутреннего бледного шара, либо субталамического ядра. Авторы пришли к выводу, что все пациенты имели сопоставимое улучшение двигательной функции после любого типа стимуляции.
Пациентов рандомизировали для стимуляции либо внутреннего бледного шара, либо субталамического ядра. Авторы пришли к выводу, что все пациенты имели сопоставимое улучшение двигательной функции после любого типа стимуляции. В этой статье исследуется, как глубокая стимуляция мозга вернула Эрин жизнь. Эта процедура была первой в своем роде, проведенной в медицинском центре Олбани — единственном учреждении, предлагающем такое лечение между Нью-Йорком и Бостоном. По словам самой Эрин: «Теперь я могу быть тем, кто я есть на самом деле, и рассказывать людям свою историю и, надеюсь, вдохновлять людей и помогать им на этом пути».
В этой статье исследуется, как глубокая стимуляция мозга вернула Эрин жизнь. Эта процедура была первой в своем роде, проведенной в медицинском центре Олбани — единственном учреждении, предлагающем такое лечение между Нью-Йорком и Бостоном. По словам самой Эрин: «Теперь я могу быть тем, кто я есть на самом деле, и рассказывать людям свою историю и, надеюсь, вдохновлять людей и помогать им на этом пути».