байкальские бактерии могут хранить неизвестные науке антибиотики
6 марта, 2020 17:04
Источник:
Газета.ru
Биологи из Иркутского государственного университета вместе с коллегами из Университета Северной Флориды (США) изучили обмен веществ байкальских актинобактерий — крупных микроорганизмов, способных синтезировать биологически активные вещества. Оказалось, что у них отсутствуют гены распространенных для этой группы ферментов, отвечающих за производство антибиотиков. Это значит, что эти микроорганизмы борются с микробами при помощи других белков и, возможно, пока неизвестных науке соединений. Статья опубликована в Aquatic microbial ecology. Работа выполнена при поддержке гранта Российского научного фонда.
Поделиться
Актинобактерии – класс бактерий больших размеров и сложных форм, обладающих способностью разрушать токсичные соединения, загрязняющие окружающую среду. Они – производители вторичных продуктов обмена веществ, которые не нужны им для роста и развития, но выполняют некоторые иные функции. Среди таких соединений – стимулирующие различные клеточные процессы факторы роста и феромоны для «химического общения». Человек же использует свойство этих веществ, чтобы подавлять рост патогенных бактерий и грибов, и применяет их в медицине. В этой работе ученые исследовали образование вторичных продуктов обмена веществ у 24 штаммов актинобактерий, выделенных из отложений Байкала. Ученые сравнили его с процессами у морских и пресноводных организмов.
Они – производители вторичных продуктов обмена веществ, которые не нужны им для роста и развития, но выполняют некоторые иные функции. Среди таких соединений – стимулирующие различные клеточные процессы факторы роста и феромоны для «химического общения». Человек же использует свойство этих веществ, чтобы подавлять рост патогенных бактерий и грибов, и применяет их в медицине. В этой работе ученые исследовали образование вторичных продуктов обмена веществ у 24 штаммов актинобактерий, выделенных из отложений Байкала. Ученые сравнили его с процессами у морских и пресноводных организмов.
«Предыдущие исследования освещают экологию и закономерности географического распространения актинобактерий из наземных и морских экосистем. Однако представители этого класса из пресноводных отложений по-прежнему недостаточно изучены», – считает руководитель проекта по гранту РНФ Максим Тимофеев, доктор биологических наук, директор НИИ биологии Иркутского государственного университета.
Образцы извлекли со дна озера на глубине 200 метров. Чтобы получить колонии актинобактерий, отложения поместили на питательную среду, которая позволила подавить рост остальных микроорганизмов. Спустя три дня из колоний выделили ДНК и при помощи молекулярных методов определили, есть ли специфичные для актинобактерий гены – так можно убедиться, что выросли необходимые для исследования бактерии. В этом случае и в самом эксперименте цепочки ДНК «размножали», потому что в самой клетке материала для анализа слишком мало, а искусственное копирование молекулы решает проблему.
Исследователи уделили внимание генам, которые связаны с синтезом биологически активных соединений. Они обнаружили, что у выделенных штаммов байкальских актинобактерий отсутствуют гены ФАД-зависимых галогеназ. Эти ферменты используют энергию, заключенную в ФАД, и отвечают за присоединение к различным молекулам галогенов, например хлора и брома. В результате получаются такие антибиотики, как тетрациклины, хлорамфеникол и прочие.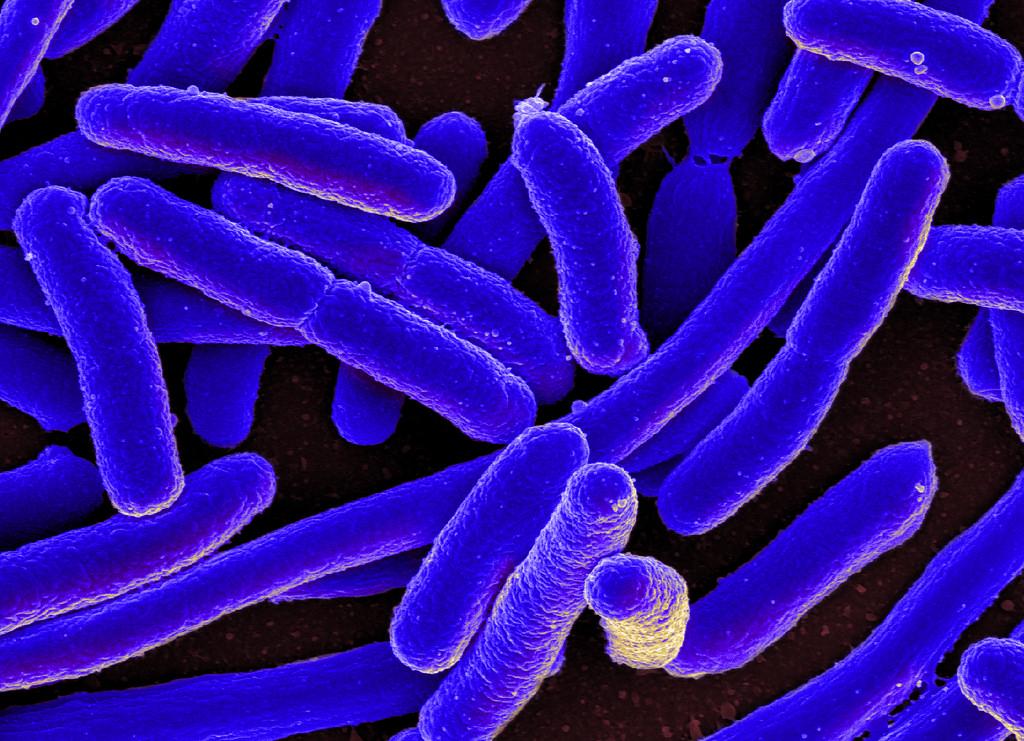 Больше всего галогеназ у морских микроорганизмов. Тот факт, что их нет у байкальских актинобактерий, свидетельствует об их приспособленности к жизни в воде с низким содержанием солей. Вместе с тем биологическая активность наблюдалась у 75% выделенных в ходе исследования штаммов актинобактерий. А значит, она проявилась за счет других ферментов.
Больше всего галогеназ у морских микроорганизмов. Тот факт, что их нет у байкальских актинобактерий, свидетельствует об их приспособленности к жизни в воде с низким содержанием солей. Вместе с тем биологическая активность наблюдалась у 75% выделенных в ходе исследования штаммов актинобактерий. А значит, она проявилась за счет других ферментов.
«Обычные актинобактерии могут включать атомы галогенов в состав химических молекул, которые они синтезируют. Отсутствие данной способности у байкальских актинобактерий является их уникальным отличием, говорящем о длительной эволюции этих видов в условиях ультрапресной среды. Особенности байкальских актинобактерий позволяют говорить об их значительном потенциале для производства неизвестных науке антибиотиков и природных соединений», – говорит Максим Тимофеев.
Теги
Биология, Спецпроект
Бактерии могут менять форму для защиты от антибиотиков
Бактерии могут менять форму для защиты от антибиотиков | НОМЕКО
02. 10.2019
10.2019
Микробиологи из Великобритании доказали, что бактерии могут менять форму и становиться «невидимыми» для антибиотиков, а по окончании их приема вновь вызывать заболевание. Результаты работы описаны в статье, опубликованной в Nature Communications.
Как и все живое на земле, бактерии постоянно развиваются, приспосабливаясь к изменяющимся условиям, в частности, к новым видам антибиотиков. Так, микроорганизмы научились менять свой геном, скрываясь от действия лекарств; разрушать или выводить препарат, которому удалось проникнуть внутрь бактерии; прекращать рост и деление, «обманывая» иммунную систему.
Ученые из Университета Ньюкасла решили сосредоточиться на малоизученном механизме, который делает бактерии устойчивыми даже к самым современным антибиотикам.
Суть его в следующем. Практически все бактерии имеют клеточную стенку — оболочку, которая защищает их разрывов и внешних воздействий, а также придает нужную форму и участвует в делении. У клеток человека такой стенки нет, поэтому наша иммунная система легко определяет бактерии как чужеродные, а антибиотики могут убивать их, не причиняя вреда организму.
У клеток человека такой стенки нет, поэтому наша иммунная система легко определяет бактерии как чужеродные, а антибиотики могут убивать их, не причиняя вреда организму.
Однако порой микробы выживают и без этого защитного слоя, в так называемой L-форме. На существование таких бактерий, лишенных внешнего покрова, ученые обратили внимание еще в 1935 году. Но из-за отсутствия методов их обнаружения доказать, что именно перерождение бактерий в L-форму отвечает за устойчивость к антибиотикам, до сих пор не удавалось.
Найти такие бактерии в образцах, взятых из организма человека, стало возможным лишь благодаря флуоресцентным зондам, которые «распознают» бактериальную ДНК.
В течение полугода ученые из Ньюкаслского университета каждые две недели брали образцы мочи у 30 пациентов с рецидивирующими инфекциями мочевыводящих путей. Собранную базу данных из 360 образцов они поместили в питательные среды с высоким содержанием сахара (он помогает выделить живые L-формы, присутствующие в моче).
В результате впервые удалось достоверно установить, что многие виды бактерий, в том числе кишечная палочка и энтерококк, переживают лечение антибиотиками. И происходит это благодаря образованию L-форм, которые спокойно продолжают жить в организме человека, вызывая повторные пиелонефриты и циститы. Также ученые выяснили, что по завершении лечения антибиотиками эти формы снова восстанавливают свою клеточную стенку.
Данное исследование показывает, как важно тестировать антибиотики в условиях, максимально приближенных к условиям человеческого организма. Правда, при проведении теста на устойчивость бактерий к антибиотикам нередко используются материалы, не позволяющие выживать хрупким L-формам, а значит, не выявляющие причину постоянных рецидивов болезни.
По мнению авторов работы, нужно провести еще серию исследований, чтобы окончательно определить, насколько этот механизм важен по сравнению с другими механизмами устойчивости к антибиотикам. Возможно, сочетание препаратов, одновременно разрушающих клеточную стенку бактерий и нацеленных на L-формы, станет ключом к преодолению их устойчивости к лекарствам.
Возможно, сочетание препаратов, одновременно разрушающих клеточную стенку бактерий и нацеленных на L-формы, станет ключом к преодолению их устойчивости к лекарствам.
ПОСЛЕДНИЕ НОВОСТИ
Ученые выяснили, какие гены отвечают за самый агрессивный рак почки
Новая методика поможет очистить сточные воды от антибиотиков
Препарат от артрита может помочь при диабете и ожирении
ВИЧ способен повышать риски развития лимфомы
19.10.2022
подробнее >>
Разработан новый подход к анализу рисков тромбообразования
21.10.2022
подробнее >>
Ученые доказали, что омега-3 защищает мозг от старения
17.10.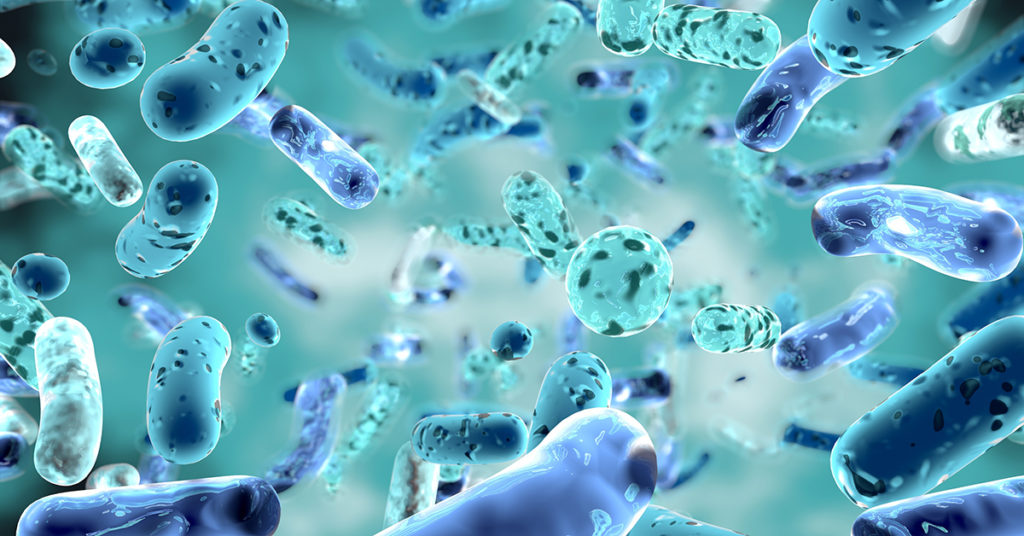 2022
2022
подробнее >>
Создана модель для разработки эффективных противоэпилептических препаратов
14.10.2022
подробнее >>
Деменцию смогут выявлять за девять лет до появления симптомов
12.10.2022
подробнее >>
Количество стволовых клеток в почках с возрастом уменьшается
10.10.2022
подробнее >>
Грамположительные бактерии: характеристики, лечение и примеры
Бактерии бывают всех форм и размеров. Один из способов, которым ученые их классифицируют, — это их реакция на окрашивание по Граму при просмотре под микроскопом. Это относится к тесту окрашивания, при котором грамположительные бактерии имеют толстую клеточную стенку и кажутся синими или фиолетовыми.
Поделиться на PinterestDesign от Medical News Today; фотография Reptile8488/Getty Images
И наоборот, грамотрицательные бактерии плохо удерживают краситель. Грамотрицательные бактерии могут казаться красными под микроскопом, потому что красно-розовый йод используется вместе с краской по Граму в качестве контроля.
Грамотрицательные бактерии могут казаться красными под микроскопом, потому что красно-розовый йод используется вместе с краской по Граму в качестве контроля.
Заболевание могут вызывать как грамположительные, так и грамотрицательные бактерии. Однако они требуют разного лечения. Таким образом, медицинские работники должны уметь идентифицировать тип бактерий, чтобы обеспечить наилучший уход.
Продолжайте читать, чтобы узнать больше о грамположительных бактериях, в том числе об их характеристиках, типичных примерах и заболеваниях, которые они могут вызывать.
Грамположительные бактерии — это бактерии с толстой клеточной стенкой.
Во время окрашивания по Граму — теста, который специалисты используют для изучения бактерий под микроскопом — они кажутся фиолетовыми или синими. Это связано с тем, что клеточная стенка сохраняет цвет по методу окрашивания, разработанному Гансом Христианом Грамом в 1884 г.
Специалисты делят их на грамположительные кокки или бациллы в зависимости от их формы.
Грамположительные бактерии отличаются от грамотрицательных по своему строению. Вот их ключевые характеристики:
- Наружная мембрана: Грамположительные бактерии не имеют наружной мембраны, а грамотрицательные бактерии имеют.
- Цвет: Грамположительные бактерии под микроскопом выглядят синими или фиолетовыми.
- Клеточная стенка: Эта структура окружает клеточную мембрану. У грамположительных бактерий клеточная стенка состоит из нескольких слоев молекул и белков. Он защищает бактерии от повреждения.
- Пептидогликановый слой: У грамположительных бактерий пептидогликан представляет собой структуру толщиной от 20 до 80 нм (нанометров), обнаруженную внутри их клеточной стенки. Толщина этого слоя у грамотрицательных бактерий составляет всего 2–3 нм.
- Форма: Грамположительные бактерии бывают различной формы:
- кокки (сферической или круглой формы)
- бациллы (палочковидные)
- ветвящиеся нити (нитевидные формы)
5 Грамположительные бактерии структуры.
 У них гораздо более тонкий слой пептидогликана, поэтому они не сохраняют кристаллический фиолетовый краситель.
У них гораздо более тонкий слой пептидогликана, поэтому они не сохраняют кристаллический фиолетовый краситель.У них также есть внешняя липидная мембрана, которая защищает их от окружающей среды. Это означает, что они более устойчивы к антибиотикам и другим лекарствам.
Хотя грамотрицательные бактерии труднее поддаются лечению, грамположительные бактерии также могут вызывать проблемы со здоровьем. Многие виды грамположительных бактерий вызывают заболевания, требующие применения специфических антибиотиков.
Узнайте больше о разнице между грамположительными и грамотрицательными бактериями.
Эти овальные или сферические бактерии являются одними из наиболее распространенных известных типов бактерий. Они могут жить парами, цепочками или группами.
Staphylococcus
Эти бактерии растут группами. Staphylococcus обычно заселяет кожу и слизистые оболочки, не вызывая инфекций, и составляет нормальную флору в организме.
Однако, если они попадают в организм и начинают расти в количестве, они могут вызывать серьезные бактериальные инфекции.

Некоторые виды бактерий и инфекций включают:
- Staphylococcus aureus : Это наиболее патогенные бактерии стафилококка. Он вызывает инфекции, такие как:
- bacterial pneumonia
- food poisoning
- skin infections such as cellulitis and folliculitis
- MRSA, a superbug infection
- infections of the lining of the heart, or endocarditis
- Staphylococcus epidermidis : S. epidermis вызывает инфекции в условиях стационара и у человека с ослабленной иммунной системой. Он может вызывать:
- инфекции хирургических участков или мочевых катетеров
- кератит глаз
- эндофтальмит, инфекция внутреннего глаза
- Staphylococcus saprophyticus : Эти бактерии населяют половые органы и промежность. Они могут вызывать такие инфекции, как:
- инфекции мочевыводящих путей
- инфекции почек,
- инфекции уретры, предстательной железы и придатка яичка
бактерии Streptococcus
растут цепочками.
 Они также являются частью нормальной флоры организма, и их можно найти на:
Они также являются частью нормальной флоры организма, и их можно найти на:- кожа
- рот
- пищеварительная система
- половые органы
Когда они проникают в организм и начинают расти, они могут вызывать инфекцию. Некоторые типы бактерий и инфекций включают:
- Streptococcus pneumoniae : Streptococcus pneumoniae является основной причиной бактериальной пневмонии. Это также может вызвать инфекцию носовых пазух и менингит.
- Streptococcus pyogenes : Эти бактерии могут вызвать широкий спектр инфекций, в том числе:
- Scarlet Fever
- Срытокотону. также называемый стрептококком B. Он может вызывать многие серьезные инфекции у новорожденных, такие как:
- сепсис
- пневмония
- менингит
- Enterococcus : Наиболее распространенными типами являются Enterococcus faecalis и Enterococcus faecium .
 Они могут вызывать:
Они могут вызывать:- инфекции мочевыводящих путей
- инфекционный эндокардит
- инфекции кровотока
Бациллы представляют собой палочковидные бактерии, обычно обитающие на коже. Врачи далее подразделяют их на спорообразующие и неспорообразующие.
Формирование спор и бездействие — стратегия, которая помогает бактериям выживать в суровых условиях. Когда окружающая среда становится более благоприятной, они могут прорастать и превращаться в активные бактерии.
Существует два типа:
Bacillus
Эти бактерии являются аэробными, то есть им для выживания необходим кислород.
Споры Bacillus anthracis производят токсин сибирской язвы, потенциально смертельный для людей и животных. Эти споры могут годами сохраняться в почве, прежде чем заразить человека.
Сибирская язва в основном поражает пастбищных животных, таких как крупный рогатый скот и овцы. Однако люди, имеющие дело с инфицированными продуктами животного происхождения, могут заразиться.

Сибирская язва может вызывать различные симптомы: от язв на коже до тяжелого, иногда смертельного, респираторного заболевания.
Bacillus cereus — еще одна спорообразующая бактерия. Он может вызывать:
- болезни пищевого происхождения
- раневые инфекции
- респираторные инфекции
клостридии
Эти бактерии являются анаэробными, то есть им не требуется кислород для выживания. Споры также создают токсины, которые могут вызывать серьезные заболевания человека.
Типы бактерий и инфекций включают:
- Clostridium botulinum : Ботулинический токсин является наиболее смертельным известным токсином. Это может вызвать ботулизм, редкое, но потенциально смертельное заболевание.
- Clostridium perfringens : Люди могут заразиться пищевым отравлением от мяса, зараженного этой бактерией . Это приводит к диарее и спазмам в животе в течение 24 часов или менее.

- Clostridium difficile : Заражение этой бактерией может произойти после лечения антибиотиками. Это также может вызвать различные желудочно-кишечные симптомы. Этот микроорганизм связан с внутрибольничными вспышками и вспышками в жилых домах престарелых.
- Clostridium tetani : Споры этих бактерий вырабатывают столбнячный токсин, который может вызвать инфекцию столбняка. Споры существуют в почве, пыли и навозе и могут попасть в организм через открытые раны.
Лечение грамположительных бактериальных инфекций обычно включает антибиотики. Тип антибиотика зависит от конкретных бактерий, вызывающих инфекцию. Общие варианты лечения грамположительных инфекций:
Пенициллин
Этот антибиотик воздействует на клеточную стенку бактерий, пытаясь разрушить стенку и бактерии. Он может лечить широкий спектр бактериальных инфекций. Например, пенициллин эффективен против Streptococcus 9.
 0060 инфекции, в том числе фарингит и инфекции носовых пазух.
0060 инфекции, в том числе фарингит и инфекции носовых пазух.Его также можно использовать при инфекциях Streptococcus .
Гликопептиды
Врачи могут выбрать эти антибиотики, если у человека серьезная инфекция с участием резистентных к лекарствам бактерий, например, MRSA. Они также разрушают клеточные стенки бактерий.
Они также могут лечить инфекции Enterococcus и Clostridium difficile .
Эритромицин
Если у человека аллергия на пенициллин, обычной альтернативой является эритромицин. Он принадлежит к классу антибиотиков макролидов наряду с кларитромицином и азитромицином. Эти антибиотики работают, препятствуя бактериям производить белки. Они также могут лечить:
- бактериальная пневмония
- острый фарингит
- стафилококковые кожные инфекции
Если у человека сибирская язва, ботулизм или другое заболевание, связанное с токсинами, он также может принимать антибиотики.
 Однако, если споры присутствуют и выделяют токсины, человеку также может потребоваться лечение антитоксинами. Эта терапия работает путем нейтрализации токсинов, вырабатываемых бактериями.
Однако, если споры присутствуют и выделяют токсины, человеку также может потребоваться лечение антитоксинами. Эта терапия работает путем нейтрализации токсинов, вырабатываемых бактериями.Врачам также может потребоваться поддерживающая терапия. Это может включать:
- жидкости для внутривенного введения
- питание
- механическая вентиляция легких
Грамположительные бактерии представляют собой тип бактерий с толстой клеточной стенкой. Эта клеточная стенка помогает защитить бактерии от антибиотиков и других веществ, которые могут их повредить.
Грамположительные бактерии могут вызывать целый ряд инфекций, от пищевых отравлений до серьезных респираторных заболеваний. Некоторые грамположительные бактерии вырабатывают токсины, которые могут вызывать смертельные заболевания. Примеры, приведенные в этой статье, не являются исчерпывающими — существуют другие типы грамположительных бактерий, как и другие антибиотики для их лечения.
Лечение обычно включает антибиотики.
 В некоторых случаях врачи могут порекомендовать антитоксиновую терапию.
В некоторых случаях врачи могут порекомендовать антитоксиновую терапию.Борьба с лекарственно-устойчивыми бактериями: натуральное соединение показывает многообещающие результаты
Поделиться на PinterestПриродное соединение, полученное из растений, может быть эффективным антибактериальным препаратом. Изображение предоставлено: Андрей Онуфриенко/Getty Images.
- Появление устойчивых к антибиотикам бактерий угрожает сделать существующие методы лечения неэффективными и подчеркивает необходимость в новых противомикробных препаратах
- Недавнее исследование показало, что гидрохинин, производное противомалярийного препарата хинина, проявляет антибактериальную активность в отношении нескольких клинически важных бактерий.
- Примечательно, что гидрохинин был эффективен против полирезистентного штамма бактерии Pseudomonas aeruginosa , которая может вызвать инфекцию после операции .

Новое исследование, опубликованное в журнале Tropical Medicine and Infectious Disease показывает, что гидрохинин может убивать и подавлять рост нескольких клинически важных бактерий, включая устойчивый к антибиотикам бактериальный штамм.
Автор исследования доктор Роберт Болдок, старший преподаватель Портсмутского университета в Соединенном Королевстве, сказал:
«Прогрессирующая устойчивость к противомикробным препаратам представляет собой одну из самых серьезных угроз для общественного здравоохранения во всем мире. Без антибиотиков излечимые в настоящее время бактериальные инфекции могут стать опасными для жизни. В результате открытие новых антибиотиков имеет первостепенное значение в гонке против устойчивости к антибиотикам. Это исследование показывает, что гидрохинин, органическое соединение с противомалярийными свойствами, также обладает способностью убивать бактерии».
По данным Всемирной организации здравоохранения (ВОЗ), устойчивость к противомикробным препаратам является одной из основных угроз для здоровья человека в 21 веке.

Устойчивость к противомикробным препаратам стала причиной не менее 1,27 миллиона смертей во всем мире в 2019 г., и, при отсутствии новых методов лечения, ожидается, что к 2050 г. это число вырастет до 10 миллионов в год. Таким образом, существует острая потребность в новых противомикробных препаратах, которые эффективны против устойчивых к антибиотикам бактерий.
Недавно исследователи в Таиланде оценили антибактериальные свойства гидрохинина в отношении ряда клинически важных бактерий. Гидрохинин представляет собой органическое соединение, тесно связанное с противомалярийным препаратом хинином, и используется в кремах для осветления кожи.
Предыдущие исследования показали, что богатые гидрохинином экстракты смолы, полученные из растений, произрастающих в Таиланде, обладают антибактериальными и противогрибковыми свойствами.
В настоящем исследовании исследователи изучили, обладает ли гидрохинин в своем очищенном состоянии способностью убивать или подавлять рост патогенных бактерий.

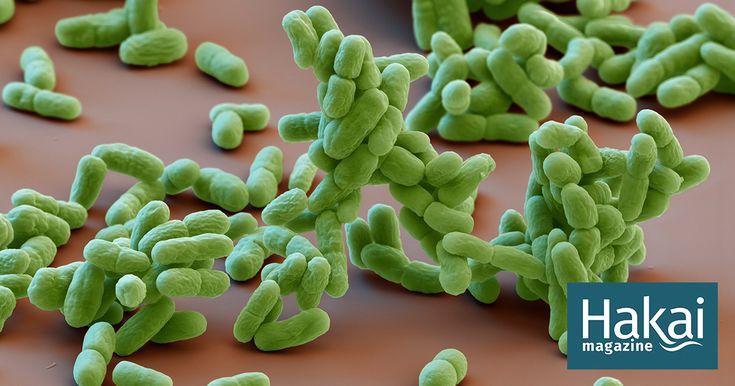
Исследователей особенно интересовала активность гидрохинина в отношении бактерии Pseudomonas aeruginosa , которая вызывает трудноизлечимые инфекции.
P. aeruginosa является одной из основных причин инфекций кровотока и пневмонии, которые приобретаются в больничных условиях. Такие инфекции преимущественно возникают у лиц с низким или ослабленным иммунитетом, в том числе у пациентов с тяжелыми ожогами или муковисцидозом.
По сравнению с другими бактериями P. aeruginosa по своей природе более устойчив к широкому спектру антибиотиков. Более того, появление штамма P. aeruginosa с множественной лекарственной устойчивостью еще больше ограничило терапевтические возможности.
В результате инфекции, вызванные полирезистентными штаммами P. aeruginosa , связаны с высокими показателями заболеваемости и смертности.
Одной из причин более низкой внутренней чувствительности к антибиотикам является то, что клеточная мембрана дикого типа P.
 aeruginosa обладает низкой проницаемостью, что ограничивает способность антибиотиков проникать в бактериальную клетку.
aeruginosa обладает низкой проницаемостью, что ограничивает способность антибиотиков проникать в бактериальную клетку. Внутренняя устойчивость к антибиотикам дикого типа P. aeruginosa также обусловлена экспрессией насосов оттока, которые охватывают внутреннюю и внешнюю клеточные мембраны. Эти насосы для оттока позволяют бактериям, таким как P. aeruginosa , удалять токсичные вещества, такие как антибиотики, которые проникли в клетки.
Сверхэкспрессия этих насосов оттока является основным механизмом возникновения множественной лекарственной устойчивости у этой бактерии . Генетические мутации или перенос генетического материала от других бактерий являются одним из механизмов, которые могут привести к гиперэкспрессии эффлюксных насосов.
Кроме того, воздействие антибиотиков и других токсичных веществ также может привести к адаптивному ответу, включающему активацию этих насосов оттока, что приводит к развитию множественной лекарственной устойчивости.

Чтобы изучить возможность появления новых резистентных штаммов после воздействия лекарств, исследователи также изучили влияние гидрохинина на экспрессию эффлюксных насосов в P. aeruginosa .
В настоящем исследовании исследователи оценили антибактериальные свойства гидрохинина в отношении группы клинически значимых бактерий, включая Staphylococcus aureus , Escherichia coli , Klebsiella pneumoniae , а также чувствительный к антибиотикам и полирезистентный штамм P. aeruginosa .
Используя бактерии, выращенные в лаборатории, исследователи обнаружили, что гидрохинин способен убивать и подавлять рост всех бактериальных штаммов. Однако концентрации гидрохинина, необходимые для уничтожения или подавления роста P. aeruginosa были выше, чем для других бактериальных штаммов.
Чтобы лучше понять механизмы, которые могли бы объяснить более высокую концентрацию гидрохинина, необходимую для проявления его антибактериального действия против P.
 aeruginosa, , исследователи изучили изменения в профиле экспрессии генов штаммов P. aeruginosa после обработки гидрохинином.
aeruginosa, , исследователи изучили изменения в профиле экспрессии генов штаммов P. aeruginosa после обработки гидрохинином.Исследователи обнаружили, что экспрессия генов двух эффлюксных насосов, которые выкачивают из клетки такие вещества, как антибиотики, повышалась в штаммов P. aeruginosa при обработке более низкими концентрациями гидрохинина.
Повышенная регуляция генов насосов оттока предполагает, что обработка гидрохинином вызывала защитный ответ у P. aeruginosa , который мог сделать бактерию менее восприимчивой к этому препарату.
Понимание механизмов, лежащих в основе действия гидрохинина, может помочь в разработке стратегий предотвращения появления новых штаммов бактерий, устойчивых к лекарственным препаратам. Например, гидрохинин можно использовать в сочетании с другими препаратами, например, с теми, которые ингибируют функцию насосов оттока, для лечения инфекций, вызванных P. aeruginosa .
Доктор Болдок сказал: «Мы также рассмотрели реакцию, опосредованную бактериями, обработанными гидрохинином.
 Делая это, возможно, удастся упредить будущие механизмы устойчивости к антибиотикам и сформулировать стратегии или комбинации лекарств, чтобы свести к минимуму риск устойчивости».
Делая это, возможно, удастся упредить будущие механизмы устойчивости к антибиотикам и сформулировать стратегии или комбинации лекарств, чтобы свести к минимуму риск устойчивости».«Важно, что будущие исследования будут направлены на определение эффективности гидрохинина против более широкого спектра микробов, а также на выяснение того, как действует этот препарат. Есть надежда, что с дальнейшими исследованиями и разработками это соединение может помочь в борьбе с трудноизлечимыми бактериальными инфекциями», — добавил он.
Однако мнения о терапевтическом потенциале гидрохинина разделились. Доктор Риете Вентер, адъюнкт-профессор Университета клинических и медицинских наук Южной Австралии, сообщила MNT : «Устойчивость к противомикробным препаратам является проблемой, вызывающей озабоченность во всем мире, поэтому исследования по выявлению соединений с противомикробной активностью являются своевременными и очень важными. Однако гидрохинин лишь незначительно активен против бактериальных патогенов».


 У них гораздо более тонкий слой пептидогликана, поэтому они не сохраняют кристаллический фиолетовый краситель.
У них гораздо более тонкий слой пептидогликана, поэтому они не сохраняют кристаллический фиолетовый краситель.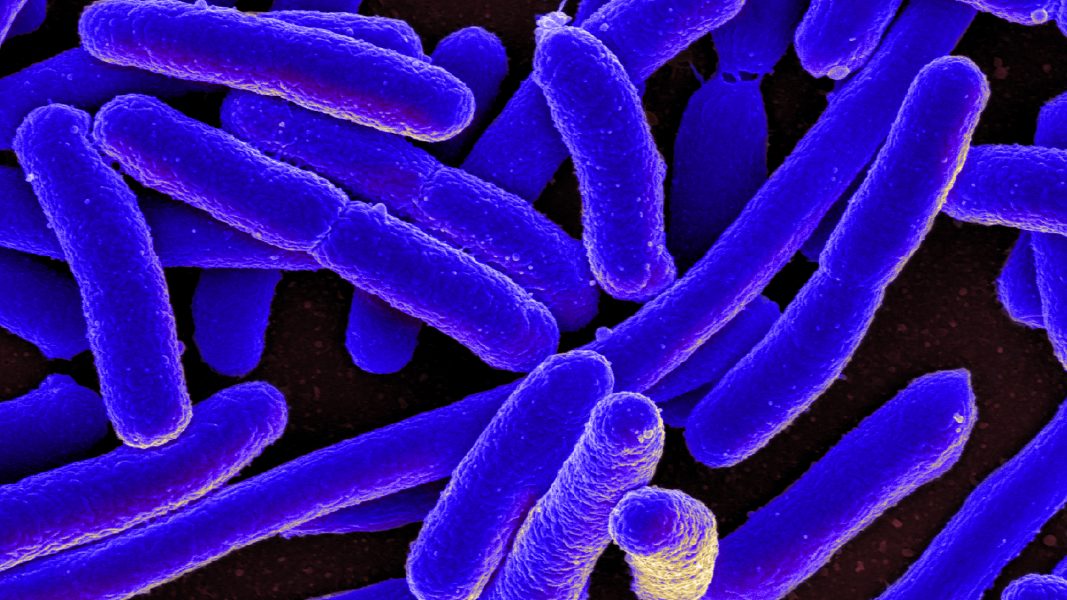
 Они также являются частью нормальной флоры организма, и их можно найти на:
Они также являются частью нормальной флоры организма, и их можно найти на: Они могут вызывать:
Они могут вызывать:

 0060 инфекции, в том числе фарингит и инфекции носовых пазух.
0060 инфекции, в том числе фарингит и инфекции носовых пазух. Однако, если споры присутствуют и выделяют токсины, человеку также может потребоваться лечение антитоксинами. Эта терапия работает путем нейтрализации токсинов, вырабатываемых бактериями.
Однако, если споры присутствуют и выделяют токсины, человеку также может потребоваться лечение антитоксинами. Эта терапия работает путем нейтрализации токсинов, вырабатываемых бактериями. В некоторых случаях врачи могут порекомендовать антитоксиновую терапию.
В некоторых случаях врачи могут порекомендовать антитоксиновую терапию.


 aeruginosa обладает низкой проницаемостью, что ограничивает способность антибиотиков проникать в бактериальную клетку.
aeruginosa обладает низкой проницаемостью, что ограничивает способность антибиотиков проникать в бактериальную клетку. 
 aeruginosa, , исследователи изучили изменения в профиле экспрессии генов штаммов P. aeruginosa после обработки гидрохинином.
aeruginosa, , исследователи изучили изменения в профиле экспрессии генов штаммов P. aeruginosa после обработки гидрохинином. Делая это, возможно, удастся упредить будущие механизмы устойчивости к антибиотикам и сформулировать стратегии или комбинации лекарств, чтобы свести к минимуму риск устойчивости».
Делая это, возможно, удастся упредить будущие механизмы устойчивости к антибиотикам и сформулировать стратегии или комбинации лекарств, чтобы свести к минимуму риск устойчивости».