Содержание
Элизабет пэрриш до и после фото: первый генномодифицированный человек
Содержание
- Миссис Малапроп и леди Макбет
- Вердикт: правда
- Без вердикта
- Эксперимент не по правилам
- Элизабет Пэрриш — первый генно-модифицированный человек (5 фото)
- Элизабет Пэрриш — первый генно-модифицированный человек
- Человек будущего-генетически модифицированный человек?
- Популярные темы:
Миссис Малапроп и леди Макбет
Утверждение: Элизабет Пэрриш — американская певица и актриса
Вердикт: правда
Информации немного, впрочем, как и фильмов, в которых снималась актриса Элизабет Пэрриш. Она появлялась в картинах «Сироты» (1987г.) и «Увидимся утром» (1989г.), а также в сериалах «Закон и порядок» (1990 – 2010гг.), «Кейт и Элли» (1984 –1989гг.), «На пороге ночи» (1956 – 1984гг.) и «Медсестра» (1981 – 1982гг.). Актриса засветилась и на бродвейских подмостках — сыграла в спектаклях «Храните это в семье», «Пиквик», «La Cage aux Folles» и «Смертельная ловушка».
Портал Кинопоиск, посвящённый кинематографу и актёрам, также имеет страницу посвященную актрисе, но без фотографии и не указаны ни дата, ни место рождения.
Впрочем, фото актрисы можно найти на сайте школы актерского мастерства Stella Adler. Там же можно узнать, что Элизабет Пэрриш является мастером-преподавателем в консерватории Стеллы Адлер, а ее главные роли в театре включают миссис Малапроп, леди Макбет, Мэдди Руни и др.
К генной инженерии актриса Элизабет Пэриш не имеет никакого отношения.
1 of 4Элизабет Пэрриш. Кадр из фильма «Сироты» (1987 г.)Элизабет Пэрриш. Скриншот с сайта stellaadler.comЭлизабет Пэрриш. Кадр из сериала «Закон и порядок»Марджи Джиллис, Элизабет Пэрриш в спектакле «Кентавр». (Фото: Адриенн Сюрпренант)
Нулевой пациент
Утверждение: Элизабет Перриш — первый генно-модифицированный человек.
Без вердикта
Элизабет Пэрриш, директор фармацевтической компании BioViva, называет себя «нулевым пациентом», видимо имея в виду, что именно она станет отправной точкой распространения ГМО-пандемии в цивилизованном мире. Это она провела генетический эксперимент сама над собой, в результате которого пресса окрестила её «первым генно-модифицированным человеком». Она не актриса и в этом легко убедиться, посмотрев профайл в Linkedin.
Это она провела генетический эксперимент сама над собой, в результате которого пресса окрестила её «первым генно-модифицированным человеком». Она не актриса и в этом легко убедиться, посмотрев профайл в Linkedin.
Как сообщает официальный сайт компании BioViva, в 2015 году сорокачетырёхлетняя американка решила испытать на себе генную терапию с целью омоложения. Так как в Америке эксперименты на людях запрещены, Элизабет улетела в Колумбию, где получила инъекции двух экспериментальных генных терапий, разработанных её компанией. Первая инъекция вводилась в мышцы ног с целью предотвратить возрастные мышечные истощения.
Со второй инъекцией Элизабет Пэрриш внутривенно получила дозу вирусов, содержащих генетический материал для продуцирования теломеразы, белка, способного удлинить теломеры (боле подробно об эксперименте Пэрриш можно прочитать и )
Для справки: Теломеры — это такие «колпачки» на конце хромосом, которые укорачиваются, когда клетки делятся. Длина теломер у каждого человека индивидуальна. С возрастом длина теломер уменьшается из-за процесса, называемого пределом Хейфлика (число делений клетки). Укорочение теломер приводит к увеличению количества стареющих клеток. Более короткие теломеры также связаны с более высокой вероятностью сердечно-сосудистых заболеваний, диабета 2 типа, хронической обструктивной болезнью легких и некоторых форм деменции.
С возрастом длина теломер уменьшается из-за процесса, называемого пределом Хейфлика (число делений клетки). Укорочение теломер приводит к увеличению количества стареющих клеток. Более короткие теломеры также связаны с более высокой вероятностью сердечно-сосудистых заболеваний, диабета 2 типа, хронической обструктивной болезнью легких и некоторых форм деменции.
Спустя полгода после инъекции, в апреле 2016-го, как сообщается на сайте компании BioViva, длина теломер Элизабет увеличилась на 9%, что, соответствует омоложению примерно на 20 лет.
Однако независимых подтверждений этой информации нет. Эксперимент был проведен не по правилам установленным в научном мире, и его не могут изучить и проверить независимые эксперты-генетики.
Эксперимент не по правилам
Любые клинические испытания должны быть одобрены регулирующими органами и проводиться только после получения соответствующего разрешения. Эксперимент проведенный тайно в неизвестной клинике за пределами страны не считается ценным для учёных мира. Журнал Массачусетского технологического института MIT Technology Review несколько недель сопоставлял факты, провёл целое расследование, но так и не смог 100% подтвердить или опровергнуть заявление Пэрриш.
Журнал Массачусетского технологического института MIT Technology Review несколько недель сопоставлял факты, провёл целое расследование, но так и не смог 100% подтвердить или опровергнуть заявление Пэрриш.
Доказательством того, что медицинская процедура действительно состоялась 15 сентября в Колумбии, служат слова людей связанных с компанией BioViva. Эксперт по геномике Гарвардской медицинской школы Джордж Чёрч и одновременно научный консультант компании Элизабет, сказал журналистам, что тоже хотел бы наверняка знать, что именно произошло в Латинской Америке, но, тем не менее, допускает, что все сказанное Пэрриш вполне реально.
«Были некоторые признаки того, что это может произойти. Компании в скрытом режиме могут делать все, что хотят», — сказал он в интервью MIT Technology Review. По словам Чёрча, студент в его лаборатории вполне может подготовить все для генной терапии над животными, в течение нескольких дней.
Живой научно-популярный журнал Фестиваля Науки «Кот Шрёдингера» попросил учёных — первооткрывателей механизмов клеточного старения прокомментировать поступок Пэрриш. Вот что сказал лауреат Нобелевской премии за открытие теломеразы Джек Шостак: «Я не одобряю подобные трюки. Это совершенно ненаучный подход к сложной проблеме. Его единственная цель — одурачить доверчивых людей и выманить у них деньги на «лекарство», которое может оказаться весьма опасным».
Вот что сказал лауреат Нобелевской премии за открытие теломеразы Джек Шостак: «Я не одобряю подобные трюки. Это совершенно ненаучный подход к сложной проблеме. Его единственная цель — одурачить доверчивых людей и выманить у них деньги на «лекарство», которое может оказаться весьма опасным».
Российский биолог, научный журналист, член Комиссии РАН по борьбе с лженаукой и фальсификацией научных исследований в интервью «Российской газете» сказал следующее:
«Это действительно подозрительная история… На самом деле, никаких независимых исследований, доказывающих, что она это с собой сделала, нет. С другой стороны, нет и особых оснований ей не верить. Потому что сама процедура несложная, и в данном случае её проще сделать, чем соврать… Тут надо отдавать себе отчет, что со стороны Пэрриш это был пиар-ход для инвесторов. Она никому не продавала «лекарство от старости», не утверждала, что оно работает. Её мысль заключалась в том, что нужны инвесторы, которые готовы профинансировать дальнейшие испытания генной терапии на людях… Но сама идея Пэрриш интересная».
Элизабет Пэрриш — первый генно-модифицированный человек (5 фото)
Элизабет Пэрриш — CEO биотехнологической компании BioViva USA Inc. стала первой гено-модифицированной женщиной. Дело в том, что процесс старения организма Элизабет происходит ускоренными темпами. В 2015 году она отправилась в Колумбию чтобы испытать на себе разработку своей компании — две генные терапии.
Первым делом ей ввели в мышцы ног препарат, который должен был остановить возрастную потерю мышечной массы. Вторая терапия — направлена на остановку сокращения длины теломер. Теломеры — это окончания хромосом, их длина уменьшается с возрастом и приводит к росту риска развития онкологических заболеваний, диабета второго типа, некоторых видом деменции и т.д.
Для контроля Элизабет сдала анализ крови и ей замеряли длину теломер лейкоцитов. В 2015 году до начала терапии она составляла 6710 пар оснований, т.е. теломеры 45-летней женщины соответствовали состоянию клеток 60-летнего человека. После введения генного материала в марте 2016 года длина теломер увеличилась до 7330 пар оснований. Практически, это означало, что клетки Пэрриш помолодели на 20 лет.
После введения генного материала в марте 2016 года длина теломер увеличилась до 7330 пар оснований. Практически, это означало, что клетки Пэрриш помолодели на 20 лет.
В 2018 году Элизабет прошла очередное обследование. Оказалось, что у нее увеличилась мышечная масса, уменьшилось количество внутримышечного жира. Причем за три года после терапии изменения сохранялись на хорошем уровне.
Что касается длины теломер, то к 2018 году их длина еще увеличилась до 8120 пар оснований! То есть процесс старения клеток Элизабет не только остановился, но и пошел вспять — клетки омолодились еще на 10 лет.
Правда открытыми остаются вопросы будущих изменений в организме женщины, а также касается ли удлинение теломер только лимфоцитов или и других клеток. Но Пэрриш заявляет, что надеется на положительные результаты и видит своей целью разработку генных препаратов, которые позволят поддерживать состояние людей еще до того, как они превратятся в пациентов.
Элизабет Пэрриш — первый генно-модифицированный человек
Практически всю свою историю человечество искало секрет вечной молодости, первые упоминания о чём-то подобном появляются уже у Геродота, писавшем об источнике вечной молодости где-то в Эфиопии. Наибольшую популярность эта легенда обрела в XVI веке, когда его поисками занимался Хуан Понсе де Леон.
Наибольшую популярность эта легенда обрела в XVI веке, когда его поисками занимался Хуан Понсе де Леон.
Современная же наука подошла к проблеме с другой стороны — со стороны генетики. Для большинства людей генные модификации существуют лишь в фантастических произведениях, но они уже стали реальностью. Знакомься, Элизабет Пэрриш — первый генно-модифицированный человек.
В 2015 году 45-летняя Элизабет, руководитель крупной научно-исследовательской компании BioViva начала курс генной терапии, который должен был замедлить или вовсе остановить процессы старения. В 2018 году первый этап завершился успешно.
Но сначала немного о сути. В 1961 году было установлено, что клетка может делиться определенное количество раз до тех пор, пока ее защитные отростки — теломеры — не достигнут минимальных размеров. Лишаясь защиты, клетка перестает делиться и начинается процесс старения организма.
о есть, чем короче теломеры, тем старее организм, а без них высокий риск повреждения или мутации ядра. Потому Пэрриш решила провести эксперимент по искусственному удлинению теломер. Подопытной стала сама женщина.
Потому Пэрриш решила провести эксперимент по искусственному удлинению теломер. Подопытной стала сама женщина.
Последствия эксперимента предсказать было невозможно, потому Элизабет пришлось записать видеообращение, где она подтвердила свое согласие. Операция прошла в Колумбии, поскольку опыты на людях запрещены в США и еще потому, что некоторые используемые вещества не сертифицированы американской комиссией.
Кроме того, старость не является диагнозом, хотя в международном списке болезней присутствует. А это лишь усложняло получение разрешения.
Непосредственно перед процедурой у Пэрриш взяли кровь, длина ее теломер тогда составляла 6,71 кб, а уже в марте 2016 года — 7,33 кб. В этом году две независимых комиссии подтвердили, что организм Элизабет помолодел на 20 лет, что сказалось и на ее внешности.
«Мы затеяли всё это, чтобы донести до общества, показать: генная терапия для борьбы со старением, для предотвращения опасных возрастных заболеваний уже есть, она работает. Пусть и на одном человеке, но такой пример уже есть.
Пусть и на одном человеке, но такой пример уже есть.
Нельзя закрывать на это глаза, когда население земного шара стареет и сотни тысяч людей каждый день умирают в муках от болезней, которые запускаются из-за дряхления организма», — поделилась Элизабет.
Стоит заметить, что эксперимент еще не окончен. Да, ученым удалось достичь ощутимых результатов, но никто не знает, чего ожидать в долгосрочной перспективе. Но в любом случае, это огромный шаг вперед, хотя мы подозреваем, что больше всего проблем вызовет не разработка новых способов, а противостояние с излишне консервативным населением.
Человек будущего-генетически модифицированный человек?
В будущем богатые люди смогут вносить изменения в макромолекулы, отвечающие за реализацию генетической программы, отмечал ученый в своей последней книге, которая будет опубликована 16 октября.
Английский физик-теоретик Стивен Хокинг, который умер семь месяцев назад в возрасте 76 лет, предсказывал появление в будущем суперлюдей с измененными ДНК, которые могут стать реальной угрозой человечеству. Как пишет в воскресенье газета The Sunday Times, такое опасение Хокинга содержится в его последней книге, которая будет опубликована 16 октября.
Как пишет в воскресенье газета The Sunday Times, такое опасение Хокинга содержится в его последней книге, которая будет опубликована 16 октября.
В своем труде под названием «Короткие ответы на серьезные вопросы» физик предположил, что богатые люди смогут в довольно близкой перспективе вносить изменения в макромолекулы, отвечающие за реализацию генетической программы. Модифицируя свою ДНК и своих детей, они, писал Хокинг, смогли бы улучшить свою память, сопротивляемость болезням, продолжительность жизни и повысить уровень интеллекта.
«Уверен, что в течение этого века люди откроют для себя возможность модифицировать как свои интеллектуальные способности, так и инстинкты, например, агрессию, — пишет ученый в книге, выдержки из которой приводит издание. — Возможно, против генной инженерии на людях будут приняты законы, однако некоторые не смогут побороть искушение улучшить человеческие характеристики, такие как память, сопротивляемость болезням, продолжительность жизни».
Подобное развитие ситуации, опасался ученый, несет в себе риски тем людям, которые не пройдут улучшение на генетическом уровне. «Появление суперлюдей сразу приведет к появлению серьезных политических проблем с неулучшенными людьми, которые не будут в состоянии с ними конкурировать. По-видимому, они вымрут или станут малозначимыми. Вместо этого мы получим расу людей, которые сами себя проектируют, все больше и больше улучшаясь», — предположил физик-теоретик.
«Появление суперлюдей сразу приведет к появлению серьезных политических проблем с неулучшенными людьми, которые не будут в состоянии с ними конкурировать. По-видимому, они вымрут или станут малозначимыми. Вместо этого мы получим расу людей, которые сами себя проектируют, все больше и больше улучшаясь», — предположил физик-теоретик.
Генетически модифицированные люди будут иметь IQ от 1000 и выше
Генетически модифицированные люди могут иметь IQ на уровне 1000 и выше. По крайней мере, согласно научной теории профессора Стивена Хсу.
Хсу можно считать глубоким эрудитом. Его работы касаются квантовой физики, темной энергии, финансов, информационной безопасности, геномики и биоинформатики. Он официально является вице-президентом по научным исследованиям Университета штата Мичиган, где возглавляет кафедру теоретической физики.
Профессор Хсу считает, что изменив геном человека, можно резко повысить его интеллектуальные способности. Подробное описание теории приводится в журнале ArXiv e-prints. Ее популярное изложение дает Nautilus.
Ее популярное изложение дает Nautilus.
Возможность появления сверхразума является прямым результатом генетической основы интеллекта. Такие характеристиками как рост и познавательные способности контролируют тысячи генов, и каждый их них оказывает свое небольшое воздействие, — пишет Хсу.
Опираясь на предыдущие исследования генома, Хсу считает, что с интеллектом связано около 10 000 генетических вариантов. Если путем настройки каждого из них нам удастся получить нужную версию, то, по его словам, мы сможем создать человеческих существ с показателем умственного развития в 100 раз выше среднего. Это соответствует IQ в более чем 1000 баллов.
Хсу является научным консультантом BGI (бывший Пекинский институт геномики), а также одним из основателей его Лаборатории когнитивной геномики. По слухам, которые появились в прошлом году, BGI секвенирует геномы 2000 самых умных людей планеты с целью вывода сверхразумного поколения, которое сможет поднять IQ нации.
Хсу и BGI не единственные, кто прогнозирует появление сверхразума посредством генетических улучшений. В своей недавно опубликованной книге «Superintelligence» директор созданного в Оксфорде Института будущего человечества Ник Бостром соглашается с тем, что генетика является ключом к появлению сверхразумных людей. Генетический скрининг эмбрионов перед имплантацией мог бы помочь родителям найти и выбрать эмбрионы с аллелями, определяющими высокий уровень интеллекта. Бостром надеется, что дальнейшее развитие генной инженерии сделает возможным синтез геномов в спецификацию, что сильно упростит поставленную задачу.
В своей недавно опубликованной книге «Superintelligence» директор созданного в Оксфорде Института будущего человечества Ник Бостром соглашается с тем, что генетика является ключом к появлению сверхразумных людей. Генетический скрининг эмбрионов перед имплантацией мог бы помочь родителям найти и выбрать эмбрионы с аллелями, определяющими высокий уровень интеллекта. Бостром надеется, что дальнейшее развитие генной инженерии сделает возможным синтез геномов в спецификацию, что сильно упростит поставленную задачу.
По словам Бострома, в будущем технология позволит наделять эмбрион предпочтительной комбинацией генов, передаваемых от каждого из родителей, и генов, им не присущих, которыми обладает лишь небольшое количество людей в мире. Такой микс сможет оказать серьезный положительный эффект на познавательные способности детей.
Хсу считает, что таким способом можно развить способности выше, чем у любого из 100 миллиардов человек, когда-либо живших на Земле:
Представьте себе, что способности самых великих умов человечества в своем максимальном виде будут присутствовать у одного индивидуума. Это практически идеальное воспроизведение изображений и речи, сверхбыстрое мышление и расчеты, сильная геометрическая визуализация, даже в более высоких измерениях; способность параллельно и одновременно решать множество аналитических и мыслительных задач. Этот список можно продолжить.
Это практически идеальное воспроизведение изображений и речи, сверхбыстрое мышление и расчеты, сильная геометрическая визуализация, даже в более высоких измерениях; способность параллельно и одновременно решать множество аналитических и мыслительных задач. Этот список можно продолжить.
Перспектива того, что на одной планете с обычными людьми будут жить «сверхчеловеки», чье величие так воспевал философ Фридрих Ницше в своем произведении «Так говорил Заратустра», пугает. Пристального внимания заслуживают соответствующие нравственные вопросы, которые придется решить до того, как такие возможности станут реальностью.
Некоторые страны могут узаконить генную модификацию детей раньше других. Очевидно, что первой доступ к технологии получит элита, которая сможет наделить сверхразумом себя и своих детей. Но будем надеяться, что плодами генной инженерии сможет воспользоваться каждый желающий, иначе нас ждет такое неравенство, которого еще никогда не было в истории человечества.
Какой он, «человек будущего» — генно-модифицированный человек?
Национальная академия наук США заявила, что в ближайшее время приступит к работам по изменению генома человека.
Чем грозит такой научный прорыв?
Наука уже не просто идет семимильными шагами, она передвигается со скоростью времени. Кто бы из нас мог предположить хотя бы 10 лет назад, что скоро появится возможность побороть любую болезнь путем изменения генома человека. Такое можно было увидеть только в фантастических фильмах! — СЕГОДНЯ ЭТО УЖЕ РЕАЛЬНОСТЬ!!!
Многие годы ученые разных стран бились над геномом человека. И вот, 21 мая 2010 года Крейг Вентер, американский ученый, гентик заявил о создании им искусственной клетки. Это был прорыв в генной инженерии. И спустя всего 7 лет, ученые утверждают, что готовы к созданию генетически модифицированного человека.
По утверждению ученых, таким образом они смогут побороть любую болезнь.
В США данные работы стали возможны применительно к людям, больных ВИЧ, онкологическими заболеваниями и болезнью Альцгеймера.
По сообщению Национальной академии наук США, речь о работах по созданию людей с исключительными возможностями, не идет.
Но эксперименты на людях и животных уже идут полным ходом во всем мире:
В Китае, создали генетически модифицированных свиней, внедрив им 3 гена человека. И теперь свиное сердце или легкое можно без опаски отторжения пересаживать человеку
И теперь свиное сердце или легкое можно без опаски отторжения пересаживать человеку
В США и Тайланде уже широко используются генные вакцины – они предотвращают сердечно-сосудистые заболевания и глаукому.
Многие крупные фармацевтические компании начали закрывать проекты по исследованию химических препаратов, перенаправляя средства в генную инженерию.
Какие гены можно внедрить в человека, чтобы сделать его совершенным?
По заявлению ученых, человеческий организм на столько не совершенен, что с помощью генной инженерии человеку могут открыться новые горизонты:
- Ген пятнистой акулы. Иммунитет против всех существующих у человека болезней, в том числе и рака
- Ген сокола-сапсана. Острота зрения человека может увеличится в 15 раз!
- Ген кошки. Расширит диапазон слуха человека в 6 раз (с 10 до 60 Гц)
- Ген бабочки семейства Saturniidae (павлиноглазка), сообщает newsli.ru. Увеличит обоняние человека в 50 раз
- Ген кролика. У человека никогда не будут болеть зубы, и они будут расти всю жизнь
- Ген аквариумной рыбки Danio rerio.
 У человека будут регенерироваться внутренние органы и ткани
У человека будут регенерироваться внутренние органы и ткани - Ген свиньи. Человек сможет испытывать оргазм в течении 30 мин
- Ген черепахи. Человек сможет побороть старость
И многое другое…
Но, как всегда это «палка о двух концах». Ведь этим можно воспользоваться не только для лечения, но и для управления людьми, вживляя им с рождения гены безвольных и слабохарактерных… Склонных к насилию и убийствам… Не ощущающих боли и страха… — УНИВЕРСАЛЬНЫХ СОЛДАТ!
Как будет называться данная особь млекопитающего? – человек ли?
Тем временем:Первый в мире генно-модифицированный человек — Элизабет Пэрриш
Идея вечной молодости или хотя бы более долгой и здоровой жизни волновала человечество на всех этапах развития цивилизации. Ученых всегда интересовала возможность увеличения продолжительности жизни человека, и вот, когда достижения в области правильного питания и активного образа жизни были исчерпаны, они обратили свой взор в сторону генных изменений.
Когда мы видим сюжеты о том, что генетики проводят эксперименты на лабораторных животных, изменяют геном, например, с целью замедлить старение клеток, нам кажется, что все это из области фантастики и отдаленного будущего. Но, оказывается, что фантастика стала реальностью. На Земле уже живет человек с искусственно измененными генами.
Это американка Элизабет Пэрриш, которая согласилась на вмешательство генетиков ради того, чтобы остановить старение своего организма, ну и, разумеется, чтобы принести пользу миру.
На самом деле она еще и является одним из руководителей научно-медицинской компании BioViva, которая и проводит этот смелый эксперимент.
Чтобы понять суть искусственных изменений, необходимо немного осветить проблему старения с точки зрения генетики. Сам процесс старения заложен в нашей ДНК, а начинается он с процесса уменьшения концевых отростков хромосом, так называемых теломер.
Чем старше биологический возраст человека, тем короче его теломеры. В процессе роста клеток происходит деление ДНК, что сопровождается укорачиванием теломер и в конечном итоге приводит к старению и гибели клетки.
В конце 2015 года Элизабет Пэрриш ввели генетический материал, который, проникнув внутрь ядра каждой клетки ее организма, должен был запустить изменения, и способствовать увеличению длины теломер. Таким образом, по предположению ученых, будет остановлен процесс старения и произойдет общее омоложение организма.
Принимая во внимание то, что результаты такого эксперимента могут быть самыми непредсказуемыми, вплоть до летального исхода, Элизабет даже записала обращение, в котором подтверждала свое согласие на инъекцию и озвучила понимание серьезности генетического вмешательства. Для введения генетического материала ей даже пришлось ехать в Колумбию, так как на территории Соединенных Штатов подобные опыты с людьми запрещены законодательно.
И вот ученые уже обнародовали первые результаты эксперимента. Пока все выглядит более чем оптимистично: биологический возраст женщины уменьшился примерно на 20 лет. Это выражается в состоянии лейкоцитов ее крови, а также в теломерах хромосом, которые удлинились, вместо того, чтобы дальше разрушаться.
Во внешности 45 летней женщины также произошли некоторые изменения. Ее кожа стала более упругой и улучшилось состояние волос.
Видео:ГМО мутанты биороботы уже реальность. Люди ИКС не фантастика. Чудеса генетики и генной инженерии
>4 удивительных факта об Элизабет Пэрриш, которая стала первым генетически модифицированным человеком
Бессмертие Элизабет Пэрриш
В сентябре 2015 года Элизабет Пэрриш, директор фармацевтической компании BioViva, первой в мире решилась изменить свои гены, чтобы отсрочить старость. С помощью специального вируса она активировала в организме фермент теломеразу. Он известен тем, что делает клетки человека бессмертными. Есть гипотеза, что таким способом можно продлить молодость, и Элизабет надеется подтвердить это на собственном опыте.
Почему мы стареем?
Со временем большинство клеток изнашивается, и организм стареет. Отчего так происходит, учёные до сих пор не знают. Десятилетиями спорят: мы дряхлеем из-за поломок и механического износа органов или из-за программы старения, включающейся по сигналу из мозга?
Леонард Хейфлик. В 1960-е годы открыл ограничение числа делений у клеток человека: клетки умирают приблизительно после 40–60 делений (предел Хейфлика). Последовательно выступает против терапии старения и продления жизни. Отрицает как желательность, так и возможность антивозрастной медицины.
В 1960-е годы открыл ограничение числа делений у клеток человека: клетки умирают приблизительно после 40–60 делений (предел Хейфлика). Последовательно выступает против терапии старения и продления жизни. Отрицает как желательность, так и возможность антивозрастной медицины.
Но есть и хорошая новость: мы уже знаем, как стареют клетки. Когда они делятся, каждая хромосома теряет небольшой кусок. В новом поколении клеток хромосомы становятся короче. Затем ещё короче. Ещё…
Чтобы новые клетки не страдали, на концах хромосом размещены специальные повторяющиеся фрагменты — теломеры. Они не несут важной информации, поэтому их укорачивание не вредит клеткам. Но неизбежно наступает точка невозврата: примерно после 50 делений теломеры заканчиваются — клетка больше не может делиться и погибает. Это число называется пределом Хейфлика, по фамилии учёного, открывшего этот эффект. Считается, что укорачивание теломер — одна из причин старания людей.
Образ жизни может влиять на длину теломер. Больше всего не повезло курильщикам и людям, которые не занимаются спортом и часто волнуются: у них теломеры короче, чем у тех, кто ведёт здоровую и спокойную жизнь. А вот алкоголики могут вздохнуть спокойно: употребление спиртного никак не отражается на длине теломер. Впрочем, длину измеряли только в лейкоцитах.
Больше всего не повезло курильщикам и людям, которые не занимаются спортом и часто волнуются: у них теломеры короче, чем у тех, кто ведёт здоровую и спокойную жизнь. А вот алкоголики могут вздохнуть спокойно: употребление спиртного никак не отражается на длине теломер. Впрочем, длину измеряли только в лейкоцитах.
Вечно молодые
Некоторым клеткам позарез необходимо быть бессмертными. Например, стволовым — своеобразным поставщикам клеток для всего тела. Стволовая клетка может превратиться в какую угодно. Иными словами, это команда запасных, которые всегда готовы заменить выбывших из строя по причине болезни или травмы. Половым клеткам тоже надо быть бессмертными, ведь они дают начало новому человеку. Во взрослом человеке 37 200 000 000 000 клеток. Чтобы получить такое количество, самой первой оплодотворённой яйцеклетке необходимо поделиться как минимум 45 раз. В принципе, длины теломер должно на это хватить, но как быть с обновлением тканей? И будущими детьми? Получается, чтобы люди росли и растили детей, половым клеткам необходимо решить проблему укорачивания теломер.
Для этого есть специальный фермент теломераза. Она удлиняет теломеры и позволяет клетке делиться бесконечно долго. О том, что такой фермент существует, догадался советский биолог Алексей Оловников ещё в 1973 году. Через 11 лет учёные из Калифорнийского университета в Беркли выделили теломеразу из клеток. И в 2009-м получили за это открытие Нобелевскую премию. Как выразился Леонард Хейфлик, «проницательное предположение Оловникова получило экспериментальное подтверждение».
Иллюстрация: Science Photo Library/East News / Компьютерное изображение хромосом.
Многие россияне обиделись на Нобелевский комитет, хотя сам Алексей Матвеевич не стал комментировать его решение, а некоторое время спустя выдвинул новую теорию, ещё более смелую. Он предположил, что теломеры — лишь немые свидетели старения, а вызывают его другие специальные молекулы ДНК. Их он назвал хрономерами. По версии Оловникова, хрономеры находятся в клетках мозга и постепенно укорачиваются, отсчитывая время нашей жизни. Иными словами, хрономеры — это физическое воплощение биологических часов. Самое же неординарное предположение заключается в том, что на укорачивание хрономер влияет смена фаз Луны, возможно, через её гравитационное поле. Экспериментальных подтверждений этой экстравагантной гипотезы пока нет.
Иными словами, хрономеры — это физическое воплощение биологических часов. Самое же неординарное предположение заключается в том, что на укорачивание хрономер влияет смена фаз Луны, возможно, через её гравитационное поле. Экспериментальных подтверждений этой экстравагантной гипотезы пока нет.
— Эксперты при виде моих гипотез традиционно чешут в затылках, — говорит Алексей Оловников. Но не отчаивается и в статьях заранее благодарит экспериментаторов, которые смогут подтвердить его теорию. Так же как учёные из Калифорнийского университета подтвердили его догадку о существовании теломеразы более 30 лет назад.
В конце XX века выяснилось, что активация теломеразы в отдельных клетках приводит к их бессмертию. Но что значит «активация»? Строго говоря, ген теломеразы есть во всех клетках организма, но они, как правило, не подозревают о его существовании, поскольку ген выключен. В стволовых и половых клетках он, наоборот, включён, и теломераза удлиняет теломеры при малейшей необходимости. Получается, что, искусственно включив этот ген, можно заставить теломеразу работать в любой клетке и фактически обессмертить её. Более того, с помощью определённых вирусов ген теломеразы можно встроить в любую клетку — даже ту, в которой его и в помине не было.
Получается, что, искусственно включив этот ген, можно заставить теломеразу работать в любой клетке и фактически обессмертить её. Более того, с помощью определённых вирусов ген теломеразы можно встроить в любую клетку — даже ту, в которой его и в помине не было.
Это открытие заинтриговало весь мир. У учёных появился инструмент, способный делать клетки бессмертными. Можно ли обессмертить самих людей? Однозначного ответа на этот вопрос до сих пор нет, однако за годы исследований накопилось множество любопытных данных.
Как вырастить мышь-долгожителя
В конце 1990-х биологи вывели генетически модифицированные породы мышей, чтобы детально изучить свойства теломеразы. Грызуны, у которых она от рождения не работала, имели множество проблем с внутренними органами и старели значительно раньше обычных животных. С другой стороны, у них возникало меньше злокачественных опухолей. Другие мыши, которые от рождения имели чрезмерно активную теломеразу, чаще болели раком. И тоже жили меньше обычного. Почему? Дело в том, что раковые клетки научились включать ген теломеразы гораздо раньше учёных и пользуются этим для того, чтобы делиться бесконечно. Таким образом, в организме мыши с выключенной теломеразой раковой опухоли гораздо сложнее появиться, чем у животного с активно работающим ферментом.
Почему? Дело в том, что раковые клетки научились включать ген теломеразы гораздо раньше учёных и пользуются этим для того, чтобы делиться бесконечно. Таким образом, в организме мыши с выключенной теломеразой раковой опухоли гораздо сложнее появиться, чем у животного с активно работающим ферментом.
Ещё один интересный эксперимент провели на породе мышей, от рождения склонных к раку: опухоли вырастают у них очень легко, почти не встречая сопротивления со стороны организма. Биологи отключили у этих мышек теломеразу в надежде, что они будут меньше болеть раком. Результат оказался противоположным: без фермента грызуны покрылись опухолями значительно раньше, чем их сородичи.
Фото: Depositphotos / Эксперименты на мышах показали действенность терапии теломеразой.
Не совсем понятно, почему это происходит. Одна из версий заключается в том, что, если теломераза не работает, стволовые клетки теряют свои теломеры и стареют. А ведь из стволовых получаются клетки иммунной системы, наши главные защитники от опухолей. Из старых стволовых клеток борцы с раком выходят так себе.
Из старых стволовых клеток борцы с раком выходят так себе.
Другая версия состоит в том, что, как только молекулы ДНК лишаются теломер и оголяют свои концы, клетка хочет как-нибудь их соединить. Но склеивать случайные молекулы ДНК — не самая лучшая идея, это приводит к мутациям и повышает вероятность рака.
Что будет с человеком, если отключить его теломеразу? Такой эксперимент, понятное дело, не поставишь, но можно изучить болезни, связанные с неправильной работой фермента. Одна из них называется врождённый дискератоз. Он проявляется в преждевременном старении: у больных рано седеют волосы и выпадают зубы, они часто болеют раком и редко доживают до 50 лет.
Омолодить старика
Чтобы понять, может ли включение теломеразы повернуть старение вспять, понадобились специальные мыши. Они были устроены хитрым образом: учёные выключили их ген теломеразы, но его можно было включить, скормив зверькам особое вещество. Изначально эти мышки быстро старели: у них раньше, чем у обычных особей, появлялись старческие нарушения работы семенников, селезёнки, кишечника и мозга, ухудшалось обоняние. Включение теломеразы омолодило животных: их внутренние органы стали лучше работать, мыши начали точнее распознавать запахи.
Включение теломеразы омолодило животных: их внутренние органы стали лучше работать, мыши начали точнее распознавать запахи.
BioViva — американская фармацевтическая компания, основанная в 2015 году. Разрабатывает и патентует методы генной терапии. Два основных проекта — генная конструкция с теломеразой и конструкция с ингибитором миостатина (белок, вызывающий атрофию мышц, — Элизабет вколола себе и её). Клинические испытания, подтверждающие безопасность этих методов, не проводились.
Укол вирусом делали в некой лаборатории за пределами США, её название не сообщают. Длину теломер измеряла независимая компания SpectraCell в Техасе. В крови содержится много разных клеток с разной длиной теломер, этим объясняется большая погрешность их измерения. Использовали ослабленный вирус AAV (аденоассоциированный вирус), предварительно вставив в него ген теломеразы. Вирус внедряется в 19-ю хромосому в клетках крови, и в результате в них постоянно экспрессируется теломераза.
Наиболее впечатляющие результаты получили в 2012 году учёные из Испанского национального центра по исследованию рака. Они экспериментировали на самых обыкновенных мышах. Особи были двух возрастов: взрослые, то есть те, кому исполнился год, и престарелые, двухлетние. Исследователи заразили грызунов вирусом, который активирует теломеразу. В результате престарелые мыши стали жить на 13 % дольше, а взрослые — аж на 24 %. Что примечательно, заболеваемость раком не выросла.
Сорокачетырёхлетняя американка Элизабет Пэрриш решила повторить этот опыт на себе. Как сообщает официальный сайт компании BioViva, в апреле 2016-го, спустя полгода после инъекции вирусом, длина теломер Элизабет увеличилась на 9 %, что соответствует омоложению тканей на 20 лет. Звучит ободряюще, однако вряд ли стоит воспринимать этот результат как доказательство молодильной силы теломеразы. Во-первых, измерение длины теломер имеет большую погрешность — целых 8 %. Во-вторых, тестирование настоящих лекарств — процесс более сложный. Как минимум необходимы контрольная группа и большое количество испытуемых. Об этом нам рассказала Мария Бласко, руководитель группы испанских учёных, поставивших исходный эксперимент с активацией теломеразы:
Во-вторых, тестирование настоящих лекарств — процесс более сложный. Как минимум необходимы контрольная группа и большое количество испытуемых. Об этом нам рассказала Мария Бласко, руководитель группы испанских учёных, поставивших исходный эксперимент с активацией теломеразы:
— Любая новая терапия, генная в том числе, должна быть одобрена регулирующими органами и получить соответствующие разрешения для проведения клинических испытаний. Ведь клинические исследования должны гарантировать пациентам безопасность и максимальный шанс на успех. Наша группа проверяет терапию теломеразой на мышиных моделях, чтобы потом провести валидные клинические испытания и достоверно оценить пользу для пациентов.
«Кот Шрёдингера» попросил учёных — первооткрывателей механизмов клеточного старения прокомментировать поступок Пэрриш. Вот что сказал лауреат Нобелевской премии за открытие теломеразы Джек Шостак:
— Я не одобряю подобные трюки. Это совершенно ненаучный подход к сложной проблеме. Его единственная цель — одурачить доверчивых людей и выманить у них деньги на «лекарство», которое может оказаться весьма опасным.
Леонард Хейфлик к поступку Элизабет тоже отнёсся без энтузиазма:
— Я не поддерживаю опыты на себе в отсутствие рациональных объяснений. С древнейших времён люди экспериментируют, пытаясь отсрочить старость. Но по разным причинам успеха пока никто не достиг. Более того, у нас нет средства для определения эффекта. Люди веками считают, что их знаний по биологии достаточно, чтобы понять, как победить старение. Но поскольку этот процесс — результат второго закона термодинамики, вероятность успешного вмешательства близка к нулю. Всё во Вселенной стареет.
Фото: Depositphotos / Мезенхимальные стволовые клетки.
Хейфлик добавил, что не понимает саму идею поиска вечной молодости:
— Я бы не хотел, чтобы тираны, диктаторы и убийцы жили дольше.
А вот Алексей Оловников говорит об Элизабет менее категорично:
— Я восхищён её мужеством. В поступке Пэрриш есть две составляющие: смелость и желание пропиарить свою фирму BioViva.
Так или иначе, сама возмутительница спокойствия настроена решительно. Она планирует запатентовать свой метод омоложения, а пока путешествует по миру в поисках фирмы, которая согласится провести настоящие клинические исследования. Этим летом она побывала в Москве, где провела пресс-конференцию. Элизабет сообщила, что своим экспериментом хотела ускорить проведение клинических испытаний антивозрастной генной терапии. По её словам, учёные уже нашли способ продлить молодость, и она не видит смысла скрывать его.
Она планирует запатентовать свой метод омоложения, а пока путешествует по миру в поисках фирмы, которая согласится провести настоящие клинические исследования. Этим летом она побывала в Москве, где провела пресс-конференцию. Элизабет сообщила, что своим экспериментом хотела ускорить проведение клинических испытаний антивозрастной генной терапии. По её словам, учёные уже нашли способ продлить молодость, и она не видит смысла скрывать его.
Иллюстрация: Depositphotos / Схематичное изображение двойных спиралей ДНК.
Но на самом деле учёные пока боятся повторить этот опыт на людях и спорят о том, может ли вообще активация теломеразы продлить жизнь. Энтузиасты считают этот фермент настоящим эликсиром молодости, ведь если результаты эксперимента будут такими же, как на мышах, люди будут жить на 18 лет дольше. Скептики опасаются раковых опухолей и других побочных эффектов. Они сравнивают активацию теломеразы с окрашиванием седых волос, имея в виду, что, даже если теломеры удлинятся, это не обязательно устранит причину старения клеток. Да и означает ли омоложение клеток омоложение организма как суммы этих клеток? Со временем мы узнаем ответы на все эти вопросы, а пока нам остаётся самое интересное: искать их.
Да и означает ли омоложение клеток омоложение организма как суммы этих клеток? Со временем мы узнаем ответы на все эти вопросы, а пока нам остаётся самое интересное: искать их.
Мышам продлили жизнь с помощью назальной генной терапии
Биология
На мышах
Сложность
3.4
Jaijyan et al. / PNAS, 2022
Жизнь мыши можно увеличить на треть или даже больше, если раз в месяц вводить в ее организм вирусный вектор с дополнительным геном. Это продемонстрировала группа исследователей, связанная с компанией BioViva — ее основательница Элизабет Пэрриш когда-то утверждала, что проверила похожую методику на себе самой. В новом эксперименте выяснилось, что для генной терапии подходит теломераза или фоллистатин, а сам препарат работает, даже если распылять его в носу. Статья опубликована в журнале Proceedings of the National Academy of Sciences.
В новом эксперименте выяснилось, что для генной терапии подходит теломераза или фоллистатин, а сам препарат работает, даже если распылять его в носу. Статья опубликована в журнале Proceedings of the National Academy of Sciences.
В 2015 году Элизабет Пэрриш (Elizabeth Parrish) заявила, что получила инъекцию аденовирусного вектора с геном теломеразы — фермента, который занимается удлинением ДНК. Считается, что укорочение теломер (концевых участков хромосом) может быть одной из причин старения, и Пэрриш таким образом предполагала если не продлить себе жизнь, то хотя бы снизить биологический возраст.
Стала ли Пэрриш на самом деле здоровее, неизвестно. Позже она утверждала, что ее теломеры действительно удлинились — однако другой информации о ее здоровье нет, да и эта получена вне рамок научного эксперимента. Поначалу Пэрриш собиралась продавать такую генную терапию старения с помощью своей компании BioViva, научным консультантом которой стал в том числе известный генетик Джордж Чёрч (George Church).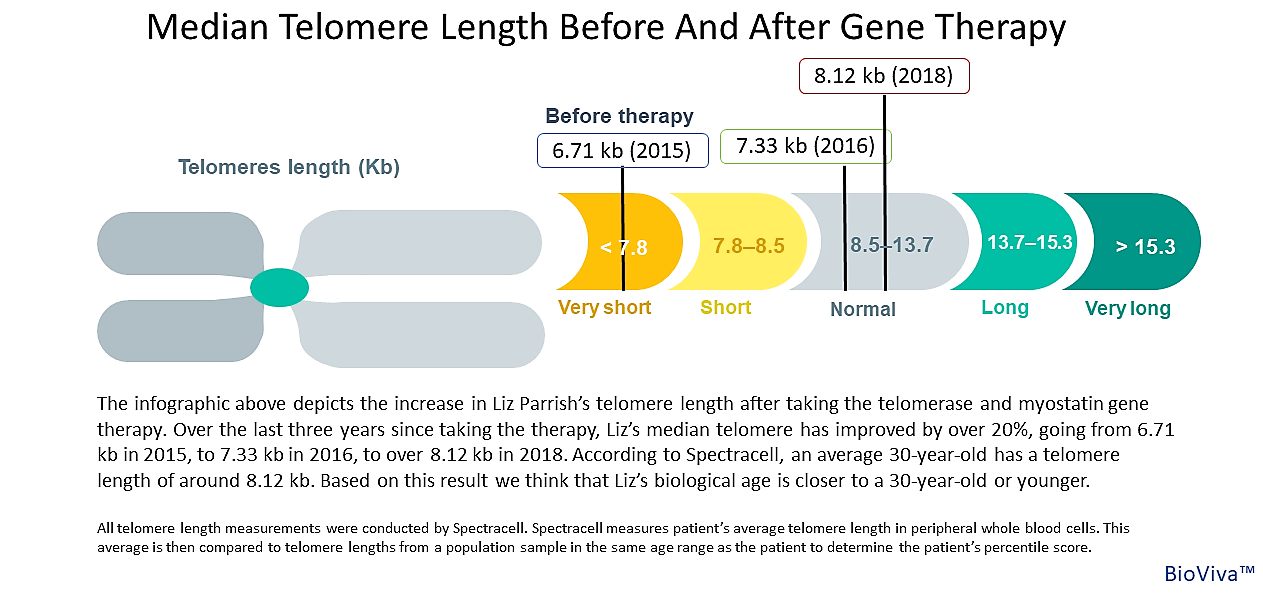 Однако до сих пор у компании не было крупных экспериментальных публикаций по этой теме, а на сайте предлагается купить только тесты для определения биологического возраста.
Однако до сих пор у компании не было крупных экспериментальных публикаций по этой теме, а на сайте предлагается купить только тесты для определения биологического возраста.
Теперь у BioViva вышло большое исследование, руководителями которого значатся сама Пэрриш, а также ее научные консультанты: Джордж Черч и Хуа Чжу (Hua Zhu). В этой работе ученые опробовали на мышах два вида генной терапии. В первом случае мышам добавляли ген теломеразы — по предыдущим работам уже известно, что такая терапия может сделать их жизнь дольше. Во втором случае — ген фоллистатина: это молекула-ингибитор многих сигнальных веществ, в том числе миостатина, который тормозит рост мышц. В ранних исследованиях фоллистатин помог мышам нарастить мышечную массу, но влияние на продолжительность жизни в них не подсчитывали.
В качестве средства доставки авторы работы использовали вирусные векторы на основе цитомегаловируса — поскольку они довольно крупные (а значит, могут вместить большие гены), не встраиваются в геном человека и, как известно по клиническим испытаниям других препаратов, не вызывают побочных эффектов. При этом они попробовали вводить вирусные векторы двумя путями: классическим, интраперитонеально (укол в брюшину), и интраназально (распыляя в виде спрея в носу). Всего, таким образом, получилось семь групп животных: контрольная группа получила укол без вакцины, еще две — укол или спрей «пустого» вектора, две — укол или спрей с геном теломеразы и две — укол или спрей с геном фоллистатина.
При этом они попробовали вводить вирусные векторы двумя путями: классическим, интраперитонеально (укол в брюшину), и интраназально (распыляя в виде спрея в носу). Всего, таким образом, получилось семь групп животных: контрольная группа получила укол без вакцины, еще две — укол или спрей «пустого» вектора, две — укол или спрей с геном теломеразы и две — укол или спрей с геном фоллистатина.
Всех мышей начинали «лечить», когда им было 18 месяцев — по мнению авторов статьи, это соответствует 56 годам у людей. Они получали по одной дозе в месяц до 29 месяцев (около 80 «человеческих» лет) — к этому моменту все животные в контрольных группах умерли. Но в 32 месяца ученые решили продолжить терапию, чтобы выяснить, как она влияет на максимальную продолжительность жизни.
A — кривые выживаемости мышей. Mock — «пустой» укол, WT — «пустой» вектор, TERT — ген теломеразы, FST — ген фоллистатина, IP — укол в брюшину, IN — спрей в нос. В — сравнение возраста мышей в эксперименте и человека
Jaijyan et al. / PNAS, 2022
/ PNAS, 2022
Поделиться
Оказалось, что оба гена в составе вирусных векторов позволяют мышам прожить существенно дольше, чем в контроле: фоллистатин — на 32,5 процента в среднем, теломераза — на 41,4 процента. А максимальная продолжительность жизни составила около 37 месяцев для фоллистатина и 40 месяцев для теломеразы. При этом метод введения на длину жизни практически не повлиял.
Ученые проверили, действительно ли при этом изменяются концентрации соответствующих белков. И заметили, что они растут и в крови, и в тканях — но в разных тканях по-разному. Возможно, это связано с тем, что вирусный вектор неравномерно распределяется по организму или не везде может проникнуть. Длина теломер при этом выросла во всех исследованных тканях и практически достигла уровня, характерного для молодой 8-месячной мыши.
D — концентрация фоллистатина в крови после введения вектора, E — относительное увеличение (по сравнению с общим уровнем РНК в клетке) работы генов фоллистатина (синий) и теломеразы (зеленый) в разных тканях
Jaijyan et al. / PNAS, 2022
/ PNAS, 2022
Поделиться
Кроме того, исследователи обнаружили, что после генной терапии мыши лучше сохраняют вес и меньше лысеют, чем обычные пожилые животные. И у них ниже уровень глюкозы в крови — то есть меньше предрасположенность к диабету, который часто развивается с возрастом. И во всех этих случаях способ введения снова не играл роли.
B — изменение веса тела экспериментальных мышей с возрастом (красной стрелкой отмечено прекращение терапии, зеленой — возобновление). E — изменение концентрации глюкозы в крови после приема сладкой пищи
Jaijyan et al. / PNAS, 2022
Поделиться
Не все эти результаты оказались для авторов работы неожиданностью. Например, они уже знали, что мышиный цитомегаловирус хорошо заселяет организм при введении через нос — поэтому несложно объяснить, что оба метода введения вектора сработали одинаково. Но они не ожидали, что и фоллистатин, и теломераза окажут сходное влияние на уровень глюкозы в крови — поскольку здесь механизмы их действия совсем не совпадают.
Но они не ожидали, что и фоллистатин, и теломераза окажут сходное влияние на уровень глюкозы в крови — поскольку здесь механизмы их действия совсем не совпадают.
Исследователи полагают, что такую генную терапию можно будет испытать как средство от разных возрастных болезней. Но прежде чем переходить от мышей к людям, нужно будет проверить, не потеряет ли этот метод в эффективности. Неизвестно, хорошо ли человеческий цитомегаловирус будет проникать через слизистую носа, и сможет ли вектор добраться в разные ткани. Кроме того, у человека теломеры гораздо короче, чем у мыши, и уровень экспрессии собственной теломеразы гораздо ниже, поэтому и здесь эффект может оказаться другим.
Авторы статьи рассчитывают также, что в дальнейшем с помощью цитомегаловирусного вектора можно будет доставлять несколько генов сразу, например, теломеразу и фоллистатин одновременно. Этот подход уже использовали их коллеги: мы раньше рассказывали о том, как геронтологи вылечили мышей от возрастных болезней с помощью двух генов и продлили жизнь мухам — с помощью коктейля из трех.
Полина Лосева
Читайте также
Физики научились лучше видеть сквозь муть
Разделение на этапы при ударе о воду оказалось важным свойством игры в «блинчики»
Бывшие игроки в регби столкнулись с высоким риском болезни двигательного нейрона и деменции
Туманные модели
Как физики, медики и климатологи описывают аэрозоли
Может ли эта женщина вылечить старение с помощью генной терапии? | Старение
Элизабет Пэрриш — генеральный директор BioViva, биотехнологической компании из Сиэтла, работающей над разработкой методов лечения, замедляющих процесс старения. В апреле компания сообщила, что сама Пэрриш прошла «первую успешную генную терапию против старения человека». Лечение, как утверждалось, изменило биологический возраст ее иммунных клеток на 20 лет.
«Есть много фантастических выводов, к которым [люди] могут прийти, — говорит Пэрриш, — победить смерть, или люди становятся бессмертными, или что-то в этом роде. То, что мы пытаемся сделать, это затронуть самую большую точку страданий в промышленно развитом мире прямо сейчас, а именно болезни старения».
В сентябре 2015 года Пэрриш, которому тогда было 44 года, вылетел в Колумбию, чтобы пройти два экспериментальных курса генной терапии. Одним из них был ингибитор миостатина, препарат, который проходит испытания в качестве средства для лечения потери мышечной массы. Другим была генная терапия теломеразой — препарат, который, как утверждает BioViva, изменил биологический возраст ее клеток, удлинив части ее генетического материала, называемые теломерами.
Гены содержатся в скрученных молекулах ДНК, называемых хромосомами. На концах этих хромосом находятся участки ДНК, называемые теломерами. Теломеры защищают важный генетический материал от повреждений, которые могут привести к болезнетворным нарушениям или гибели клеток. Теломеры также позволяют клетке и ее ДНК делиться, но по мере деления клетки часть теломер теряется до тех пор, пока после конечного числа делений клетка не умирает, что может способствовать процессу старения человека.
Теломеры также позволяют клетке и ее ДНК делиться, но по мере деления клетки часть теломер теряется до тех пор, пока после конечного числа делений клетка не умирает, что может способствовать процессу старения человека.
Если у кошки девять жизней, то у делящейся человеческой клетки их примерно от 50 до 70 – если, как предполагается, вы не удлините теломеры, чтобы увеличить продолжительность жизни клетки и повысить ее способность противостоять повреждениям. Генная терапия, которую получил Пэрриш, предназначена именно для этого, побуждая клетку производить теломеразу, белок, который восстанавливает теломеры.
Посмотрите интервью с Элизабет Пэрриш из BioViva.
Лечение вызывает большие споры. Поскольку BioViva не провела необходимую доклиническую работу для перехода к исследованиям на людях, Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США не санкционировало эксперимент Пэрриш — отсюда и ее поездка в неназванную клинику в Колумбии.
Компания BioViva утверждает, что через шесть месяцев после лечения теломеры в лейкоцитах Пэрриша удлинились на 9%. Это заявление было встречено смесью насмешек и недоверия со стороны многих ученых, которые ссылались на отсутствие надлежащей научной процедуры. «Мы использовали стороннее тестирование для всего», — утверждает Пэрриш. «Мы использовали стандартную систему тестирования теломер, которую продают врачи, а пациенты могут купить через Интернет. Этот тест показал, что мои теломеры в моих [белых кровяных тельцах] удлинились на 20 лет».
Это заявление было встречено смесью насмешек и недоверия со стороны многих ученых, которые ссылались на отсутствие надлежащей научной процедуры. «Мы использовали стороннее тестирование для всего», — утверждает Пэрриш. «Мы использовали стандартную систему тестирования теломер, которую продают врачи, а пациенты могут купить через Интернет. Этот тест показал, что мои теломеры в моих [белых кровяных тельцах] удлинились на 20 лет».
Скептицизм ученых выходит за рамки надежности систем тестирования компании. На своем веб-сайте BioViva утверждает, что ее работа основывается на работе Марии Бласко, директора Испанского национального центра исследования рака. В исследовании 2012 года результаты Бласко показали, что аналогичная генная терапия теломеразой может увеличить среднюю продолжительность жизни мышей примерно на 20%. С тех пор ее работа была сосредоточена на оценке того, может ли эта технология улучшить результаты у мышей с заболеваниями сердца и крови, возникающими из-за очень коротких теломер.
Бласко не связана с работой BioViva и не имеет никакого отношения ни к компании, ни к Пэрришу. «Клиническая проверка нашей стратегии генной терапии теломеразой, как и любых других методов лечения, должна быть достигнута посредством тщательных испытаний, подтвержденных и поддержанных регулирующими органами», — говорит она.
Мы должны быть в состоянии сказать: Это не убивает мышей, это не убивает человеческие клетки – давайте просто проведем тест
Элизабет Пэрриш
В профиле своей компании Пэрриш описывает себя как «гуманитарного работника, предпринимателя и новатора». » и «ведущий голос в области генетического лечения». В этом списке отсутствует слово «ученый». Она также называет себя «нулевым пациентом» для этих методов лечения — термин, с которым некоторые могут не согласиться. «Нулевой пациент» обычно используется для описания первого пациента во время вспышки инфекционного заболевания, а не первого пациента, получившего лечение. Некоторые утверждают, что лучшим описанием будет то, что ее исследование было n = 1 (исследование только на одном человеке).
Некоторые утверждают, что лучшим описанием будет то, что ее исследование было n = 1 (исследование только на одном человеке).
«Возможно, она нулевой пациент, но только для распространения лженауки, которая вырастет из ее истории», — говорит Тимоти Колфилд, профессор юридического факультета и Школы общественного здравоохранения Университета Альберты. Колфилд обеспокоен тем, что работе Пэрриша не хватает научной строгости и существует риск того, что ее подхватят недобросовестные специалисты, знающие о том, что антивозрастные средства продают больше. «Люди забывают, что большинство клинических испытаний не увенчались успехом, — говорит он. «Лекарства часто выглядят многообещающе на мышах, но не работают на людях — это другие животные».
Но Пэрриш, которая говорит, что к ней уже обращались люди, чтобы спросить, могут ли они попробовать ее омолаживающую генную терапию, утверждает, что было проведено достаточно исследований на животных, чтобы перейти на людей. «Я думаю, что мы делаем что-то неправильно. Мы должны быть в состоянии сказать: «Это выглядит многообещающе, это не убивает мышей, это не убивает человеческие клетки». Итак, что мы сказали [когда решили протестировать методы лечения ее компании]: «Давайте просто проведем тест; давайте посмотрим, безопасно ли это».
Мы должны быть в состоянии сказать: «Это выглядит многообещающе, это не убивает мышей, это не убивает человеческие клетки». Итак, что мы сказали [когда решили протестировать методы лечения ее компании]: «Давайте просто проведем тест; давайте посмотрим, безопасно ли это».
Пэрриш и ее команда планируют изучить влияние генной терапии на другие клетки ее тела и оценить эффект лечения потери мышечной массы. Между тем, они хотят протестировать лечение на большем количестве людей, но сначала им нужно найти страну с менее строгими требованиями, чем в США. «Мы все еще ищем более быстрый маршрут, — говорит Пэрриш. «Мы ездили из страны в страну с группами, которые просили эти страны изменить регулирование. Они придут с новыми нормативными стандартами… с быстрым путем, чтобы как можно быстрее предоставить людям наиболее жизненно важные терапевтические средства».
Хотя Колфилд признает, что процесс разработки лекарств является строгим, он утверждает, что это необходимо для поддержания научной строгости. «Конечно, мы все ищем способы быстрее доставить эффективные лекарства в клиники, но эта идея покупать за границей до тех пор, пока вы не найдете нормативно-правовую базу, которая наиболее дружелюбна к вашей идее о том, как следует заниматься наукой, является ужасной ошибкой», — сказал он. говорит. «Хорошая наука должна быть универсальной».
«Конечно, мы все ищем способы быстрее доставить эффективные лекарства в клиники, но эта идея покупать за границей до тех пор, пока вы не найдете нормативно-правовую базу, которая наиболее дружелюбна к вашей идее о том, как следует заниматься наукой, является ужасной ошибкой», — сказал он. говорит. «Хорошая наука должна быть универсальной».
Быстро дистанцироваться от BioViva был Джордж М. Мартин, профессор патологии Вашингтонского университета. Мартин согласился быть советником компании после того, как Пэрриш посетил его университет, но отказался от этой роли, узнав об эксперименте Пэрриша над собой. «Я ушел в отставку всего через несколько недель после того, как принял приглашение, я никогда не присутствовал на заседании совета директоров и, конечно же, не имел ни малейшего представления о ее планах проводить вмешательства на людях без какой-либо доклинической работы», — говорит он.
Джордж Черч, профессор генетики Гарвардской медицинской школы и еще один советник BioViva, с опаской относится к мысли, что у него есть «связи» с компанией. «Я бы не назвал их галстуками, — говорит он. «Я консультирую людей, которым нужен совет, и они явно нуждаются в совете». Черч говорит, что посоветовал компании пройти через надлежащие регулирующие каналы и провести необходимую доклиническую работу. «Если вы просто позволяете людям бегать без каких-либо советов, особенно если они не имеют подготовки в области медицинских исследований, то вы навлекаете последствия».
«Я бы не назвал их галстуками, — говорит он. «Я консультирую людей, которым нужен совет, и они явно нуждаются в совете». Черч говорит, что посоветовал компании пройти через надлежащие регулирующие каналы и провести необходимую доклиническую работу. «Если вы просто позволяете людям бегать без каких-либо советов, особенно если они не имеют подготовки в области медицинских исследований, то вы навлекаете последствия».
Он отмечает, что этот момент был трагически отмечен испытанием генной терапии во Франции, которое, как считается, вызвало рак у двух участников в 2003 году, и смертью в 1999 году Джесси Гелсингера, первого человека, умершего в ходе клинических испытаний. для терапии. Обе неудачи, по его словам, отбросили назад всю отрасль. «С тех пор область значительно улучшилась и стала намного безопаснее, но новые лекарства должны тестироваться в плацебо-контролируемых испытаниях, сначала на животных».
И не только ученые с осторожностью относятся к передовым методам лечения, таким как генная терапия или те, которые используют стволовые клетки. Общественность и политики, чье отношение может либо помочь, либо помешать потенциальным достижениям медицины, также нервничают по поводу науки, которая возится с внутренней работой жизни. Если споры вокруг нового мощного инструмента для редактирования генома Crispr/Cas9, что угодно, подход Пэрриша к борьбе со старением не будет развернут без тщательного изучения.
Общественность и политики, чье отношение может либо помочь, либо помешать потенциальным достижениям медицины, также нервничают по поводу науки, которая возится с внутренней работой жизни. Если споры вокруг нового мощного инструмента для редактирования генома Crispr/Cas9, что угодно, подход Пэрриша к борьбе со старением не будет развернут без тщательного изучения.
Дункан Бэрд — профессор онкологии и генетики в Медицинской школе Университета Кардиффа. Он призывает с осторожностью относиться к нетерпеливому подходу Пэрриша к поиску методов лечения. «Жизнь и старение слишком сложны с биологической точки зрения, чтобы сводить все к этим объектам на концах хромосом [теломерах]», — говорит он. «Выбрать одно конкретное явление длины теломер в качестве ключевого фактора старения и сказать, что если вы собираетесь удлинить теломеры, вы волшебным образом излечите старение, я думаю, это фантастично».
Без более глубокого понимания биологических процессов, лежащих в основе старения, такое вмешательство может быть опасным, говорит Бэрд. По его словам, одна из причин, по которой теломеры стали такой длины, заключается в том, чтобы ограничить количество раз, когда клетка может пролиферировать, и, таким образом, ограничить ее способность быть раковой. «Вмешательство в фундаментально важный механизм подавления опухоли, который развился у долгоживущих видов, таких как наш, не кажется мне особенно хорошей идеей».
По его словам, одна из причин, по которой теломеры стали такой длины, заключается в том, чтобы ограничить количество раз, когда клетка может пролиферировать, и, таким образом, ограничить ее способность быть раковой. «Вмешательство в фундаментально важный механизм подавления опухоли, который развился у долгоживущих видов, таких как наш, не кажется мне особенно хорошей идеей».
Попытки бороться со старением и его многочисленными проявлениями принадлежат не только Пэрришу. По всему миру группы преданных своему делу исследователей проводят кропотливую и тщательную работу, необходимую для того, чтобы разгадать биологические тайны старения и, возможно, однажды выяснить, как с этим бороться. Но, как это часто бывает в науке, кажется, что успех может заключаться в том, что Пэрриш отказывается принять: в самом времени.
Лиз Пэрриш хочет жить вечно
Информационный бюллетень Outside по электронной почте включает в себя наши самые сильные тексты, самые амбициозные репортажи и отмеченные наградами рассказы о природе.
Зарегистрироваться Сегодня.
Она прилетела рано утром в понедельник, не сказав ни мужу, ни детям, куда она идет и что делает. Когда она приземлилась в Боготе, было уже поздно. Небо было туманным и темным, воздух на удивление прохладным, на дорогах многолюдно и хаотично.
Хозяева приготовили постель в их квартире, но она не могла заснуть. Два препарата генной терапии, которые ей предстояло получить на следующий день, — в десятках флаконов, упакованных в сухой лед, — только что прибыли из США, и все допоздна говорили о том, как они могут изменить ход истории. Когда они отвезли ее в клинику во вторник утром, она смотрела в окно и пыталась отключиться от мира, а затем сгорбилась над своим телефоном и написала своим детям: «Я люблю вас». Мало кто из участников эксперимента, если таковые вообще были, знали, что она мать.
В исследованиях, которые она читала, и на видео, которые она видела, мыши, получившие лечение, которое она собиралась получить, перерождались, их шерсть блестела, а мышцы напрягались. Изменение произошло почти мгновенно — вопрос дней, недель.
Изменение произошло почти мгновенно — вопрос дней, недель.
Но лабораторные мыши отличаются от людей. Она знала, что бесчисленные лекарства, которые действуют на них, ничего не делают для нас. «Я надеялась на магию, — говорит она. «Конечно, был». Она представила иглы, пронзающие ее кожу, часы, внезапно вращающиеся в обратном направлении, разрушительное воздействие времени, погоды и невзгод, видимо, исчезнувшее. Она подумала о том, что все это может когда-нибудь означать для нее и всех остальных: конец смерти.
Комната в клинике была чистой и просторной. Там была кровать и справа от нее капельница, а также была зона для переодевания, где она надела белое платье с голубым узором из атомных частиц. На видео процедуры, которое она согласилась показать мне почти три года спустя, ее длинные волосы рассыпались по подушке, когда она ложилась. Она пыталась поднять настроение, рассказывая анекдоты, то же самое, что она делала во время рождения двух своих детей. Остальные в палате — врач, медсестра и двое мужчин с видеокамерами — захихикали. Потом начали втыкать иглы.
Потом начали втыкать иглы.
За период, который длился глубокой ночью, было сделано более 100 инъекций в трицепсы, бедра, ягодицы и даже в лицо, чуть ниже щеки. Темп был мучительно медленным. «Значит, ты говоришь, что это все равно попадет в мои органы, верно?» — спросила она у доктора, когда он ввел иглу ей под коленную чашечку. Так и будет, заверил он ее.
Некоторые флаконы все еще были заморожены, и доктор вытаскивал их один за другим, баюкая в руках, пока они не оттаяли. — Готов к этому? — спросил он, когда она перевернулась, чтобы обнажить лопатки. Она обняла подушку. — Поторопись, — засмеялась она. «Я не могу дождаться, чтобы сделать это».
После полуночи ей сделали последнюю инъекцию. Она была голодна, ей не до шуток, и она не знала, что будет дальше. Это было 16 сентября 2015 года, и была составлена странная история болезни: в ходе непроверенной процедуры, которая нарушила бы федеральные правила США, Элизабет Пэрриш, здоровая 44-летняя женщина с острова Бейнбридж, штат Вашингтон, основатель из небольшого биотехнологического стартапа под названием BioViva, получила, по ее мнению, более мощную дозу генной терапии, чем любой другой человек. Она сделала это, чтобы бороться с тем, что она называла «болезнью» старения. По ее собственным словам, она была нулевой пациенткой в поисках радикального увеличения продолжительности жизни.
Она сделала это, чтобы бороться с тем, что она называла «болезнью» старения. По ее собственным словам, она была нулевой пациенткой в поисках радикального увеличения продолжительности жизни.
Пэрриш в Вашингтоне (Энни Мари Массельман)
Два дня спустя, после наблюдения за ее лихорадкой или рвотой, врач решил, что она может безопасно летать. Пэрриш, высокий блондин скандинавского происхождения, надел хирургическую маску в аэропорт и отправился домой. Даже тогда она не рассказала своей семье, что она сделала, позволив им поверить, что это была просто очередная поездка по ее новому делу. «Я не хотела, чтобы мой муж нервничал, и я не хотела, чтобы он нервировал меня», — говорит она. «Мне просто нужно, чтобы все было нормально». Когда позже я спросил, могу ли я взять интервью у ее мужа, она попросила, чтобы я этого не делал. «Я бы очень хотела, чтобы моя семья не вмешивалась в это», — сказала она. Это было частью привычки: она предпочитала, чтобы я никогда не приходил к ней домой, поэтому мы разговаривали по телефону или встречались в соседних кафе. Она попросила меня запланировать интервью через дополнительный офис BioViva в Лондоне. Она не особенно привыкла к тому, что люди обращают на нее внимание — и теперь, после того, как она генетически модифицировала себя, они обращали на нее больше внимания, чем когда-либо. Этот осмотр заставил ее чувствовать себя неловко.
Она попросила меня запланировать интервью через дополнительный офис BioViva в Лондоне. Она не особенно привыкла к тому, что люди обращают на нее внимание — и теперь, после того, как она генетически модифицировала себя, они обращали на нее больше внимания, чем когда-либо. Этот осмотр заставил ее чувствовать себя неловко.
Через две недели после Боготы, когда компания Пэрриш выпустила пресс-релиз об эксперименте, в нем не было видно, что она была подопытным кроликом. «BioViva лечит первого пациента с помощью генной терапии, чтобы обратить старение вспять», — говорится в сообщении. «Субъект чувствует себя хорошо и возобновил обычную деятельность». Она сделала все возможное, чтобы сделать именно это. Она читала книги, писала электронные письма, стирала, готовила ужин, гуляла с собакой в лесу и водила детей в школу. Она мало тренировалась — не больше, чем обычно, и меньше, чем могли бы порекомендовать врачи. Она вела журнал. Она посмотрела в зеркало. Она ждала, что что-то произойдет. Каждый день в течение нескольких месяцев она фотографировала свое лицо, но если и были какие-то изменения, то не могла их увидеть.
Каждый день в течение нескольких месяцев она фотографировала свое лицо, но если и были какие-то изменения, то не могла их увидеть.
До одного дождливого январского утра 2013 года, менее чем за три года до того, как она стала нулевой пациенткой, Пэрриш, по ее словам, была «почти нормальной», просто обычной мамой и частично занятой домохозяйкой. В тот день она высадила мужа на паромном терминале Бейнбридж-Айленд, через залив от Сиэтла. Затем она повела своего девятилетнего сына на прием к врачу. Мальчик часто вставал ночью, чтобы сходить в туалет, и она и ее муж заметили, что он все худеет. В клинике врач проверил его кровь, проверил мочу, а затем серьезно посмотрел на Пэрриша. «Вам нужно ехать прямо в отделение неотложной помощи», — сказал он. «У него диабет 1 типа». Тип 1, когда-то известный как юношеский диабет, представляет собой хроническое заболевание, при котором поджелудочная железа не может вырабатывать инсулин, гормон, который позволяет сахару проникать в клетки и снабжать их энергией. Чтобы ребенок остался живым и здоровым, новая реальность — это жизнь с тщательно контролируемым уровнем сахара в крови и, в некоторых случаях, с бесконечными инъекциями.
Чтобы ребенок остался живым и здоровым, новая реальность — это жизнь с тщательно контролируемым уровнем сахара в крови и, в некоторых случаях, с бесконечными инъекциями.
Пэрриш набрала номер своего мужа и передала трубку доктору, не в силах сообщить новости сама. Сын умолял отпустить его домой. Вместо этого они поехали прямо к парому и поехали по неспокойным водам залива Эллиотт, ошеломленно наблюдая, как перед ними возвышается центр Сиэтла. Ее муж ждал возле паромного причала; вместе они помчались в детскую больницу Сиэтла.
Подобные вещи не должны были случиться с ее детьми. «Я был очень нервным родителем, — говорит Пэрриш. До того, как семья переехала на лесистый остров Бейнбридж, когда дети были маленькими и жили в Сиэтле, она превратила свой дом в местную тусовку — отчасти для того, чтобы они не терялись из виду. Футбол был разрешен, но она не позволяла им заниматься более рискованными видами деятельности, такими как сплав по реке или скалолазание. И все же ничто из этого не помогло ее сыну.
Детская больница Сиэтла раскинулась на 25 акрах в богатой северной части города. Он неизменно входит в число лучших педиатрических учреждений США, а его 403 койки заняты самыми нуждающимися в стране детьми — детьми с раком, сердечными заболеваниями, неврологическими расстройствами, повреждениями головного мозга. Медсестры и врачи провели для Пэрриш и ее мужа многодневный ускоренный курс лечения диабета. Они заверили ее, что у ее сына заболевание поддается лечению. «Я не могу сказать достаточно хороших слов о Children’s, — говорит Пэрриш. Но опыт современной американской медицины также разозлил ее.
В пресс-релизе не сообщалось, что Пэрриш был подопытным кроликом эксперимента. «BioViva лечит первого пациента с помощью генной терапии, чтобы остановить старение», — говорится в сообщении. «Субъект чувствует себя хорошо и возобновил обычную деятельность».
Еще до того, как ее сыну поставили диагноз, Пэрриш одержимо читала медицинские новости и научные журналы, а также страницу в Facebook I F#ing Love Science, отслеживая клинические исследования, как некоторые люди следят за спортом. Работая с людьми, которых она встретила в Интернете, она основала некоммерческую группу Stem Cell Voice, чтобы информировать общественность о стволовых клетках и, в конечном итоге, подтолкнуть регулирующие органы к более быстрому внедрению на практике изменяющих жизнь методов лечения. Состояние ее сына побудило Пэрриш взглянуть глубже, и ее обеспокоил разрыв связи. Казалось, что наука ускоряется — мы расшифровали геном человека, клонировали человеческие стволовые клетки и начали выращивать замещающие органы, — но медицина стояла на месте, думала она, сдерживаемая чрезмерно рьяным Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов, которое потребовало многих лет испытаний и сотен миллионов исследований. долларов на исследования и разработки, прежде чем новые методы лечения были одобрены. Теперь, когда ее сын лежал на больничной койке, задержки были личными.
Работая с людьми, которых она встретила в Интернете, она основала некоммерческую группу Stem Cell Voice, чтобы информировать общественность о стволовых клетках и, в конечном итоге, подтолкнуть регулирующие органы к более быстрому внедрению на практике изменяющих жизнь методов лечения. Состояние ее сына побудило Пэрриш взглянуть глубже, и ее обеспокоил разрыв связи. Казалось, что наука ускоряется — мы расшифровали геном человека, клонировали человеческие стволовые клетки и начали выращивать замещающие органы, — но медицина стояла на месте, думала она, сдерживаемая чрезмерно рьяным Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов, которое потребовало многих лет испытаний и сотен миллионов исследований. долларов на исследования и разработки, прежде чем новые методы лечения были одобрены. Теперь, когда ее сын лежал на больничной койке, задержки были личными.
«Почему бы нам не создать биобанк его поджелудочной железы?» — спросила она медсестру своего сына. Она полагала, что часть его можно сохранить, заморозить и дождаться будущего, когда его можно будет реконструировать для повторного производства инсулина. Разве они не знали, что теперь возможно со стволовыми клетками?
Она полагала, что часть его можно сохранить, заморозить и дождаться будущего, когда его можно будет реконструировать для повторного производства инсулина. Разве они не знали, что теперь возможно со стволовыми клетками?
– Оглянитесь, – сказала медсестра, пытаясь дать Пэрришу хоть какую-то перспективу. Ее сын выживет. На многих окружающих кроватях лежали дети, которые этого не хотели. «Но это было еще более неприемлемо, — говорит Пэрриш. «Я просто помню, как был так зол, так зол, что дети умирали».
Семья отправилась домой в Бейнбридж, а Пэрриш ушел в темное место. Она представила своего сына мертвым. Она представила себе его похороны. Она представила свою смерть. Она попыталась медитировать, но вместо этого увидела, как спускается вниз и находит его тело, снова и снова прокручивая образ его мертвого.
Вскоре ее сын вернулся в школу, а муж — на работу, а Пэрриш вышла в интернет, направив свою безотлагательность на поиски лекарств. Она ездила на медицинские конференции, где останавливала исследователей в холлах вопросом: «Может ли это помочь детям?» она спросила. «Как это может помочь детям?»
«Как это может помочь детям?»
В сентябре 2013 года Пэрриш прилетел в Кембридж, Англия, на шестую раз в два года конференцию Фонда SENS. SENS, что расшифровывается как «Стратегии искусственного незначительного старения», возглавляет самое узнаваемое лицо антивозрастного движения Обри де Грей, любитель пива с длинной взлохмаченной бородой. Де Грей, сыгравший главную роль в документальном фильме 2014 года под названием « Бессмертники, », имеет опыт работы в области компьютерных наук и биологии, и он использует унаследованные деньги, а также пожертвования титанов Кремниевой долины, таких как Питер Тиль, для финансирования тщательных исследований старения. Конференция привлекает исследователей, философов и ученых, таких как Джордж Черч, знаменитый генетик из Гарварда. Все участники собираются вместе в общежитиях Квинс-колледжа.
Пэрриш, одна из примерно 200 присутствующих, мчалась за экспертами, когда они закончили свои выступления, засыпая их вопросами, обсуждая будущее генетики с Черчем, чьи проекты в Гарварде включают попытку воскресить шерстистого мамонта путем клонирования, прежде чем она действительно даже знал, кто он такой. Она смотрела презентации об ограничении калорий, редактировании генов и регенерации тканей и слышала, как один за другим лектор упоминал что-то, называемое теломерами — крошечные кусочки генетического материала, описываемые как внутренние часы организма. Люди здесь открыто мечтали о бессмертном будущем, о лекарствах от всех болезней, и когда Пэрриш задала свой обычный вопрос исследователям, занимающимся борьбой со старением, некоторые, казалось, ответили: «Да, эта наука 9».0097 может помочь детям. Конечно, мог. Исцеление от смерти поможет всем. «Что вам нужно?» она спросила. Им нужно было больше денег.
Она смотрела презентации об ограничении калорий, редактировании генов и регенерации тканей и слышала, как один за другим лектор упоминал что-то, называемое теломерами — крошечные кусочки генетического материала, описываемые как внутренние часы организма. Люди здесь открыто мечтали о бессмертном будущем, о лекарствах от всех болезней, и когда Пэрриш задала свой обычный вопрос исследователям, занимающимся борьбой со старением, некоторые, казалось, ответили: «Да, эта наука 9».0097 может помочь детям. Конечно, мог. Исцеление от смерти поможет всем. «Что вам нужно?» она спросила. Им нужно было больше денег.
С деньгами легко, подумал Пэрриш. Она помогала своему мужу в семейном бизнесе по разработке программного обеспечения и наблюдала, как другие технологические компании внедряют его. Финансирование этого исследования казалось гораздо более важным, чем создание приложения. Хотя у нее не было нужных степеней и она никогда не запускала стартап, она отчаянно нуждалась в лекарствах. У нее был ум для науки. Она знала, что может очаровывать людей. Она решила создать компанию.
У нее был ум для науки. Она знала, что может очаровывать людей. Она решила создать компанию.
Сам того не осознавая, Пэрриш опередил Силиконовую долину и ее новых миллиардеров среднего возраста, в том числе основателей Google Сергея Брина и Ларри Пейджа. Менее чем через две недели после SENS 6 Google запустила устройство для продления жизни под названием Calico, вложив в него 1,5 миллиарда долларов. Год спустя управляющий хедж-фондом Джун Юн учредил премию Palo Alto Longevity Prize в размере 1 миллиона долларов. В 2016 году стартап Ambrosia из Bay Area начал предлагать лечение парабиоза — переливание крови пожилых людей с кровью подростков и молодых людей — по цене 8000 долларов за литр. В прошлом году новый Фонд долголетия Силиконовой долины, возглавляемый 23-летней Лаурой Деминг, быстро собрал 22 миллиона долларов, а компания Unity Biotechnology в районе залива Сан-Франциско, целью которой является извлечение умирающих клеток из организма до того, как они смогут накопиться, завершила сбор средств в размере 151 доллар. миллионный раунд финансирования от таких людей, как Тиль и основатель Amazon Джефф Безос. Долина нашла новую проблему для взлома. Если тело было машиной, смерть была просто инженерным вызовом.
миллионный раунд финансирования от таких людей, как Тиль и основатель Amazon Джефф Безос. Долина нашла новую проблему для взлома. Если тело было машиной, смерть была просто инженерным вызовом.
Другой участник конференции из SENS 6 сказал Пэрриш, что ей действительно нужно с кем-то встретиться. Его звали Билл Эндрюс. Он был ультрамарафонцем, микробиологом и ведущим экспертом по теломерам — возможно, единственным человеком в мире борьбы со старением со статусом де Грея, с которым он сыграет в фильме «: Бессмертники». Пэрриш позвонила Эндрюс почти сразу же, как вернулась домой из Кембриджа. Она не помнит подробностей их первого разговора, только то, что у него были ответы. «Мы действительно поладили, — сказала она мне. «Мы говорили, говорили и говорили».
Для Билла Эндрюса, которому сейчас 66 лет, поиски начались в 1962 году, когда ему было десять лет. Он был во дворе своего дома в Южной Калифорнии и смотрел на ночное небо через подержанный телескоп — его рождественский подарок — с восьмидюймовым рефлектором. Отец Эндрюса, такой же высокий и задумчивый, как и он сам, заметил большой интерес сына к науке. «Он вышел на лужайку перед домом, — вспоминает Эндрюс, — и сказал: «Билл, когда ты вырастешь, ты должен стать врачом и найти лекарство от старения». Я не знаю, почему никто этого не сделал». Эндрюс никогда не забывал слова своего отца. «Я планирую жить вечно», — пишет он в своей новой книге «9 лет».0097 Удлинение теломер. «Многие люди утверждают, что старение — это то, что мы можем делать изящно. Это не. Старение — одна из худших вещей, которые могут случиться с человеком».
Отец Эндрюса, такой же высокий и задумчивый, как и он сам, заметил большой интерес сына к науке. «Он вышел на лужайку перед домом, — вспоминает Эндрюс, — и сказал: «Билл, когда ты вырастешь, ты должен стать врачом и найти лекарство от старения». Я не знаю, почему никто этого не сделал». Эндрюс никогда не забывал слова своего отца. «Я планирую жить вечно», — пишет он в своей новой книге «9 лет».0097 Удлинение теломер. «Многие люди утверждают, что старение — это то, что мы можем делать изящно. Это не. Старение — одна из худших вещей, которые могут случиться с человеком».
Иллюстрация теломер на кончиках человеческих хромосом (Hybrid Medical/Science Source)
Еще до того, как Эндрюс поступил в колледж и задолго до того, как он получил докторскую степень. по молекулярной биологии в Университете Джорджии он поставил под сомнение господствующие теории о старении. «Раньше все думали, что мы стареем из-за воздействия окружающей среды», — говорит он, и все согласны с тем, что мы просто ломаемся, «как старые грузовики в поле». Но это казалось неправильным. Почему люди, живущие в высоких широтах, стареют с той же скоростью, что и люди на экваторе? Почему собаки и кошки стареют с разной скоростью?
Но это казалось неправильным. Почему люди, живущие в высоких широтах, стареют с той же скоростью, что и люди на экваторе? Почему собаки и кошки стареют с разной скоростью?
«Я думал, что внутри нас должны быть часы, которые тикают, и это единственный способ объяснить старение», — говорит он. Эндрюсу было за сорок, когда он услышал о концепции, которая имела смысл. В 1993 году в калифорнийском отеле недалеко от озера Тахо он присутствовал на выступлении Кэлвина Харли, в то время главного научного сотрудника корпорации Geron, название которой происходит от геронтологии, науки о старении, и с благоговением слушал, как Харли доказывал, что повторяющиеся Последовательности ДНК, называемые теломерами, служат клеточными часами организма. После этого Эндрюс выбежал вперед и попросил у Харли работу. Он получил это.
Теломеры расположены на концах хромосом внутри ядер клеток человека. Всякий раз, когда клетка делится и ее ДНК реплицируется, теломеры становятся все короче, сжимаются и сжимаются, пока они почти не истощаются, и клетки больше не могут делиться.
Теломеры и теломераза, фермент, который их удлиняет, были открыты в конце 1970-х и начале 1980-х годов учеными Элизабет Блэкберн, Кэрол Грейдер и Джеком Шостаком. Они совершили независимый прорыв, изучая прудовую пену и дрожжевые клетки, и их работа оказалась настолько значимой для других организмов, что в 2009 году они получили Нобелевскую премию..
В компании Geron Эндрюсу и его команде было поручено найти ген человеческой теломеразы, который теоретически мог бы производить фермент и помогать восстанавливать истощенные теломеры. Они искали контрольные последовательности в раковых клетках, затем Эндрюс использовал написанную им компьютерную программу для анализа структур многообещающих кандидатов. Чуть более чем за три месяца они нашли правильный ген: TRC3, позднее переименованный в TERC, или компонент теломеразной РНК. Год спустя они открыли важнейший белковый компонент, hTERT, или обратную транскриптазу теломеразы человека. Они начали тестировать его в чашках Петри, наблюдая за бесконечным делением нормальных клеток. Они проверили отключение hTERT в раковых клетках, остановку производства теломеразы, уничтожение раковых клеток за счет ускорения их старения. Вскоре исследователи Geron выращивали человеческую кожу из клеток старых людей на спинах лабораторных мышей, затем обрабатывали ткань теломеразой и наблюдали исчезновение морщин, волдырей и возрастных пятен.
Они проверили отключение hTERT в раковых клетках, остановку производства теломеразы, уничтожение раковых клеток за счет ускорения их старения. Вскоре исследователи Geron выращивали человеческую кожу из клеток старых людей на спинах лабораторных мышей, затем обрабатывали ткань теломеразой и наблюдали исчезновение морщин, волдырей и возрастных пятен.
В 1995 году компания Geron опубликовала информацию об открытии теломеразы в престижном журнале Science. Он подал множество патентных заявок, некоторые из них в партнерстве с Университетом Колорадо. Компания думала, что у нее могут быть два прорыва: лекарство от рака, которое будет включать ингибирование теломеразы в раковых клетках, и лекарство от старения, которое потребует добавления или индуцирования ее в здоровых. Сначала он решил сосредоточиться на раке.
«Это просто потрясло меня, — говорит Эндрюс. «Люди искали что-то, что могло бы вылечить старение с незапамятных времен, и это было самым близким».
Эндрюс покинул Geron и в 1999 году основал Sierra Sciences, биотехнологическую компанию, полностью сосредоточенную на проблемах старения. Спонсируемый пятью крупными инвесторами, он начал искать фармацевтическое решение — по сути, теломерное лекарство. К середине 2000-х годов с десятками сотрудников и ежемесячным бюджетом в миллион долларов они определили более 900 химических веществ, которые в значительной степени индуцировали теломеразу. Бессмертие казалось совсем рядом. Затем разразился финансовый кризис 2008 года, и финансирование иссякло.
Спонсируемый пятью крупными инвесторами, он начал искать фармацевтическое решение — по сути, теломерное лекарство. К середине 2000-х годов с десятками сотрудников и ежемесячным бюджетом в миллион долларов они определили более 900 химических веществ, которые в значительной степени индуцировали теломеразу. Бессмертие казалось совсем рядом. Затем разразился финансовый кризис 2008 года, и финансирование иссякло.
К 2013 году, когда Лиз Пэрриш позвонила Эндрюсу, Sierra Sciences работала примерно на 100 000 долларов в месяц, удерживаясь на плаву в основном за счет интеллектуальной собственности, которую она предоставила по лицензии другим компаниям. До тех пор, пока Эндрюс не сможет снова собрать серьезные деньги, теломерный препарат, одобренный Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA), нигде не появится. Когда Пэрриш позвонил, ему был 61 год, на полвека больше, чем когда он впервые решил вылечить старение, и часы все еще тикали.
Есть интересная запись первых разговоров Пэрриш и Эндрюс: недолговечный подкаст, который Пэрриш запустила, когда основала предшествовавшую BioViva компанию, которую она назвала BioTrove Investments. Они вдвоем обсуждают основы теломеразы, hTERT и концепцию, называемую пределом Хейфлика, научный принцип, установленный в 1961 году Леонардом Хейфликом, профессором медицинской микробиологии, и его коллегой Полом Мурхедом.
Они вдвоем обсуждают основы теломеразы, hTERT и концепцию, называемую пределом Хейфлика, научный принцип, установленный в 1961 году Леонардом Хейфликом, профессором медицинской микробиологии, и его коллегой Полом Мурхедом.
«Многие люди утверждают, что старение — это то, что мы можем сделать изящно, — пишет Билл Эндрюс в своей новой книге «Удлинение теломер». — Это не так. Старение — одна из худших вещей, которые могут случиться с человеком».
До этого считалось, что человеческие клетки функционируют как бактерии — что они могут делиться вечно. Хейфлик доказал, что это неправда. Он заметил, что человеческие клетки в чашке Петри могут делиться конечное количество раз, около 50, прежде чем остановятся и войдут в своего рода зомби-состояние, известное как старение. Клетки молодого человека в целом могут удваиваться дольше, чем клетки пожилого человека.
«Каким-то образом клетки знают, сколько им лет», — говорит Эндрюс в подкасте. «Число дивизий выравнивается. Это предел Хейфлика. Теперь известно, что это вызвано укорочением теломер». Пэрриш спрашивает, как теломераза влияет на предел Хейфлика. «Ну, — отвечает Эндрюс, повышая голос, — это стирает его».
Это предел Хейфлика. Теперь известно, что это вызвано укорочением теломер». Пэрриш спрашивает, как теломераза влияет на предел Хейфлика. «Ну, — отвечает Эндрюс, повышая голос, — это стирает его».
Билл Эндрюс (слева) и Обри де Грей (Майлин Холлеро)
Далее Эндрюс говорит, что генная терапия — это самый простой способ обойти ограничения, но FDA вряд ли одобрит такое лечение, потому что старение не классифицируется как болезнь. Он предупреждает, что последствия активации теломеразы во всех клетках неизвестны, и что генная терапия — это серьезное обязательство — вы не можете просто отменить ее. «Возможно, это нормально», — говорит он. — Мы просто еще не знаем.
Он также упоминает исследование 2010 года под руководством Рональда ДеПиньо из Гарвардского университета, в котором результатом включения гена теломеразы у лабораторных мышей стало видимое и резкое возвращение молодости. «То, действительно ли это обращение старения вспять, требует дополнительных исследований», — заключает он. «Но это определенно выглядело хорошо. Я бы точно хотел быть одной из этих мышей».
«Но это определенно выглядело хорошо. Я бы точно хотел быть одной из этих мышей».
Пэрриш смеется. Возможно, она уже знает, что Эндрюс согласится создать часть ее генной терапии. — Да, — говорит она. — Я думаю, мы бы все это сделали.
За шесть месяцев до Боготы, в марте 2015 года, Пэрриш впервые появилась на публике в качестве генерального директора BioViva. Местом действия был бизнес-парк в Скоттсдейле, штат Аризона, который служит местом встречи People Unlimited, самопровозглашенной «образовательной, общественной и общественной организации для людей, увлеченных неограниченной продолжительностью жизни». Это была дружная толпа из нескольких десятков человек, многие из которых были постарше, и они были особенно открыты для послания Пэрриша.
Группа, три лидера которой ранее руководили организацией под названием «Фонд Вечного огня», только что потеряла одного из них, проповедника по имени Чарльз Пол Браун, который начал собирать свою паству в 1960-х годах после того, как пережил то, что он назвал «Крещением». плоти» и якобы стать бессмертным. Аколиты платили тысячи долларов в год, чтобы учиться у него, его жены Бернадин и их друга и делового партнера Джеймса Строула. Но Браун страдал болезнью Паркинсона и болезнью сердца и умер в возрасте 79 лет.. Представитель People Unlimited признал, что Браун на самом деле не практиковал то, что проповедовал — во-первых, он недостаточно тренировался, — и Строул и Бернадин продолжили, пытаясь вдохновить паству без него.
плоти» и якобы стать бессмертным. Аколиты платили тысячи долларов в год, чтобы учиться у него, его жены Бернадин и их друга и делового партнера Джеймса Строула. Но Браун страдал болезнью Паркинсона и болезнью сердца и умер в возрасте 79 лет.. Представитель People Unlimited признал, что Браун на самом деле не практиковал то, что проповедовал — во-первых, он недостаточно тренировался, — и Строул и Бернадин продолжили, пытаясь вдохновить паству без него.
Пэрриш вышла на сцену People Unlimited в блузке с воротником и черном блейзере, найдя свое место между маленьким роялем и беспорядком других музыкальных инструментов. Она всегда ненавидела публичные выступления. Но теперь она становилась другим человеком.
«Причина, по которой я занялась этим, заключалась в том, чтобы вылечить детскую болезнь», — сказала она. «Никогда не думал, что буду говорить о долголетии. Но когда я начал изучать науку, я начал понимать, что пришло время вести новую войну — первую войну стариков. Излечивая старение, мы можем помочь многим болезням, которые есть у детей».
С удивительной беглостью она пробежалась по истории смертности. Когда-то люди умирали в основном от инфекционных заболеваний. Затем мы разработали антибиотики. Сейчас мы умираем в основном от болезней старения — рака, сердечных заболеваний, болезни Альцгеймера. По ее словам, нам необходимо разработать новый вид прорывной технологии. Нам нужна генная терапия.
На экране за ее спиной появился логотип. «Это моя компания, BioViva, — сказала она. Она величественно распахнула объятия, широко улыбнулась, а затем хихикнула. «Мы хотим изменить все».
Чтобы получить разрешение правительства США «предоставить вам генную терапию, — продолжал Пэрриш, — мне пришлось бы собрать почти миллиард долларов. На испытания уйдет около 15 лет. И когда я смотрю туда, я вижу людей, которые не хотят ждать 15 лет». Толпа начала аплодировать, и Пэрриш подхватил это. «Как мы на самом деле изменим эту парадигму? Ну, что мы делаем, так это сжигаем и сравниваем все с землей. И мы начинаем сначала». Люди улюлюкали и аплодировали.
Люди улюлюкали и аплодировали.
В США, продолжила она, биоэтика «ведется примерно так: врач не причинит вреда, и все же врач пропишет вам каждое лекарство. Они наложат линии на ваше тело. Они будут держать вас в живых до тех пор, пока вы совершенно не сможете больше оставаться в живых, а затем они отпустят вас и будут чувствовать, что проделали хорошую работу. Я хочу изменить это. Я хочу сказать, что их эксперимент фактически провалился. Теперь мы перейдем к тому, что они считают экспериментальной медициной».
К моменту выступления в Скоттсдейле Пэрриш уже звонила инвестору за инвестором, наконец найдя того, кто мог предоставить 250 000 долларов, необходимых для оплаты эксперимента по генной терапии в Боготе. Она уже знала, что подопытным будет она.
Она также собрала команду врачей и ученых в BioViva, в том числе рентгенолога по имени Джейсон Уильямс, который стал главным врачом компании. Уильямс был примечателен по двум причинам. Во-первых, Пэрриш понял, что у него есть опыт использования генной терапии, предназначенной для подавления белка миостатина, который регулирует рост мышц. (Эксперименты с ингибированием миостатина привели к появлению в Университете Джонса Хопкинса комично разорванных «могучих мышей», а также к рождению примерно в 2000 году в Берлине очень крепкого мальчика, которого врачи назвали Суперребенком.) Во-вторых, он недавно открыл клинику в Боготе. после столкновения с FDA из-за неутвержденного лечения стволовыми клетками, которое он проводил в Алабаме.
(Эксперименты с ингибированием миостатина привели к появлению в Университете Джонса Хопкинса комично разорванных «могучих мышей», а также к рождению примерно в 2000 году в Берлине очень крепкого мальчика, которого врачи назвали Суперребенком.) Во-вторых, он недавно открыл клинику в Боготе. после столкновения с FDA из-за неутвержденного лечения стволовыми клетками, которое он проводил в Алабаме.
Одной из первых вещей, которые предпримет BioViva, станет «совершенно особенная генная терапия», — сказал Пэрриш аудитории People Unlimited. «Это особенное, потому что это единственная генная терапия, которая действительно обращает старение у животных. Он обращал старение в каждую ткань человека, к которой применялся». Она снова улыбнулась. «Это наша самая большая надежда. Почему его никогда не применяли в человеческом теле, я понятия не имею. Наверное, поэтому я и пришел». Толпа снова зааплодировала. — Спасибо, спасибо, — сказала она.
Как Пэрриш знал, Строул и Бернадин планировали что-то большое на 2016 год: собрание в Южной Калифорнии, которое они назвали RAADfest — Фестиваль революции против старения и смерти, — который объединил бы истинных сторонников People Unlimited с более научным набором SENS. 6.
6.
«Я так понимаю, мы встретимся в 2016 году», — сказал Пэрриш собравшимся в People Unlimited. «Моя компания сделает все возможное, чтобы получить результаты изменения возраста к тому времени, когда мы встретимся».
Случилось так, что новости о генной терапии Пэрриша появились еще до RAADfest. В конце 2015 года Антонио Регаладо, репортер из MIT Technology Review, начал ковыряться, звоня научным консультантам BioViva и требуя подробностей о том, что произошло в ходе эксперимента. По крайней мере, у одного из бесплатных консультантов, который во многих случаях встречался с Пэрриш на конференциях и был достаточно очарован, чтобы быть упомянутым на веб-сайте BioViva, теперь возникли собственные вопросы о том, что она сделала.
Она решила опередить репортера Technology Review , который изначально не знал, что она была подопытной эксперимента. Воскресным утром в октябре, за три дня до того, как его история была опубликована под названием «Повесть о самодельной генной терапии», она зашла на Reddit, представившись «женщиной, которая хочет вас генетически сконструировать» и как генеральный директор БиоВива. «Я не врач и не ученый, — написала она. Но BioViva только что лечила своего первого пациента от старения. «АМА», — напечатала она, — спрашивайте меня о чем угодно.
«Я не врач и не ученый, — написала она. Но BioViva только что лечила своего первого пациента от старения. «АМА», — напечатала она, — спрашивайте меня о чем угодно.
Первый комментатор спросил ее любимую начинку для пиццы. — Вяленые помидоры, — ответила она. «:)»
Следующий человек спросил: Как вы выбрали первого пациента? «Я — нулевой пациент», — ответила она. «У меня старение как болезнь».
Испытывать продукцию BioViva сначала на себе, по словам Пэрриш, было единственным этическим выбором. Ей вводили hTERT и ингибитор миостатина. Пользователи Reddit высоко оценили ее храбрость. «Я горжусь тем, что приняла участие в помощи миллионам людей, даже если это имело плохие результаты», — написала она. «Я счастлив быть пациентом Zero. Это для всего мира, для больных детей и больных стариков».
Был ли риск рака? — спросил кто-то. «БиоВива» будет отслеживать все известные биомаркеры рака в ее организме, — ответил Пэрриш. Но введение гена теломеразы лабораторным животным не увеличило заболеваемость раком, сказала она.
«Помните, что самый важный фактор риска развития рака — старение», — написала она. «Большинство видов рака возникает у людей старше 65 лет».
Как насчет обычных людей: смогут ли они позволить себе лечение? «Технология генной терапии очень похожа на вычислительную технику, — ответила она. «Нам пришлось построить суперкомпьютер, который стоил 8 миллионов долларов в 19 веке.60-е годы. Теперь у всех есть технологии, которые работают предсказуемо и по цене, которую может себе позволить средний человек».
По мере того, как АМА продолжалась, вопросы становились все более экзистенциальными. «Если/когда это станет реальностью для широкой публики, — спросил кто-то, — как это повлияет на численность населения?» А как насчет физических ограничений планеты? А как насчет того, что мы могли бы создать два класса людей: высший класс, который мог позволить себе платить за эту терапию, и низший класс, который умирает точно по графику?
BioViva не «пыталась определить, кому жить, а кому умереть», — писал Пэрриш. «Каждый имеет право на жизнь без страданий». Пользователь подверг критике ее логику: «Неверно, что технология продления жизни уменьшит количество жизней, прожитых в страданиях… Вы пытаетесь создать технологии, которые, в случае успеха, могут изменить распределение смертей среди населения, и потенциальные более широкие последствия этого изменения заслуживают некоторого внимания».
«Каждый имеет право на жизнь без страданий». Пользователь подверг критике ее логику: «Неверно, что технология продления жизни уменьшит количество жизней, прожитых в страданиях… Вы пытаетесь создать технологии, которые, в случае успеха, могут изменить распределение смертей среди населения, и потенциальные более широкие последствия этого изменения заслуживают некоторого внимания».
Она ответила быстро. «По мере увеличения продолжительности жизни показатели рождаемости снижаются во всем мире», — написала она. «Люди создадут лучшие технологии, и космические путешествия увеличатся». Вскоре она расписалась. Хорошие результаты, казавшиеся ей очевидными, оказались менее очевидными для остального мира.
К тому времени, когда в октябре 2015 года вышла статья MIT Technology Review , один из членов научно-консультативного совета BioViva, геронтолог Вашингтонского университета Джордж Мартин, ушел в отставку. Другой, Джордж Черч, подчеркнул свою поддержку надлежащих клинических испытаний и, похоже, преуменьшил свои связи с BioViva.
«Я консультирую людей, которым нужен совет, а они явно нуждаются в совете», — сказал он позже The Guardian — даже когда его лаборатория приняла образцы крови, которые Пэрриш прислал после эксперимента в Боготе. Ранний защитник теломер Майкл Фоссел, врач, написавший 1996 book Reversing Human Aging, вместе с The Telomerase Revolution в 2015 году, который теперь руководил биотехнологической компанией, которая планировала использовать hTERT для борьбы с болезнью Альцгеймера, хвалил Пэрриша в своем блоге.
«Мы не можем не приветствовать смелость Лиз в использовании себя в качестве субъекта, процедура с долгой (и иногда неоднозначной) историей в медицинской науке», — написал он. И это «подрывает большую часть этической критики, которая была бы более острой, если бы она использовала других пациентов». Но стандартный путь, включая одобренные FDA испытания, гарантировал три вещи: безопасность, эффективность и достоверность. В случае с Пэрришем то, что произошло, было больше похоже на одиночное испытание с одним испытуемым, которое не было достаточно строгим, чтобы обеспечить достоверное доказательство чего бы то ни было. «Легко действовать, может быть даже легко действовать с искренним состраданием, — заключил Фоссель, — но трудно действовать эффективно и еще труднее добиться того, чтобы сострадание было не только намерением, но и конечной реальностью».
«Легко действовать, может быть даже легко действовать с искренним состраданием, — заключил Фоссель, — но трудно действовать эффективно и еще труднее добиться того, чтобы сострадание было не только намерением, но и конечной реальностью».
Пэрриш Reddit AMA и история Регаладо сопровождались потоком сообщений в блогах, видео на YouTube и интервью на таких сайтах, как Singularity Weblog и Longevity Reporter. The Guardian и Discover называется журнал.
«Эксперимент, скорее всего, запомнят либо как новый закон медицинского шарлатанства, либо, возможно, как маловероятное начало эры, когда люди получают генетические модификации не только для лечения болезней, но и для обращения вспять старения», — писал Регаладо. На периферии, куда часто опускались ноги Билла Эндрюса и Обри де Грея, где настоящая наука смешивалась с чем-то близким к религии, Пэрриш сразу же стал героем. Организаторы конференций пригласили ее выступить с программными речами по всему миру. Вскоре она улетела в Москву, Нью-Йорк, Гонконг, Париж, Осло, Оксфорд и даже в Астану, Казахстан. Она начала жить неполный рабочий день на острове Бейнбридж, неполный рабочий день на чемоданах.
Она начала жить неполный рабочий день на острове Бейнбридж, неполный рабочий день на чемоданах.
Однажды сын Пэрриш пришел домой и спросил, не модифицировала ли она себя, чтобы оставаться молодой. «Я подумала: «О, дорогой, я это сделала», — вспоминает она. Мальчик принял это. Потом запел: «Мама будет жить вечно».
Она рассказала своей лучшей подруге о том, что она сделала, а затем своему отцу, которому за семьдесят и у которого первые симптомы болезни Паркинсона. Он сказал ей, что она поступила правильно. И все же, в течение еще семи месяцев после Reddit AMA, несмотря на то, что появлялось больше новостей и Facebook освещал ее имя, Пэрриш все еще скрывала новости от своего мужа и детей.
Однажды весной 2016 года ее сын пришел домой из средней школы с вопросом. Он прочитал в Интернете, что она генетически модифицировала себя. Было ли это правдой?
Она больше не могла сдерживаться. «Я подумала: «О, дорогой, я это сделала», — вспоминает она. Мальчик, теперь одержимый футболом и успешно идущий по жизни с диабетом, принял это. Затем он начал петь: «Мама будет жить вечно. Мама будет жить вечно».
Мальчик, теперь одержимый футболом и успешно идущий по жизни с диабетом, принял это. Затем он начал петь: «Мама будет жить вечно. Мама будет жить вечно».
Пэрриш говорит, что ее муж был в ярости, когда она наконец сказала ему, но она все еще была уверена, что ее действия были необходимы. Было неправильно игнорировать проблему, особенно такую большую, как смерть, и просто оставлять ее следующему поколению, чтобы попытаться решить ее. Она сделала это для детей, сказала она мужу. «Я учу их жить».
Было ясно, что внутри нее что-то изменилось, но со временем стало неясно, было ли это что-то физическим. Она не превратилась обратно в 25-летнюю. И, с другой стороны, у нее не было рака. Ее биомаркеры — триглицериды, С-реактивные белки, мышечная масса — были многообещающими, но в конечном итоге неубедительными, поскольку они были результатами всего одного человека и не были опубликованы в рецензируемом исследовании.
В апреле 2016 года компания BioViva выпустила еще один пресс-релиз: «Первая успешная генная терапия против старения человека». Были получены результаты теломерных тестов Пэрриш. Сравнивая кровь, взятую до и после ее процедуры, специализированная лаборатория в Хьюстоне определила, что теломеры ее лейкоцитов, длина которых измерялась путем подсчета количества пар оснований ДНК, увеличились. к 9процент. В релизе говорится, что это эквивалентно обращению вспять 20-летнего старения. Но не было опубликованного исследования, соответствующего этому, и эту новость было легко проигнорировать.
Были получены результаты теломерных тестов Пэрриш. Сравнивая кровь, взятую до и после ее процедуры, специализированная лаборатория в Хьюстоне определила, что теломеры ее лейкоцитов, длина которых измерялась путем подсчета количества пар оснований ДНК, увеличились. к 9процент. В релизе говорится, что это эквивалентно обращению вспять 20-летнего старения. Но не было опубликованного исследования, соответствующего этому, и эту новость было легко проигнорировать.
На протяжении всего восхождения Пэрриш к теломерной суперзвезде Билл Эндрюс почти ничего не говорил о ее генной терапии — до недавнего времени. «Я беру на себя всю вину, — сказал он мне. «Я был трусом. Вы можете процитировать меня по этому поводу». Он не жалеет, что Пэрриш заинтересовался теломерами, и не жалеет о своем участии в ее генной терапии. Он имеет в виду, что, поскольку он сказал ей, что не может участвовать ни в каком эксперименте, потому что не хотел подвергать опасности свои годы исследований, если они пойдут не так, он не был рядом с ней, чтобы убедиться, что она это сделает. это правильно. «Она действительно выдвинула биологию теломер на передний план», — говорит Эндрюс. «Она никогда не будет исключена из истории биологии теломер». Но дело в том, что она выглядит почти так же, как и раньше, и то, что она сделала, не было научным испытанием. «Я даже не могу сказать, использовала ли она законный протокол», когда использовала генную терапию, — говорит Эндрюс. «Мы не получили достаточно данных. У нас нет ничего, что мы могли бы реально измерить». Для Эндрюса Пэрриш — пример невероятно храброго человека, но не человека, который снова стал молодым.
это правильно. «Она действительно выдвинула биологию теломер на передний план», — говорит Эндрюс. «Она никогда не будет исключена из истории биологии теломер». Но дело в том, что она выглядит почти так же, как и раньше, и то, что она сделала, не было научным испытанием. «Я даже не могу сказать, использовала ли она законный протокол», когда использовала генную терапию, — говорит Эндрюс. «Мы не получили достаточно данных. У нас нет ничего, что мы могли бы реально измерить». Для Эндрюса Пэрриш — пример невероятно храброго человека, но не человека, который снова стал молодым.
Когда RAADfest 2017 открыл свои двери в августе прошлого года, Пэрриш исполнилось 46 лет. На ней было черное платье, красная помада и Apple Watch, а в сумочке у нее был iPhone с приложением, которое позволяло ей отслеживать уровень сахара в крови ее сына в режиме реального времени днем и ночью. Второй год подряд Strole и Bernadeane проводили RAADfest в Town and Country San Diego, старом курортном отеле площадью 42 акра с бассейнами, пластиковыми фламинго и конференц-центром, который находился всего в нескольких футах от межштатной автомагистрали. 8.
8.
Пэрриш выступает на RAADfest 2017 (McKenzie Funk)
Под люстрами Town и Country седовласые посетители медленно ступали по выцветшим коврам, направляясь к главной сцене или выставочному залу, известному как RAADcity, где маркетологи продавали нутрицевтики, вода без дейтерия, банк стволовых клеток, озонотерапия и «пакеты для оптимизации здоровья» на 100 000 долларов. Билл Эндрюс иногда стоял рядом с портретом Билла Эндрюса почти в натуральную величину, который рекламировал антивозрастную сыворотку для кожи под названием One Truth 818. Один мужчина ходил в рубашке с надписью «МОГУ Я ПОСТАВИТЬ ЗАЯВКУ НА ВАШУ КРИОНИКОВУЮ СТРАХОВКУ ЖИЗНИ?»
Пэрриш пытался держаться подальше от RAADcity. Она сказала мне, что все ненаучные утверждения доставляли ей неудобство. Она широко шагала по конференц-центру, временами за ней следовала съемочная группа Би-би-си, а незнакомцы и друзья то и дело останавливали ее. Я наблюдал, как она отвечала на вопросы молодой женщины на костылях, а затем полчаса держалась за руки сгорбленной пожилой леди из People Unlimited, которая умоляла о доступе к генной терапии BioViva. Молодой человек из Нью-Йорка, чья мать была неизлечимо больна, следовал за Пэрриш, записывая все, что она говорила. Всего несколько лет назад, на SENS 6, это была она. Теперь она была на другой стороне, пытаясь дать людям надежду.
Молодой человек из Нью-Йорка, чья мать была неизлечимо больна, следовал за Пэрриш, записывая все, что она говорила. Всего несколько лет назад, на SENS 6, это была она. Теперь она была на другой стороне, пытаясь дать людям надежду.
То, что Пэрриш говорил о геномике — что мы стоим на пороге революции — казалось, сбывалось. В первый день RAADfest, когда инженер-биомедик из лаборатории Джорджа Черча в Гарварде выступал с докладом об использовании инструмента редактирования генома Crispr для включения и выключения генов, участники увидели всплывающий заголовок на своих телефонах: «Шпоры редактирования генов». Надежда на трансплантацию свиных органов людям». Несколько недель спустя FDA одобрило первое изменяющее гены лечение для борьбы с лейкемией, терапию от Novartis под названием Kymriah. Через два месяца после этого будет одобрена аналогичная генная терапия неходжкинской лимфомы рака крови. Этой осенью также будет показано, что генная терапия спасает детей от смертельной болезни головного мозга, адренолейкодистрофии, а врачи в Европе будут использовать генную терапию, чтобы восстановить кожу маленького сирийского мальчика, спасая ему жизнь.
На главной сцене я увидел воодушевляющую речь Пэрриша о медицинском выборе — «Вы имеете право делать со своим телом все, что хотите!» — и вызвал бурные аплодисменты. Затем я выслушал, как Обри де Грей помазал ее неожиданным одобрением. Расхаживая по сцене в красной рубашке и линялых джинсах, он описал откровение, которое пришло к нему только в зрелом возрасте: не все согласны с тем, что смерть — самая важная проблема в мире.
«Вы не вступаете в дискуссии с людьми об очевидных вещах, верно?» он сказал. «Я никогда не говорил: «Как ты думаешь, какого цвета небо?» Теперь он понял, что недостаточно объяснить, как люди могут продлевать жизнь, — нужно еще объяснить почему. Он мог заниматься наукой. Строул и Бернадин могли бы заняться мотивацией. «RAADfest стал успешным благодаря сочетанию этих двух вещей», — сказал он. «Но лучшее, что мы могли бы получить, — это увидеть это сочетание в одном человеке. И я считаю, что Лиз Пэрриш делает это лучше, чем кто-либо другой».
Пэрриш едва расслышал речь де Грея. Она проводила много времени в столовой, съежившись с Эндрюсом за одним из круглых столов, вполголоса болтая о сделках и контрактах. Появился и исчез загадочный инвестор, а точнее загадочный сотрудник неназванного потенциального инвестора. Другой мужчина, с бритой головой и плотным телосложением, тоже иногда зависал.
В течение двух лет Пэрриш утверждал, что BioViva скоро откроет зарубежные клиники — возможно, в Карибском бассейне или Латинской Америке, возможно, где-нибудь ближе к Европе. Незадолго до RAADfest 2016 она и Эндрюс сделали скоординированное объявление: они стали партнерами в новом предприятии под названием BioViva Fiji. Они продемонстрировали архитектурную визуализацию в целом современной клиники генной терапии, со всеми стальными балками, большими окнами и деревянными вставками. Казалось, они ждали финансирования — обычное состояние анабиоза Эндрюса, а теперь, похоже, и Пэрриша. Когда фиджийская пресса узнала о BioViva Fiji, власти заявили журналистам, что ее не существует даже на бумаге. А на RAADfest 2017 ни Пэрриш, ни Эндрюс, похоже, больше не хотели об этом говорить.
А на RAADfest 2017 ни Пэрриш, ни Эндрюс, похоже, больше не хотели об этом говорить.
Прошло несколько месяцев, прежде чем я понял, что вижу в столовой. Это была прелюдия к разрыву, дружеское (и, возможно, временное) расставание. В декабре 2017 года новая компания под названием Libella Gene Therapeutics, управляемая лысым эрготерапевтом из Канзаса Джеффом Мэтисом, объявила, что получила эксклюзивную лицензию от Билла Эндрюса на его технологию фермента транскриптазы AAV Reverse (hTERT). Теперь Либелла набирала пациентов для первого в истории исследования в Картахене, Колумбия. «Вызывая теломеразу, — говорится в пресс-релизе, — Dr. Эндрюс и Либелла Генная терапия надеются удлинить теломеры в клетках организма».
Не было ни слова о BioViva, ни о Пэрриш, ни о ее экспериментах над собой. Пэрриш и ее неоднозначные результаты, казалось, отсутствовали в этой истории. Теломераза «никогда не вводилась людям, кроме как в малых дозах», взволнованно сказал Эндрюс интервьюеру. Он был уверен, что это сработает. Предстоящий судебный процесс в Картахене, сказал он, «на самом деле является первой возможностью за более чем 25 лет исследований, когда мы действительно сможем показать, что все, что я делал, было полезным».
Предстоящий судебный процесс в Картахене, сказал он, «на самом деле является первой возможностью за более чем 25 лет исследований, когда мы действительно сможем показать, что все, что я делал, было полезным».
«Мы попадаем во время», — любит говорить Пэрриш. Это должно звучать футуристично. Мы всегда заняты чем-то, имеет она в виду. Мы заполняем пространство. Это ее стандартный ответ на вопрос, который часто слышат имморталисты: если мы будем жить вечно, не будет ли нам скучно? Это также может объяснить, как она стала Нулевой пациенткой и как с тех пор ничего не изменилось. Жизнь продолжает мчаться вперед.
Недавним солнечным днем на острове Бейнбридж мы с Пэрриш встретились за ланчем, чтобы она рассказала мне о новом направлении BioViva. Она выглядела как здоровая и нормальная 46-летняя женщина. Она сказала, что чувствовала, что у нее по крайней мере немного больше энергии, чем раньше. Она хотела заказать суп, но он не был веганским, поэтому она пошла за салатом.
«Итак, BioViva теперь биоинформатическая компания!» — объявила она. Это было поворотно. В настоящее время он не пытался проводить клинические испытания. Даже в офшорах, вдали от FDA, они стоят миллионы долларов, и сбор таких денег для проведения традиционных испытаний будет равнозначен медлительности, которую она пыталась преодолеть. BioViva станет платформой данных для других компаний, собирающей и анализирующей информацию, полученную в ходе испытаний. Она упомянула многообещающее партнерство с брокером Integrated Health Systems, у которого есть скудный веб-сайт, созданный за последние несколько месяцев, который утверждает, что связывает биотехнологические компании и платит пациентам с врачами, специализирующимися на генной терапии. Она упомянула еще одно потенциальное партнерство с компанией в Гонконге, которая занимается машинным обучением. Ей нечего было сказать о Либелле. Она просто не была сосредоточена на том, что они планировали в Колумбии.
Это было поворотно. В настоящее время он не пытался проводить клинические испытания. Даже в офшорах, вдали от FDA, они стоят миллионы долларов, и сбор таких денег для проведения традиционных испытаний будет равнозначен медлительности, которую она пыталась преодолеть. BioViva станет платформой данных для других компаний, собирающей и анализирующей информацию, полученную в ходе испытаний. Она упомянула многообещающее партнерство с брокером Integrated Health Systems, у которого есть скудный веб-сайт, созданный за последние несколько месяцев, который утверждает, что связывает биотехнологические компании и платит пациентам с врачами, специализирующимися на генной терапии. Она упомянула еще одно потенциальное партнерство с компанией в Гонконге, которая занимается машинным обучением. Ей нечего было сказать о Либелле. Она просто не была сосредоточена на том, что они планировали в Колумбии.
Пэрриш казался менее осторожным, чем раньше. В последнее время, по ее словам, она старалась проводить больше времени дома с сыном, как и в дни до того, как ему поставили диагноз, до того, как она начала постоянно путешествовать. «Я просто так застряла на этом ребенке», — сказала она мне. «Он становится таким большим. Я так горжусь им». Она рассказала мне о его футбольной команде. Она продолжала проверять его уровень инсулина с помощью приложения для телефона. Она казалась искренне счастливой. Как будто она перестала изо всех сил пытаться жить вечно, но она все еще изо всех сил старалась жить.
«Я просто так застряла на этом ребенке», — сказала она мне. «Он становится таким большим. Я так горжусь им». Она рассказала мне о его футбольной команде. Она продолжала проверять его уровень инсулина с помощью приложения для телефона. Она казалась искренне счастливой. Как будто она перестала изо всех сил пытаться жить вечно, но она все еще изо всех сил старалась жить.
Маккензи Фанк (@McKenzieFunk) — автор книги « Неожиданная удача: быстро развивающийся бизнес глобального потепления». Он живет в Сиэтле.
Лиз Пэрриш — нулевой пациент в своем собственном эксперименте по борьбе со старением
Лиз Пэрриш — генеральный директор, гуманист и нулевой пациент в своем собственном эксперименте. (Источник: BioViva) Элизабет (Лиз) Пэрриш — генеральный директор BioViva, биотехнологической компании, которая занимается разработкой генной терапии и других регенеративных методов лечения для вмешательства в процесс старения человека. В сентябре прошлого года Пэрриш добавила к описанию своей работы интересную строчку: нулевой пациент для двух методов антивозрастной терапии, которые исследует компания. Пэрриш получает два вида инъекций, которые вводят за пределами Соединенных Штатов: ингибитор миостатина, который, как ожидается, предотвратит возрастную потерю мышечной массы; и генная терапия теломеразой, которая, как ожидается, удлинит теломеры, сегменты ДНК на концах хромосом, укорачивание которых связано со старением и дегенеративными заболеваниями. Исследование, вероятно, будет продолжаться в течение многих лет. Но на прошлой неделе BioViva выпустила пресс-релиз с описанием неожиданных первых результатов, предлагая подсказку относительно того, что команда BioViva может опубликовать в ближайшие недели или месяцы. Будет неясно, что именно обнаружили исследователи BioViva, пока результаты не пройдут строгий процесс научной рецензирования, но непроверенный отчет BioViva вызывает у некоторых удивление. Теломеры Т-лимфоцитов в пробах крови, взятых у Пэрриша в сентябре, составляли 6,71 килобазы. Это меньше, чем обычно для возраста Пэрриша, но, по данным BioViva, лимфоциты из образцов, взятых в марте после шести месяцев генной терапии, имели размер 7,33 т.
Пэрриш получает два вида инъекций, которые вводят за пределами Соединенных Штатов: ингибитор миостатина, который, как ожидается, предотвратит возрастную потерю мышечной массы; и генная терапия теломеразой, которая, как ожидается, удлинит теломеры, сегменты ДНК на концах хромосом, укорачивание которых связано со старением и дегенеративными заболеваниями. Исследование, вероятно, будет продолжаться в течение многих лет. Но на прошлой неделе BioViva выпустила пресс-релиз с описанием неожиданных первых результатов, предлагая подсказку относительно того, что команда BioViva может опубликовать в ближайшие недели или месяцы. Будет неясно, что именно обнаружили исследователи BioViva, пока результаты не пройдут строгий процесс научной рецензирования, но непроверенный отчет BioViva вызывает у некоторых удивление. Теломеры Т-лимфоцитов в пробах крови, взятых у Пэрриша в сентябре, составляли 6,71 килобазы. Это меньше, чем обычно для возраста Пэрриша, но, по данным BioViva, лимфоциты из образцов, взятых в марте после шести месяцев генной терапии, имели размер 7,33 т. п.н.
п.н.
На этом изображении хромосомы теломеры выделены зеленым цветом. (Викимедиа) Компания приравнивает заявленное увеличение на 620 оснований к тому, что часы на хромосомах Пэрриша повернулись вспять на двадцать лет. Но есть многочисленные предостережения, отмеченные экспертами в области генетики и лабораторной медицины, которые были недавно опубликованы некоммерческой группой Genetics Expert News Service. Во-первых, теломеры проверяются только в ее Т-лимфоцитах, а не во всех типах тканей ее тела, поэтому даже если результат теста свидетельствует о замедлении старения Т-лимфоцитов, это не обязательно доказывает, что все ее тело несовершеннолетний. «Долгоживущие Т-клетки имеют более короткую длину теломер, чем недавно сгенерированные наивные клетки; а клетки, достигшие максимального предела клеточного деления, имеют более короткие теломеры, чем любой другой тип клеток», — говорит Рита Эффрос, профессор патологии и лабораторной медицины Калифорнийского университета в Лос-Анджелесе. «Таким образом, простое изменение доли различных типов клеток в периферической крови может легко объяснить полученные данные». Кроме того, доктор Брэдли Джонсон, адъюнкт-профессор патологии и лабораторной медицины Пенсильванского университета, отмечает: «Измерения длины теломер, как правило, имеют низкую точность, с разницей в измерениях около 10 процентов, что, по-видимому, находится в диапазоне зарегистрированного удлинения теломер. пережила Элизабет Пэрриш». Несмотря на эту критику, Пэрриш, ставший нулевым пациентом для совершенно нового лечения, является важной вехой в медицине, которая восходит к пионерам медицины, которые регулярно вводили себе различные новые лекарства более века назад. Перед тем, как появились новости BioViva, доктор Дэвид Вармфлэш из Discover взял интервью у Пэрриш о методах лечения и о ее чувствах по поводу того, что она стала первым подопытным.
«Таким образом, простое изменение доли различных типов клеток в периферической крови может легко объяснить полученные данные». Кроме того, доктор Брэдли Джонсон, адъюнкт-профессор патологии и лабораторной медицины Пенсильванского университета, отмечает: «Измерения длины теломер, как правило, имеют низкую точность, с разницей в измерениях около 10 процентов, что, по-видимому, находится в диапазоне зарегистрированного удлинения теломер. пережила Элизабет Пэрриш». Несмотря на эту критику, Пэрриш, ставший нулевым пациентом для совершенно нового лечения, является важной вехой в медицине, которая восходит к пионерам медицины, которые регулярно вводили себе различные новые лекарства более века назад. Перед тем, как появились новости BioViva, доктор Дэвид Вармфлэш из Discover взял интервью у Пэрриш о методах лечения и о ее чувствах по поводу того, что она стала первым подопытным.
Откройте для себя: Что, по вашему мнению, отличает BioViva от других биотехнологических или генно-терапевтических компаний? Вы используете себя в качестве испытуемого? Лиз Пэрриш: Да, и номер два — это отношение к биологическому старению как к болезни. На самом деле, это, наверное, номер один. Мы идем к первопричине того, от чего болеет большая часть населения. И, во-вторых, конечно, мы стопроцентно стоим за продуктом. Мы их используем. Мы не просто исследовательская компания. BioViva занимается спасением жизней, и уроки истории показывают, что одновременное использование нескольких экспериментальных методов лечения может быть кратчайшим путем к спасению жизней. Когда только начались исследования СПИДа, мы видели использование многих лекарств, которые, будучи изолированными, помогали при одном механизме заболевания, но пациенты все равно умирали от другого механизма той же болезни. Только когда врачи объединили эти препараты в коктейли, мы увидели первые реальные успехи в борьбе со СПИДом. 9века кто испытывал на себе разные лекарства?
На самом деле, это, наверное, номер один. Мы идем к первопричине того, от чего болеет большая часть населения. И, во-вторых, конечно, мы стопроцентно стоим за продуктом. Мы их используем. Мы не просто исследовательская компания. BioViva занимается спасением жизней, и уроки истории показывают, что одновременное использование нескольких экспериментальных методов лечения может быть кратчайшим путем к спасению жизней. Когда только начались исследования СПИДа, мы видели использование многих лекарств, которые, будучи изолированными, помогали при одном механизме заболевания, но пациенты все равно умирали от другого механизма той же болезни. Только когда врачи объединили эти препараты в коктейли, мы увидели первые реальные успехи в борьбе со СПИДом. 9века кто испытывал на себе разные лекарства?
LP: Да, наверное, да, оглядываясь назад. Мы сделали это не в том духе. Мы сделали это, потому что это нужно было сделать, потому что нам нужен был тестовый пациент для генной терапии, но я думаю, что это именно в этом духе, и я бы хотел, чтобы больше людей разделяли этот дух. В США проживает 5 процентов населения мира. Мы принимаем 75 процентов всех отпускаемых по рецепту лекарств, и при этом у нас самая короткая продолжительность жизни среди всех промышленно развитых стран, поэтому я хочу, чтобы больше людей отказывались от своих лекарств и других методов лечения. Я думаю, это докажет, что то, что у них есть, это то, что вы хотели бы взять. Итак, давайте поговорим о методах лечения, которые вы принимаете. Есть ли опасения, что генная терапия теломеразой может привести к злокачественным новообразованиям, к раку в любой ткани? ЛП: Теломераза никогда не выдвигалась гипотезой как единственная причина рака. Не все виды рака имеют повышенную регуляцию теломеразы. Раковые клетки могут ежедневно развиваться в вашем организме с самого раннего возраста. Но разве молодая иммунная система не удерживает полномасштабный рак в страхе? Смешение исследований долголетия с исследованиями рака является повторяющимся заблуждением и подразумевает недоказанные корреляции. Есть два направления исследований теломеразы: долголетие и рак.
В США проживает 5 процентов населения мира. Мы принимаем 75 процентов всех отпускаемых по рецепту лекарств, и при этом у нас самая короткая продолжительность жизни среди всех промышленно развитых стран, поэтому я хочу, чтобы больше людей отказывались от своих лекарств и других методов лечения. Я думаю, это докажет, что то, что у них есть, это то, что вы хотели бы взять. Итак, давайте поговорим о методах лечения, которые вы принимаете. Есть ли опасения, что генная терапия теломеразой может привести к злокачественным новообразованиям, к раку в любой ткани? ЛП: Теломераза никогда не выдвигалась гипотезой как единственная причина рака. Не все виды рака имеют повышенную регуляцию теломеразы. Раковые клетки могут ежедневно развиваться в вашем организме с самого раннего возраста. Но разве молодая иммунная система не удерживает полномасштабный рак в страхе? Смешение исследований долголетия с исследованиями рака является повторяющимся заблуждением и подразумевает недоказанные корреляции. Есть два направления исследований теломеразы: долголетие и рак. Они никогда не пересекаются. В исследованиях долголетия мы наблюдаем не увеличение количества раковых клеток в результате индукции теломеразы, а скорее защиту от рака. В предыдущих интервью с другими людьми вы упомянули трагическую историю Джесси Гелсингера, 18-летнего мальчика, который умер в ходе ранних клинических испытаний генной терапии в Пенсильванском университете в 1990-е. Этически, конечно, между вами и Гелсингером есть разница; Я слышал, ты сказал, что ради этого стоит рискнуть жизнью. Но вдобавок к трагедии, связанной с потерей Гелсингера, не отбросила ли она всю область генной терапии на несколько лет назад? С этой точки зрения, в маловероятном случае, если что-то пойдет не так в эксперименте на вас, беспокоитесь ли вы о том, что может случиться с исследованиями в области генной терапии? Считаете ли вы это возможным объяснением замедления, может быть, более консервативного подхода? ЛП: Генная терапия прошла долгий путь с 19-го века.99 трагедия Джесси Гелсингер. Соответствующие исследования не прекратились [после события], только заявки, да и то временно.
Они никогда не пересекаются. В исследованиях долголетия мы наблюдаем не увеличение количества раковых клеток в результате индукции теломеразы, а скорее защиту от рака. В предыдущих интервью с другими людьми вы упомянули трагическую историю Джесси Гелсингера, 18-летнего мальчика, который умер в ходе ранних клинических испытаний генной терапии в Пенсильванском университете в 1990-е. Этически, конечно, между вами и Гелсингером есть разница; Я слышал, ты сказал, что ради этого стоит рискнуть жизнью. Но вдобавок к трагедии, связанной с потерей Гелсингера, не отбросила ли она всю область генной терапии на несколько лет назад? С этой точки зрения, в маловероятном случае, если что-то пойдет не так в эксперименте на вас, беспокоитесь ли вы о том, что может случиться с исследованиями в области генной терапии? Считаете ли вы это возможным объяснением замедления, может быть, более консервативного подхода? ЛП: Генная терапия прошла долгий путь с 19-го века.99 трагедия Джесси Гелсингер. Соответствующие исследования не прекратились [после события], только заявки, да и то временно. Но самое важное, что сейчас меняет правила игры, это то, что у нас есть лучшие методы доставки. Сотни людей сегодня проходят генную терапию, и ни у кого из них нет проблем, которые мы видели 16 лет назад у Джесси Гелсингера. Мы также должны рассматривать это в перспективе: почти 100 000 человек уже ежегодно умирают от побочных реакций на лекарства (НПР) только в США, в то время как никто никогда не умирал от этого последнего поколения генной терапии. При этом мы в BioViva очень тщательно следим за тем, чтобы обеспечить максимально безопасный результат, при этом проверяя все ограничения. Я бы не пошел на генную терапию, которая, вероятно, убила бы пациента, как и никто в BioViva. Я просто заявил, что все данные одинаково важны, и что с этой целью я приму любой исход, вплоть до собственной смерти, чтобы продвинуть науку вперед. Мы, как компания, и я, как человек, пошли на риск, но этот риск, как мы верим, изменит мир к лучшему и даст толчок развитию отрасли с лучшим подходом к лечению болезней и увеличению продолжительности здоровой жизни.
Но самое важное, что сейчас меняет правила игры, это то, что у нас есть лучшие методы доставки. Сотни людей сегодня проходят генную терапию, и ни у кого из них нет проблем, которые мы видели 16 лет назад у Джесси Гелсингера. Мы также должны рассматривать это в перспективе: почти 100 000 человек уже ежегодно умирают от побочных реакций на лекарства (НПР) только в США, в то время как никто никогда не умирал от этого последнего поколения генной терапии. При этом мы в BioViva очень тщательно следим за тем, чтобы обеспечить максимально безопасный результат, при этом проверяя все ограничения. Я бы не пошел на генную терапию, которая, вероятно, убила бы пациента, как и никто в BioViva. Я просто заявил, что все данные одинаково важны, и что с этой целью я приму любой исход, вплоть до собственной смерти, чтобы продвинуть науку вперед. Мы, как компания, и я, как человек, пошли на риск, но этот риск, как мы верим, изменит мир к лучшему и даст толчок развитию отрасли с лучшим подходом к лечению болезней и увеличению продолжительности здоровой жизни.
Что вы думаете о том, что, несмотря на потенциал изучения вас, вы всего лишь одно данное, так что мы на самом деле узнаем? ЛП: Да, абсолютно. Это правда, но N=1 от одного человека стоит 10 000 мышей, но, конечно, тело каждого человека отличается, и люди будут реагировать по-разному. И, конечно же, FDA с 1970-х годов пропустило через эту систему на рынок почти 50 лекарств, которые оно вытащило позже, несмотря на то, что они прошли тестирование по золотому стандарту. Вот почему мы должны начать прямо сейчас и посмотреть, что произойдет. Независимо от того, какая у вас безопасность и эффективность, если вы можете получить N = 10 000, у вас, вероятно, будут побочные эффекты в будущем. На определение того, связано ли это непосредственно с генной терапией или с чем-то еще в жизни пациента, могут уйти годы, поэтому очень важно начать именно с генной терапии. В настоящее время более 100 000 человек умирают от болезней, связанных со старением, так в какой момент мы осознаем, что жизнь рискованна и что лучше всего рискнуть? Какие ткани они используют для контроля длины ваших теломер, учитывая, что теломеры различаются в разных тканях? Как правило, в исследованиях теломер используются лимфоциты, потому что к ним легко получить доступ, но какие факторы повлияли на решение о том, какие ткани использовать у вас как для мониторинга, так и для нацеливания на терапию. ЛП: В настоящее время мы используем тестирование лимфоцитов, поскольку на сегодняшний день это самый продвинутый и понятный способ определения длины теломер. Я также понимаю, что для переноса терапевтического гена через вашу кровь в ваши клетки BioViva использует так называемый вектор AAV, преимущество которого состоит в том, что он доставляет генетическую полезную нагрузку так, что он заканчивается эписомой (свободно плавающим геном), а не чем интегрирование в хромосому. Является ли это мерой безопасности для сведения к минимуму риска мутагенеза и онкогенной трансформации? Есть ли в этом какой-то возможный негатив, например, уменьшение продолжительности эффектов? ЛП: Мы не обязательно пытаемся интегрировать ген, поскольку исследования не доказали преимущества этого. Мы пытаемся создать эписому в ядре, которая будет кодировать целевой белок. Интеграция по-прежнему является важным предметом обсуждения, поскольку методы доставки, которых мы избегаем в прошлом, создают интеграционный мутагенез (интеграция в хромосому в случайных областях, что приводит к нестабильности клетки).
ЛП: В настоящее время мы используем тестирование лимфоцитов, поскольку на сегодняшний день это самый продвинутый и понятный способ определения длины теломер. Я также понимаю, что для переноса терапевтического гена через вашу кровь в ваши клетки BioViva использует так называемый вектор AAV, преимущество которого состоит в том, что он доставляет генетическую полезную нагрузку так, что он заканчивается эписомой (свободно плавающим геном), а не чем интегрирование в хромосому. Является ли это мерой безопасности для сведения к минимуму риска мутагенеза и онкогенной трансформации? Есть ли в этом какой-то возможный негатив, например, уменьшение продолжительности эффектов? ЛП: Мы не обязательно пытаемся интегрировать ген, поскольку исследования не доказали преимущества этого. Мы пытаемся создать эписому в ядре, которая будет кодировать целевой белок. Интеграция по-прежнему является важным предметом обсуждения, поскольку методы доставки, которых мы избегаем в прошлом, создают интеграционный мутагенез (интеграция в хромосому в случайных областях, что приводит к нестабильности клетки). Мы хотим отделить наш метод от более старого метода. Наш метод доставки не вызывает интеграционного мутагенеза, а если и интегрируется, то в безопасный участок на хромосоме 19.где рак не является исходом.
Мы хотим отделить наш метод от более старого метода. Наш метод доставки не вызывает интеграционного мутагенеза, а если и интегрируется, то в безопасный участок на хромосоме 19.где рак не является исходом.
Есть ли у вашей команды опасения, что лечение для замедления или обращения вспять старения здоровых тканей может также предотвратить элиминацию злокачественных или предраковых клеток? ЛП: Раковые клетки могут появиться у людей любого возраста, но пролиферация раковых клеток в большей степени снижение способности иммунной системы, чем увеличение активности теломеразы. Не все виды рака связаны с выработкой теломеразы, и рецензируемая статья 2012 года показала, что у старых мышей не наблюдалось увеличения рака при индукции теломеразы. Индукция теломеразы на самом деле может быть нашей первой линией защиты от рака, потому что молодая иммунная система регулярно избавляет организм от раковых клеток. Механизм теломеразы может эпигенетически восстанавливать клетки до состояния молодости с меньшим количеством биомаркеров генов старения. Примером может служить отключение генов, которые включаются с возрастом, таких как P53, ген, связанный с опухолью. Если бы у вас развился распространенный тип рака, как бы мы узнали, связано ли это с генной терапией или потому, что вы все равно заболели бы им? ЛП: Если бы мне поставили диагноз рака, мы могли бы секвенировать этот рак, чтобы увидеть если бы у него была дополнительная копия гена-мишени [из генной терапии]. Итак, вы получаете генную терапию теломеразы, а также ингибитор миостатина. Обсуждались ли преимущества одновременного предоставления вам двух экспериментальных методов лечения? Представьте, что это 209 год6, вам 120+, вы выглядите и чувствуете себя точно так же, как сегодня, и у вас химический состав крови как у 25-летнего. Как бы мы узнали, какая терапия привела к этому? ЛП: Такой удивительный результат, если бы он случился, обязательно был бы связан с обеими этими двумя терапиями или более. Мы считаем, что эти два типа терапии синергичны и будут приносить пользу друг другу таким образом, чтобы максимизировать результат.
Примером может служить отключение генов, которые включаются с возрастом, таких как P53, ген, связанный с опухолью. Если бы у вас развился распространенный тип рака, как бы мы узнали, связано ли это с генной терапией или потому, что вы все равно заболели бы им? ЛП: Если бы мне поставили диагноз рака, мы могли бы секвенировать этот рак, чтобы увидеть если бы у него была дополнительная копия гена-мишени [из генной терапии]. Итак, вы получаете генную терапию теломеразы, а также ингибитор миостатина. Обсуждались ли преимущества одновременного предоставления вам двух экспериментальных методов лечения? Представьте, что это 209 год6, вам 120+, вы выглядите и чувствуете себя точно так же, как сегодня, и у вас химический состав крови как у 25-летнего. Как бы мы узнали, какая терапия привела к этому? ЛП: Такой удивительный результат, если бы он случился, обязательно был бы связан с обеими этими двумя терапиями или более. Мы считаем, что эти два типа терапии синергичны и будут приносить пользу друг другу таким образом, чтобы максимизировать результат.

 У человека будут регенерироваться внутренние органы и ткани
У человека будут регенерироваться внутренние органы и ткани