Содержание
Как живут люди с искусственным сердцем в Казахстане
https://ru.sputnik.kz/20180803/iskusstvennoye-serdce-kazakhstan-6694676.html
Как живут люди с искусственным сердцем в Казахстане
Как живут люди с искусственным сердцем в Казахстане
Двое мужчин с искусственным сердцем из Актюбинской области прибыли в Астану в ожидании пересадки «живого» органа. 03.08.2018, Sputnik Казахстан
2018-08-03T18:12+0600
2018-08-03T18:12+0600
2022-09-26T16:00+0600
/html/head/meta[@name=’og:title’]/@content
/html/head/meta[@name=’og:description’]/@content
https://sputnik.kz/img/153/20/1532047_0:0:3077:1738_1920x0_80_0_0_9cbf2c186239dc96bc4fcccd1b8a96ed.jpg
астана
Sputnik Казахстан
+74956456601
MIA „Rosiya Segodnya“
2018
Sputnik Казахстан
+74956456601
MIA „Rosiya Segodnya“
Новости
ru_KK
Sputnik Казахстан
media@sputniknews. com
com
+74956456601
MIA „Rosiya Segodnya“
1920
1080
true
1920
1440
true
https://sputnik.kz/img/153/20/1532047_0:0:3077:1934_1920x0_80_0_0_8e2e75ac955e8adb4c967f8edbb46522.jpg
1920
1920
true
Sputnik Казахстан
+74956456601
MIA „Rosiya Segodnya“
Sputnik Казахстан
общество , астана
общество , астана
АСТАНА, 3 авг — Sputnik. До недавнего времени трое из десяти в мире людей с искусственным сердцем жили в Казахстане. Одному из них, Кунанбаю Абраеву из Павлодарской области в среду, 1 августа, была успешно проведена операция по замене рукотворного «мотора» на донорский орган.
Еще двое ждут своей очереди — Алексей Чабан из Петропавловска и Амангали Токов из Актюбинской области. Искусственные сердца им имплантировали в Астане.
© Photo : elorda.infoАмангали Токов
Амангали Токов
© Photo : elorda. info
info
Можно ли прожить жизнь с искусственным сердцем?
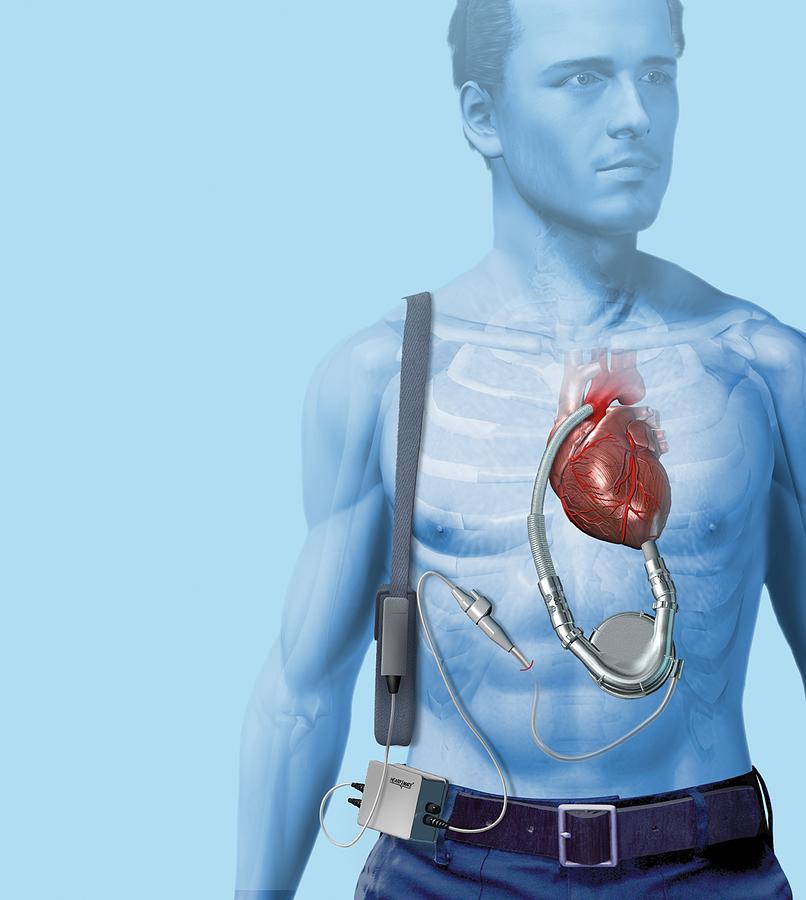
Искусственное сердце — это временный прибор, который устанавливается пациенту, нуждающемуся в пересадке сердца до момента имплантации настоящего человеческого донорского органа.
Искусственное сердце на донорское заменили пациенту казахстанские врачи
«Искусственное сердце CARMAT физиологически не отличается от человеческого сердца. Когда пациенты выполняют физическую нагрузку, частота сокращений аппарата увеличивается. И когда человек волнуется, это сердце реагирует как живое. Самый главный результат после имплантации искусственного сердца, что человеку не только продлили жизнь, но и улучшили ее качество», — цитирует Елорда Инфо первого заместителя председателя правления Национального научного кардиохирургического центра Махаббат Бекбосынову.
Врачи отмечают, что до операции все трое пациентов находились в терминальной стадии сердечной недостаточности и могли умереть в любой момент. После операции пациенты поправились и готовы к выписке домой.
После операции пациенты поправились и готовы к выписке домой.
Могут ли люди «без сердца» путешествовать на большие расстояния?
Пациенты вполне могут преодолевать большие расстояния. Алексею Чабану придется преодолеть 500 километров, чтоб вернуться в Петропавловск.
Столичные врачи подготовили персонал на родине пациента, чтобы мужчину могли грамотно вести и оказывать необходимую помощь.
Можно ли людям с искусственным сердцем заниматься спортом?
Нурлан Нигматулин перенес операцию на сердце
Врачи не только разрешили пациентам физнагрузки. К примеру, Алексей Чабан выполняет силовые упражнения с гантелями.
«Жизнь со спортом комфортная, поэтому не смог ограничить себя. Поначалу к звуку искусственного сердца тяжело привыкнуть, ты его постоянно слышишь. Но человек привыкает ко всему. Планирую жить дальше — работа, спорт, семья, все, как у нормальных людей», — поделился он с Елорда Инфо.
© Photo : elorda. infoАлексей Чабан
infoАлексей Чабан
Алексей Чабан
© Photo : elorda.info
Как выглядит искусственное сердце и есть ли у него батарейки?
Искусственное сердце CARMAT — французская разработка, в которой принимал участие европейский аэрокосмический и оборонный концерн Airbus SE. Это биопротез весом в килограмм, которое может заменить человеческое сердце.
Шестилетний мальчик перед смертью захотел стать донором
Оно работает от аккумуляторов, которые пациент носит с собой в специальной сумке.
Когда первый казахстанец получил искусственное сердце?
Первая операция по имплантации полностью искусственного сердца прошла в кардиохирургическом центре в Астане 19 октября 2017 года. Пациентом стал Кунанбай Абраев, страдавший от хронической бивентрикулярной сердечной недостаточности в терминальной стадии. Ровно через неделю после операции мужчине исполнилось 60 лет.
Адвокат рассказал о черном рынке донорских органов в Казахстане
Еще через восемь месяцев, 19 июня 2018 года, пациенту сделали ортотопическую трансплантацию сердца — промежуточную операцию в качестве подготовки к пересадке донорского органа. И, как говорилось ранее, 1 августа пациент получил «новое» сердце.
И, как говорилось ранее, 1 августа пациент получил «новое» сердце.
В Казахстане впервые пересадили печень от несовместимого донора
Искусственное сердце >
Искусственное сердце или искусственные желудочки применяются у больных в терминальной стадии сердечной недостаточности для спасения их жизни и поддержки кровообращения до того момента, когда найдется подходящей для пересадки сердца донорский орган. У некоторых больных с противопоказаниями для пересадки сердца (возраст, сопутствующие заболевания и т.д.) искусственное сердце (в нашем Центре мы используем системы типа HeartWare, или HeartMate 3) может быть имплантировано как окончательный вариант.
В нашем Центре осуществляется самая большая в мире программа по имплантации систем долгосрочной искусственной поддержки кровообращения. В нашем Центре в настоящее время после имплантации искусственного сердца более 1000 пациентов наблюдались или ещё наблюдаются уже более года и более 300 пациентов свыше трёх и более 100 лет свыше пяти лет. Эти больные находятся в кругу семьи или работают по своей прежней специальности. В редких случаях, особенно после операций на ослабленном сердце или при остром массивном инфаркте миокарда, в течение нескольких дней применяется кратковременная механическая поддержка ослабевшего сердца с помощью системы Impella.
Эти больные находятся в кругу семьи или работают по своей прежней специальности. В редких случаях, особенно после операций на ослабленном сердце или при остром массивном инфаркте миокарда, в течение нескольких дней применяется кратковременная механическая поддержка ослабевшего сердца с помощью системы Impella.
В Центре регулярно обучаются врачи из разных клиник Европы и Америки. Мы проводим сертифицированные курсы повышения квалификации и обучения применению новых систем для хирургов, кардиологов и перфузионистов из центров, начинающих программы имплантации искусственных желудочков. Международный конгресс, который организует наша клиника один раз в два года, является одним из самых крупных и посещаемых конгрессов по этой теме в мире. На базе Центра действует европейский банк данных по применению долгосрочной механической поддержки кровообращения.
В общей сложности со дня основания Центра до 1 мая 2019 г. различные типы искусственного сердца были использованы у 2715 больных. У 481 больных была впоследствии успешно произведена пересадка сердца, у 263 пациентов искусственное сердце было удалено после того, как собственное сердце восстановило свою работу. У больных с противопоказаниями для пересадки сердца (в основном у больных старше 65 лет) искусственный желудочек имплантируется в качестве окончательной терапии. В настоящее время более 40 % наших пациентов, находящихся на искусственном желудочке, старше 60 лет (см. рис. 20). Таким образом, искусственное сердце является наряду с пересадкой донорского одним из самых эффективных методов лечения пациентов в конечной стадии сердечной недостаточности в любом возрасте. В нашей клинике по состоянию на 1 мая 2019 г. у более 500 больных искусственное сердце было имплантировано на постоянной основе. В настоящее время почти 400 больных наблюдаются после вживления искусственных желудочков различных типов в нашем Центре: часть из них уже выписана домой, другие ожидают выписки. Некоторые больные настолько остались довольны результатами операции и улучшением качества своей жизни, что отказались от дальнейшей пересадки сердца.
У 481 больных была впоследствии успешно произведена пересадка сердца, у 263 пациентов искусственное сердце было удалено после того, как собственное сердце восстановило свою работу. У больных с противопоказаниями для пересадки сердца (в основном у больных старше 65 лет) искусственный желудочек имплантируется в качестве окончательной терапии. В настоящее время более 40 % наших пациентов, находящихся на искусственном желудочке, старше 60 лет (см. рис. 20). Таким образом, искусственное сердце является наряду с пересадкой донорского одним из самых эффективных методов лечения пациентов в конечной стадии сердечной недостаточности в любом возрасте. В нашей клинике по состоянию на 1 мая 2019 г. у более 500 больных искусственное сердце было имплантировано на постоянной основе. В настоящее время почти 400 больных наблюдаются после вживления искусственных желудочков различных типов в нашем Центре: часть из них уже выписана домой, другие ожидают выписки. Некоторые больные настолько остались довольны результатами операции и улучшением качества своей жизни, что отказались от дальнейшей пересадки сердца.
Вы можете посмотреть фильм, который демонстрирует имплантацию искусственнoго левого желудочка сердца типа HeartWare HVAD. Операцию проводят ведущие кардиохирурги клиники Евгений Потапов и Томас Крабач. Операция проводится через малоинвазивный доступ без вскрытия грудины и без применения аппарата искусственного кровообращения (АИК). Операция длится менее 2,5 часов, больной выписывается домой через 10 дней. Показанная техника разработана и внедрена в клиническую практику в ведущим кардиохирургом клиники Евгением Потаповым и является стандартной операцией в Берлине.
Один из пациентов с искусственным левым желудочком тренируется на роликовых коньках. Он поставил себе задачу пробежать на роликовых коньках марафонскую дистанцию. В сентябре 2014 г. пациент дал развернутое интервью одному из немецких телевизионных каналов. Это интервью (на немецком языке) вы можете посмотреть здесь. В 2017 году пациенту была успешно проведена пересадка сердца.
Средний возраст наших пациентов с искусственным сердцем чуть меньше 55 лет, более 500 больных были старше 70 лет и трое старше 80 лет во время имплантации искусственного сердца (см. рис. 15б).
рис. 15б).
Особое место занимает применение искусственного сердца у детей. В нашем Центре разработана и успешно имплантируется пациентам система BerlinHeart. Эта система может применяться у новорождённых с весом от 2000 граммов. Более 180 детей получили искусственное сердце в нашем Центре. На основании нашего опыта искусственное сердце в детской модификации pediatric Berlin Heart Excor и методика его применения, разработанные у нас, с успехом применяются во всём мире. Более 1500 операций было сделано в США и в
Канаде, есть опыт применения в странах Европы и Азии. Единственному ребёнку, получившему искусственное сердце нашей разработки в Бакулевском институте в Москве, была успешно произведена пересадка донорского сердца в Италии.
Ниже в таблице приведены типы искусственных сердец, применяемых в нашем Центре с 1986 года
| Рис. 1. Модель 1986 г. BerlinHeart искусственного сердца | Рис.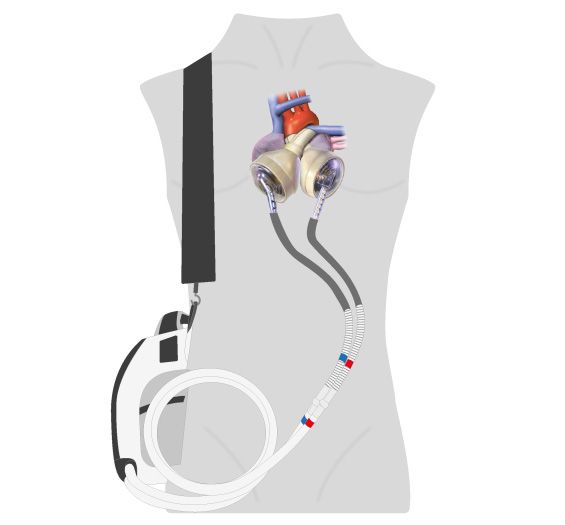 2. Первая операция по имплантации искусственного сердца проведена в 1987 г. 2. Первая операция по имплантации искусственного сердца проведена в 1987 г. | Рис. 3. Искусственные желудочки BerlinHeartt Excor |
На рис. 1 показана модель искусственного сердца, разработанного в Берлине. Эта модель была впервые имплантирована профессором Хетцером в 1987 г. (рис. 2). Всего было проведено две успешные операции. После этого удачного опыта Центр перешел на вживление искусственных желудочков фирмы BerlinHeart, показанных на рис. 3.
| Рис. 4. Схема работы искусственного желудочка | Рис. 5. Искусственный желудочек |
В 1998 г. впервые в мире был имплантирован искусственный желудочек с принципиально новым принципом действия, сконструированный при участии специалистов NASA и Майкла ДеБейки. Этот маленький насос массой всего 93 грамма способен перекачивать до 6 – 7 литров крови в минуту и тем самым обеспечивать нормальную жизнедеятельность всего организма (рис. 4 и 5).
4 и 5).
В 2002 г. в нашем Центре был также впервые был имплантирован миниатюрный искусственный желудочек ИНКОР с магнитными опорами.
| Рис. 6. Левосторонний искусственный желудочек ИНКОР с блоком управления | Рис. 7. Левосторонний искусственный желудочек ИНКОР | Рис. 8. Проф. Хетцер с первыми двумя больными через несколько дней после операции |
На рис. 6 левосторонний искусственный желудочек ИНКОР показан вместе с находящимися снаружи блоком управления и двумя аккумуляторами. На рис. 7 эта система представлена отдельно. Она способна перекачивать до 10 литров крови в минуту при потребляемой мощности около 4 – 5 Вт.
Благодаря магнитной опоре турбины трение и износ деталей отсутствуют.
Рис. 9. Трехмерная реконструкция компьютерной томографии. Впускающая канюля подшита к верхушке сердца, а выпускающая – к нисходящей части грудной аорты Впускающая канюля подшита к верхушке сердца, а выпускающая – к нисходящей части грудной аорты | Рис. 10. ИНКОР показан в момент операции |
| Рис. 11. Больной после вживления искусственного левого желудочка типа MicroMed DeBakey на своей прежней работе в качестве владельца фирмы по уборке помещений. На левом боку хорошо видна маленькая сумка с батареями и управляющим блоком | Рис. 12. Д-р Е. Потапов и пациент с искусственным левым желудочком (тип HeartMate II) во время семинара по обучению командиров отрядов специального назначения берлинской полиции. Ежегодные семинары знакомят руководящий состав берлинской полиции с особенностями больных, находящихся на искусственной поддержке кровообращения. |
Рис. 13.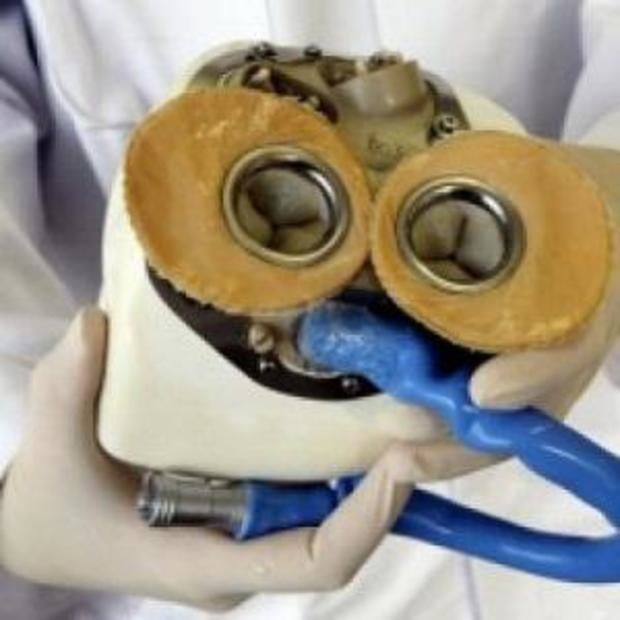 Схема имплантации двух насосов HeartWare в качестве бивентрикулярной поддержки Схема имплантации двух насосов HeartWare в качестве бивентрикулярной поддержки | а) Вид спереди | б) Вид сбоку |
| Рис. 14. Рентгеновский снимок пациента с бивентрикулярной поддержкой типа HeartWare | ||
Рис. 15 а
Рис. 15 б
Самая последняя модель искусственного желудочка HeartMate 3 (рис. 15 а), в разработке и тестировании которого принимали участие ведущие кардиохирурги нашей клиники д-р Е. Потапов и д-р Т. Крабач. Насос показан во время операции непосредственно после имплантации в верхушку левого желудочка.
Этот насос может применяться также в качестве бивентрикулярной поддержке кровообращения. Данный вариант как компьютерная томография показан на рис. 15 б.
1 – насос HeartMate 3, имплантированный в правое предсердие для поддержки малого круга кровообращения
2 – протез, огибающий корень легкого и подсоединенный к легочной артерии
3 – анастомоз с дополнительным протезом меньшего диаметра
4 – насос HeartMate 3, имплантированный в стандартной технике в верхушку левого желудочка для поддержки большого круга кровообращения
Рис. 16а. Больная после операции имплантации BVAD типа HeartWare. Пациентка держит в одной руке сумку с управляющим блоком. Другую сумку держит д-р Евгений Потапов 16а. Больная после операции имплантации BVAD типа HeartWare. Пациентка держит в одной руке сумку с управляющим блоком. Другую сумку держит д-р Евгений Потапов | Рис. 16б. Слева сидит 82-летний больной с левосторонней поддержкой (тип HeartWare), в середине показана 81-летняя женщина с левосторонней поддержкой (тип Jarvik 2000) и справа 77-летний больной с Heartassist5 |
Рис. 17 Наши пациенты во время занятий спортом, дома и на досуге
В настоящее время более 300 больных находятся на искусственной поддержке кровообращения, многие из них больше двух лет. Срок службы искусственного сердца не ограничен, некоторые пациенты живут уже более 8 лет. Подавляющее большинство пациентов с искусственным сердцем находятся дома и ведут активный образ жизни.
Рис. 18. В настоящее время более 300 больных находятся на искусственной поддержке кровообращения, многие из них больше 5 лет.
Около 20 % больных с дилатативной кардиомиопатией, которые находятся на искусственном желудочке, показывают тенденцию к улучшению функции сердца. Примерно у половины из них функция своего сердца настолько хорошо и долгосрочно восстанавливается, что они больше не нуждаются в искусственном сердце. В нашем Центре у более, чем 100 больных в подобных случаях искусственный желудочек был удален, и хорошая функция собственного сердца сохраняется годами. Для упрощения удаления искусственного желудочка сердца в нашем Центре была разработана специальная методика. Мы используем нами разработанные специальные титановые заглушки. После удаления искусственного желудочка и закрытия дефекта с помощью титановой заглушки его поверхность за 6 месяцев полностью покрывается соединительной тканью. Подробности вы можете прочитать в статье, опубликованной в журнале „Journal of Heart and Lung Transplantation“. Подобная операция была успешно проведена больному из России. После почти года на механической поддержке кровообращения собственное сердце больного восстановилось, и искусственное сердце было удалено с помощью разработанной в нашем Центре титановой заглушки.
Недавно в нашем Центре была разработана и успешно применена у более чем 5о больных методика имплантации левостороннего насоса в качестве бивентрикулярной поддержки. У больных с бивентрикулярной недостаточностью мы имплантируем после определенной модификации внутри перикарда два насоса типа HeartWare или HeartWare 3 (рис. 15а). Если раньше больным приходилось тянуть за собой тележки с компрессором весом 20 кг, и у них на животе снаружи тела находились 2 искусственных желудочка, то сейчас подобные больные носят две сумки через плечо (обе по 2,5 кг), соединенных тонким кабелем с насосами внутри грудной клетки. Схема имплантации показана на рис. 13 и 14, 15а, а больная – после операции на рис. 16а. Более подробную информацию Вы можете прочитать в статье д-ра Потапова.
Рис. 19. Титульная страница журнала „Journal of Heart and Lung Transplantation“ с фотографиями операции по удалению искусственного желудочка и имплантации пробки, проведенной в нашем Центре после восстановления собственной функции левого желудочка. Подобные операции проводят под руководством директора клиники проф. Хетцера старшие врачи клиники доктора Крабатч и Потапов Подобные операции проводят под руководством директора клиники проф. Хетцера старшие врачи клиники доктора Крабатч и Потапов | |
| Рис. 20 а | Рис. 20 б |
| Рис. 20. Рентгеновские снимки больного до и после удаления искусственного желудочка сердца. На первом снимке (а) видно искусственное сердце HeartMate II, на втором (б) – титановая заглушка, разработанная в нашем Центре | |
Рис. 21. Развитие программы механической поддержки кровообращения в нашем центре. Количество имплантаций систем постоянно возрастает. Три четверти из них составляют полностью имплантируемые системы для долгосрочной поддержки кровообращения.
Рис. 22. Более 40 % наших пациентов, находящихся на искусственном желудочке, старше 60 лет
Рис. 23. Приват-доцент Е.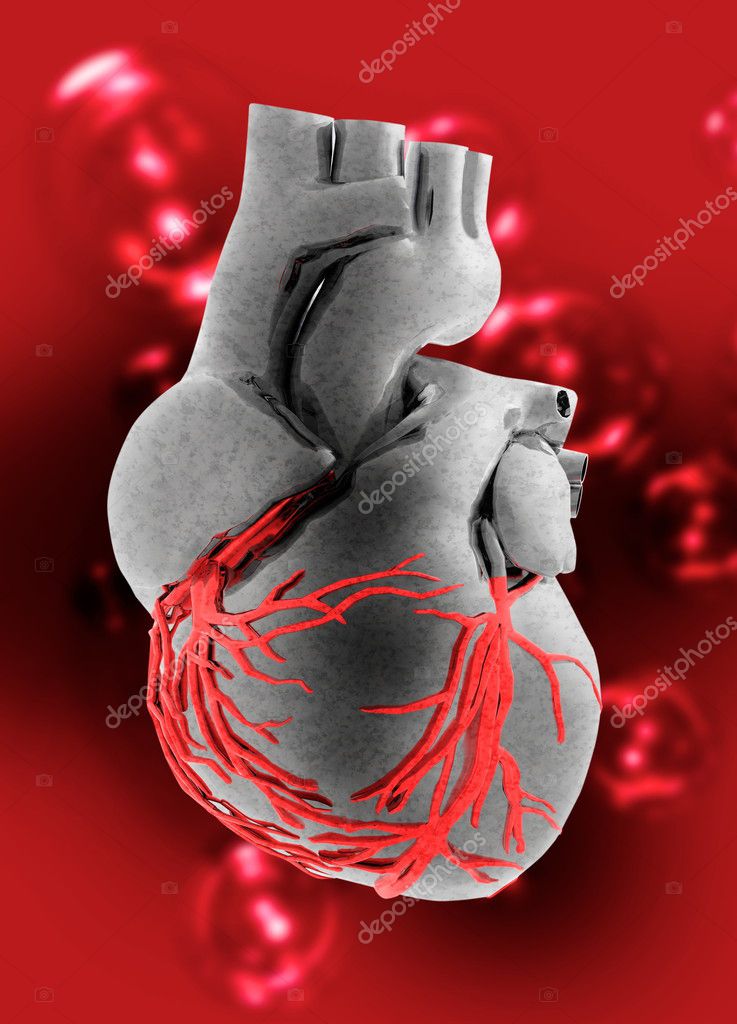 Потапов и его пациент Олег Малхов, председатель всегерманского профсоюза работников полиции
Потапов и его пациент Олег Малхов, председатель всегерманского профсоюза работников полиции
Различные типы искусственного сердца, использованные в Немецком Кардиологическом Центре в Берлине по состоянию на 1 мая 2018 г.
| Тип искусственного сердца | Длительность применения | Конфигурация | Тип кровотока | Положение | Число систем |
| Bücherl Heart | Длительное | TAH | Пульсирующий | Внутри тела | 2 |
| Berlin Heart* | Длительное | BVAD/RVAD/LVAD | Пульсирующий | Рядом с телом | 786 |
| Novacor LVAS | Длительное | LVAD | Пульсирующий | Внутри тела | 116 |
| TCI (HeartMate) | Длительное | LVAD | Пульсирующий | Внутри тела | 23 |
| Комбинация* | Длительное | BVAD | Оба | Оба | 325 |
| MicroMed* DeBakey | Длительное | LVAD | Постоянный | Внутри тела | 47 |
| Abiomed BVS 5000 | Короткое | BVAD/RVAD/LVAD | Пульсирующий | Рядом с телом | 47 |
| Hemopump | Короткое | LVAD | Постоянный | Рядом с телом | 32
|
| Biomedicus | Короткое | BVAD/RVAD/LVAD | Постоянный | Рядом с телом | 26 |
| Arrow LionHeart | Длительное | LVAD | Пульсирующий | Внутри тела | 6 |
| Impella* | Короткое | BVAD/RVAD/LVAD | Постоянный | Внутри тела | 117 |
| Incor* | Длительное | LVAD | Постоянный | Внутри тела | 214 |
| CardioWest TAН* | Длительное | TAH | Пульсирующий | Внутри тела | 53 |
| DuraHeart | Длительное | LVAD | Постоянный | Внутри тела | 18 |
| CorAid | Длительное | LVAD | Постоянный | Внутри тела | 1 |
| HeartMate II* | Длительное | LVAD | Постоянный | Внутри тела | 244 |
| HeartMate III* | Длительное | LVAD | Постоянный | Внутри тела | 153 |
| Levitronix* | Короткое | BVAD/RVAD/LVAD | Постоянный | Рядом с телом | 434 |
| Jarvik 2000 | Длительное | LVAD | Постоянный | Внутри тела | 13 |
| Ventrassist | Длительное | LVAD | Постоянный | Внутри тела | 4 |
| HeartWareHVAD* | Длительное | BVAD/RVAD/LVAD | Постоянный | Внутри тела | 953 |
| C-Puls* | Длительное | LVAD | Постоянный | Внутри тела | 6 |
| Сirculite | Длительное | LVAD | Постоянный | Внутри тела | 1 |
| Всего: | 33307 | ||||
| * – системы, применяемые в настоящее время | |||||
6 ноября 2005 г. В РНЦХ РАМН проведена уникальная кардиохирургическая операция “имплантация искусственных желудочков сердца” (Implantation of the BVAD) больному в терминальной стадии кардиомиопатии.
В РНЦХ РАМН проведена уникальная кардиохирургическая операция “имплантация искусственных желудочков сердца” (Implantation of the BVAD) больному в терминальной стадии кардиомиопатии.
Вы также можете прочитать на эту тему следующие доклады.
“Новые параметры для определения индивидуальной стратегии лечения больных с терминальной сердечной недостаточностью” приват-доцента д-ра мед. кардиохирурга Евгения Потапова.
“Стволовые клетки и механическая поддержка кровообращения” д-ра Бориса Нассери, прочитанный в ноябре 2006 г. на конгрессе, посвящённому 20-летнему юбилею Немецкого Кардиологического Центра в Берлине.
“Механическая поддержка кровообращения”. Проект в рамках сотрудничества между DHZB
и ВГМА им. Н. Н. Бурденко
Профилактика и лечение инфекции чрезкожного кабеля у больных с длительной механической поддержкой кровообращения. Е. Потапов, Р. Хетцер и рабочая группа по пересадке сердца и МПК Немецкого Кардиологического Центра в Берлине.
“Лечение больных в терминальной стадии хронической сердечной недостаточности с помощью механической поддержки кровообращения”. Лекция прочитана д-ром Потаповым 6 декабря на заседании российского общества сердечно-сосудистой недостаточности.
Немецкий кардиологический Центр в Берлине совместно с Академией натуральных наук (Academy of Life Sciences) предлагают стажировку в Немецком кардиологическом Центре в Берлине по теме “Механическая поддержка кровообращения и замена сердца”.
Более подробную информацию вы получите на странице Академии. Стажировка предназначена для врачей и перфузионистов вне зависимости от страны пребывания и рассчитана на 2 года работы в Центре. Стипендия составляет 2500 евро в месяц. Запросы направляйте, пожалуйста, на английском или немецком языках по адресу http://www.lifesciences.net/programs/mcshr.html
Вы можете прочитать доклад , сделанный прив.-доц., д-ром мед. Потаповым Е. в Москве 30.03. 2016 г.
“Хирургическое лечение сердечной недостаточности”
Рис. 25. Обложка доклада
25. Обложка доклада
65 лет первой операции с аппаратом искусственного кровообращения
65 лет назад была проведена первая операция с использованием аппарата искусственного кровообращения. «Газета.Ru» рассказывает, как создавалось само устройство, а также о первых успехах и неудачах ученых в опытах с ним.
Искусственное кровообращение позволяет поддерживать кровоток в организме или отдельном органе. Впервые мысль о возможности «сохранить в живом состоянии любую часть человеческого организма» с помощью искусственного кровообращения высказал французский физиолог Жюльен Легаллуа в 1812 году.
Сам он не решился проверить такое смелое заявление, но его идея дала старт медицинским экспериментам в этой области.
В 1857 году французский врач Шарль Броун-Секар отрезал голову собаке, чтобы проверить, сможет ли он заставить ее функционировать, вводя в артерию обогащенную кислородом кровь с помощью шприца. После того, как был запущен искусственный кровоток, через несколько минут врач зафиксировал движения глаз и мыщц.
Самый первый аппарат искусственного кровообращения был разработан в 1885 году австрийским врачом Максимиллианом фон Фреем в сотрудничестве с другим австрийцем, ученым Максом фон Грубером.
Стеклянный цилиндр играл роль легкого — в нем кровь обогащалась кислородом.
Применение такого оборудования, однако, было невозможно из-за того, что кровь свертывалась.
Прогресс наметился после открытия в 1916 году гепарина, вещества, которое предотвращало свертывание крови. В 1926 году советские ученые Сергей Брюхоненко и Сергей Чечулин разработали аппарат искусственного кровообращения (автожектор), который хорошо показал себя в экспериментах на собаках.
«Необходимо было доказать основное: центральная нервная система (которая с прекращением кровообращения перестает функционировать раньше каких-либо других систем живого организма) способна продолжить свою работу в искусственных условиях, не отличающихся в этом отношении от работы других жизненных органов», — объяснял задачу Чечулин.
Автожектор представлял собой стеклянный резервуар, в который наливалась кровь с антикоагулянтом. Кровь при помощи насосов отсасывалась из вен отсеченной головы собаки и поступала в легочную артерию изолированных легких животного, которые механически раздувались, насыщая кровь кислородом.
После этого кровь обратно возвращалась в резервуар, а оттуда — в крупные кровеносные сосуды головы, обеспечивая кровоснабжение головного мозга. Устройство автожектора обеспечивало автоматическую регуляцию нагнетания и отсасывания крови, а также ее согревания.
«Голова собаки была совершенно отделена от туловища и лежала на тарелке…
Изолированная по нашему методу голова 3 часа 24 минуты проявляет ряд тонких реакций и функций ЦНС — мигает веками на прикосновение к частям головы, при слабом дуновении, при зажигании света; делает энергичные движения при более сильных раздражениях, выделяет слюну, реагирует вспомогательными дыхательными движениями на недостаток кислорода и реагирует на разные нарушения искусственного кровообращения картиной, внешне напоминающей агонию и смерть (расширение зрачков и пр. )», — описывали исследователи свои эксперименты.
)», — описывали исследователи свои эксперименты.
close
100%
Несмотря на успехи с животными, в клинической практике устройство использовать не решались.
В июле 1952 года в США была проведена первая операция на открытом сердце, при которой использовался аппарат для искусственной перекачки крови. Американский кардиохирург и изобретатель Форест Дьюи Додрилл с помощью самостоятельно разработанного аппарата прооперировал мужчину с недостаточностью митрального клапана. Аппарат на протяжении почти часовой операции обеспечивал функции левого желудочка сердца.
«Насколько нам известно, это первый случай успешной операции на открытом сердце, в которой использовалось механическое сердце, обеспечивавшее кровоснабжение тела во время операции», — отметил Додрилл.
Но настоящим прорывом стала операция, проведенная в США 6 мая 1953 года.
Американский хирург Джек (Джон) Гиббон использовал полноценную систему обеспечения функций сердца и легких у 18-летней пациентки с сердечной недостаточностью. Произведя разрез в области подмышки, он подключил катетеры к венам и артериям. Спустя всего 26 минут Гиббон закончил операцию по устранению дефекта межпредсердной перегородки и отключил девушку от аппарата. Пациентка выжила.
Произведя разрез в области подмышки, он подключил катетеры к венам и артериям. Спустя всего 26 минут Гиббон закончил операцию по устранению дефекта межпредсердной перегородки и отключил девушку от аппарата. Пациентка выжила.
Гиббон шел к успеху не один год. В 1930-м году ему довелось лечить пациентку с тромбоэмолией — закупоркой тромбами — легочной артерии. Проводимая в таких случаях операция по иссечению участка артерии в то время почти всегда была летальной, случай пациентки Гиббона не стал исключением. Это произвело на него настолько большое впечатление, что он поставил перед собой цель — научиться улучшать состояние пациентов с такими патологиями.
Ему пришла в голову мысль перенаправлять венозную кровь из расширенных вен в аппарат, где бы кровь насыщаясь кислородом, избавлялась от углекислого газа, а затем возвращалась обратно в артерии больного.
В 1931 году Гиббон вместе с женой начали проводить подготовительные исследования по созданию аппарата искусственного кровообращения. В 1934 году им удалось добиться первых успехов: кошки с полной закупоркой легочной артерии оставались живыми на протяжении почти трех часов.
В 1934 году им удалось добиться первых успехов: кошки с полной закупоркой легочной артерии оставались живыми на протяжении почти трех часов.
Однако у аппарата еще оставались нерешенные проблемы, самыми серьезными из них были гемолиз (выход клеточного содержимого в межклеточное пространство), который развивался, когда кровь проходила через аппарат, и невозможность насыщать кислородом большие объемы крови.
Работа Гиббона над аппаратом прервалась в январе 1942 года, когда он волонтером отправился на Вторую мировую войну, где пробыл до 1945 года.
В 1946 году Гиббон вернулся к работе над аппаратом. При помощи инженеров компании IBM ему удалось создать первое устройства искусственного кровообращения, которое могло устойчиво работать непосредственно во время операций на сердце, не повреждая при этом эритроцитов и не создавая воздушных пузырей.
Самым первым пациентом Гиббона стал 15-месячный малыш, но тот погиб на операционном столе из-за неверного диагноза.
Девушка, успешно прооперированная при помощи разработки Гиббсона, была выписана из больницы уже спустя 13 дней. Через полгода она прошла через еще одну операцию, полностью устранившую дефект.
Через полгода она прошла через еще одну операцию, полностью устранившую дефект.
Последующие операции были менее удачными — четверо пациентов погибли от осложнений.
Это опустошило Гиббона и он вовсе перестал проводить операции на открытом сердце.
Тем не менее, интерес специалистов позволил развить саму технологию и сегодня оборудование, обеспечивающее жизнедеятельность человека при невозможности сердца и легких выполнять свои функции, широко используется в медицинской практике.
Как построить искусственное сердце
Фрейзер указал на большой металлический насос и на выступающий из него белый кусок трубки — «длинный вход», как он сказал. Пока это не было исправлено, оно обрекло устройство на провал. Небольшие различия, итеративно изменяемые, их последствия раскрываются только после смерти. Это было изобретение в замедленной съемке.
АбиоКор отменен. До Бивакора еще много лет. Сегодня единственная компания, производящая и продающая искусственные сердца, которые на самом деле имплантируются людям, — это SynCardia Systems в Тусоне, штат Аризона. Компания создавалась как спасательная миссия. Symbion, компания из Юты, которую помог основать Роберт Джарвик, потеряла F.D.A. одобрение сердца Jarvik-7 в 1990 из-за проблем с контролем качества; ее технология сердца была приобретена другой фирмой, которая провела десятилетние клинические испытания улучшенной версии сердца, но в 2001 году исчерпала свое финансирование. Какое-то время казалось, что технология исчезнет с лица земли. Но два кардиохирурга и инженер-биомедик собрали венчурный капитал, чтобы купить права на систему; они переименовали сердце в SynCardia Total Artificial Heart или T.A.H. Компания, базирующаяся сейчас в нескольких зданиях, окружающих песчаную автостоянку, продает где-то севернее сотни сердец в год, и все они произошли от устаревшего воздушного Jarvik-7. Хотя SynCardia преуспела в создании сети хирургов, способных установить ей сердце, бизнес компании весьма незначителен. Несколько лет назад он объявил главу 11 и был куплен новыми инвесторами. Он справился с пандемией коронавируса, которая привела к отмене операций по всей стране, за счет производства дезинфицирующего средства для рук.
Компания создавалась как спасательная миссия. Symbion, компания из Юты, которую помог основать Роберт Джарвик, потеряла F.D.A. одобрение сердца Jarvik-7 в 1990 из-за проблем с контролем качества; ее технология сердца была приобретена другой фирмой, которая провела десятилетние клинические испытания улучшенной версии сердца, но в 2001 году исчерпала свое финансирование. Какое-то время казалось, что технология исчезнет с лица земли. Но два кардиохирурга и инженер-биомедик собрали венчурный капитал, чтобы купить права на систему; они переименовали сердце в SynCardia Total Artificial Heart или T.A.H. Компания, базирующаяся сейчас в нескольких зданиях, окружающих песчаную автостоянку, продает где-то севернее сотни сердец в год, и все они произошли от устаревшего воздушного Jarvik-7. Хотя SynCardia преуспела в создании сети хирургов, способных установить ей сердце, бизнес компании весьма незначителен. Несколько лет назад он объявил главу 11 и был куплен новыми инвесторами. Он справился с пандемией коронавируса, которая привела к отмене операций по всей стране, за счет производства дезинфицирующего средства для рук.
Вместе с Карен Стамм, директором по управлению программами SynCardia, и Мэттом Шустером, инженером, я наблюдал через окно, как техник в чистой комнате собирал одно из сердец. «Ключом к созданию искусственного сердца является материал, который мы используем», — сказал Шустер. «Сегментированное полиуретановое решение. Вы услышите, как мы называем это «spuzz» — S.P.U.S. Штамм рассмеялся. «На самом деле мы производим spus здесь, в кампусе», — продолжил Шустер. «Это наша собственная запатентованная смесь. Он выходит из нашего производственного оборудования почти как сок или густой мед». Используя зубочистку, техник тщательно манипулировал слоями формованного меда. Полупрозрачное что-то перемещается по другому полупрозрачному чему-то. Процесс сборки занимает две с половиной недели.
Мы прошли через лабораторию, предназначенную для «анализа эксплантатов» — «Если мы получим сердце, мы разберем его и осмотрим», — сказал Шустер, — и вошли в другую комнату, заполненную несколькими дюжинами резервуаров с водой на полках. Внутри каждого резервуара билось сердце; рядом с баками располагались воздушные насосы или «приводы». Звук в комнате был оглушительный: быстрое, громкое тук-тук, тук-тук, , а внутри этого механический цоканье, как у пишущей машинки. Звуки повторялись два раза в секунду — индустриальный ритм, как будто мы были на фабрике по производству тиражей. — Здесь мы проводим наши долгосрочные исследования, — крикнул Штамм, перекрывая шум. С одной стороны комнаты стояли пятьдесят куб. сердца, используемые маленькими пациентами; с другой стороны, семьдесят куб.см. модели, используемые более крупными. «Вот драйвер, который представляет собой механический звук», — сказала она, указывая на механический насос, похожий на коробку для завтрака, который был соединен воздушной трубкой с сердцем внутри резервуара. «Тогда вы слышите щелк-щелк — это на самом деле клапан внутри сердца».
Внутри каждого резервуара билось сердце; рядом с баками располагались воздушные насосы или «приводы». Звук в комнате был оглушительный: быстрое, громкое тук-тук, тук-тук, , а внутри этого механический цоканье, как у пишущей машинки. Звуки повторялись два раза в секунду — индустриальный ритм, как будто мы были на фабрике по производству тиражей. — Здесь мы проводим наши долгосрочные исследования, — крикнул Штамм, перекрывая шум. С одной стороны комнаты стояли пятьдесят куб. сердца, используемые маленькими пациентами; с другой стороны, семьдесят куб.см. модели, используемые более крупными. «Вот драйвер, который представляет собой механический звук», — сказала она, указывая на механический насос, похожий на коробку для завтрака, который был соединен воздушной трубкой с сердцем внутри резервуара. «Тогда вы слышите щелк-щелк — это на самом деле клапан внутри сердца».
Привод был в центре инноваций SynCardia. Его сердце может приводиться в движение одним из двух устройств, первое размером с мини-холодильник, второе размером с тостер — оба намного меньше, чем те, которые использовали пациенты Де Вриса. Драйверы необходимо обслуживать через несколько месяцев; когда загорается сигнальная лампочка, медицинский работник отсоединяет приводную линию и как можно быстрее снова подключает ее к другому устройству, чтобы сердце пользователя не екнуло. Пока я смотрел, вода в резервуарах слегка пульсировала в ритме. нужно много удар , чтобы каждую минуту прогонять через тело пять или шесть литров крови.
Драйверы необходимо обслуживать через несколько месяцев; когда загорается сигнальная лампочка, медицинский работник отсоединяет приводную линию и как можно быстрее снова подключает ее к другому устройству, чтобы сердце пользователя не екнуло. Пока я смотрел, вода в резервуарах слегка пульсировала в ритме. нужно много удар , чтобы каждую минуту прогонять через тело пять или шесть литров крови.
«Как это на самом деле звучит в человеке?» Я попросил.
— Стало гораздо тише, — сказал Штамм. — Но ты же слышишь. Я слышал истории, в которых пациенты говорят, что если они откроют рот, то другие люди услышат щелчок». Она рассказала мне, что некоторые пациенты сначала не могли переносить шум. Но затем, по ее словам, «они не могли спать без звука ка-чанк, ка-чанк ».
Мы прошли через склад, где на полках стояло около дюжины сердец, готовых к отправке; хирургические наборы, содержащие материалы, необходимые для их установки, были упакованы в отдельную стопку. Затем мы прошли через парковку к другому зданию, где в лабораторном помещении с высоким потолком ждала группа инженеров в защитных очках. Один из них протянул мне небольшой кусочек пластика в форме песочных часов: SPUS . Прозрачный, но слегка молочный, гладкий, но липкий на кончиках моих пальцев, он был почти нереально эластичным — я потянул за его концы, растянув горловину песочных часов в несколько раз по сравнению с ее первоначальной длиной, и она без усилий вернулась к своей первоначальной форме.
Затем мы прошли через парковку к другому зданию, где в лабораторном помещении с высоким потолком ждала группа инженеров в защитных очках. Один из них протянул мне небольшой кусочек пластика в форме песочных часов: SPUS . Прозрачный, но слегка молочный, гладкий, но липкий на кончиках моих пальцев, он был почти нереально эластичным — я потянул за его концы, растянув горловину песочных часов в несколько раз по сравнению с ее первоначальной длиной, и она без усилий вернулась к своей первоначальной форме.
Через дверной проем я заметил гигантскую, изрядно поношенную машину, около дюжины футов высотой, сочетающую в себе аспекты нефтяной вышки и KitchenAid. «Реактор SPUS », — сказал Трой Виллазон, руководитель производства SynCardia. — Это начало шестидесятых. SynCardia приобрела машину в начале двадцатых годов, чтобы обеспечить стабильные поставки. «Сама техника прошла через всю историю этого материала», — сказал Вилласон. Некоторое время мы стояли и размышляли о том, использовалась ли эта самая машина при создании сердец Джарвика. «Вполне возможно», — сказал Шустер.
«Вполне возможно», — сказал Шустер.
Я остановился перед доской, на которой над обычными схемами, нарисованными от руки, были расположены четыре фотографии пациентов SynCardia. Черный мужчина на больничной койке с сумкой в руках; лысеющий белый мужчина на поле для гольфа с тонким воздушным шлангом, выходящим из-под его рубашки к клюшкам; блондин, возможно, подростка, с рюкзаком; и молодые брат и сестра сидят вместе. «Нам нравится держать мотивацию на стене», — сказал Вилласон. Девятилетний мальчик был самым молодым человеком, которому когда-либо пересадили сердце SynCardia. Самый долгоживущий пациент SynCardia использует сердце почти семь лет — достижение, которое в 1980-х годах могло бы стать прикрытием Жизнь.
Одной из самых больших проблем, с которыми сталкивается SynCardia, является устаревание. Jarvik-7, на котором основано сердце SynCardia, был разработан почти сорок лет назад; первоначальный F.D.A. разрешениям десятки лет. Сегодня замена любой отдельной части сердца — болта, клапана, резистора — может потребовать нового процесса утверждения. По мере того как поставщики прекращают свою деятельность или обновляют свои предложения, инженеры SynCardia должны искать, тестировать и затем получать одобрение на замену компонентов. Они живут в страхе перед фатальным сбоем в 9Реактор 0007 SPUS : строительство и получение разрешения на новый может занять год, в результате чего потенциальные новые пациенты останутся без сердец. Обслуживание устаревшего устройства стоит дорого. «Даже если вы не улучшаете и не меняете его, а просто продолжаете производить то же самое — люди не понимают», — сказал Шустер. «Я работал в аэрокосмической отрасли и могу сказать вам, что часто бывает проще внести серьезные изменения в аэрокосмическую оборону, чем что-то изменить в искусственном сердце». Слушая, я представил, с какой сосредоточенностью пользователи сердца должны отслеживать взлеты и падения SynCardia.
По мере того как поставщики прекращают свою деятельность или обновляют свои предложения, инженеры SynCardia должны искать, тестировать и затем получать одобрение на замену компонентов. Они живут в страхе перед фатальным сбоем в 9Реактор 0007 SPUS : строительство и получение разрешения на новый может занять год, в результате чего потенциальные новые пациенты останутся без сердец. Обслуживание устаревшего устройства стоит дорого. «Даже если вы не улучшаете и не меняете его, а просто продолжаете производить то же самое — люди не понимают», — сказал Шустер. «Я работал в аэрокосмической отрасли и могу сказать вам, что часто бывает проще внести серьезные изменения в аэрокосмическую оборону, чем что-то изменить в искусственном сердце». Слушая, я представил, с какой сосредоточенностью пользователи сердца должны отслеживать взлеты и падения SynCardia.
В Соединенных Штатах менее двадцати больниц, в которых хирурги прошли обучение установке сердца. «Это узкий рынок, — говорит Дон Уэббер, генеральный директор. компании, сказал мне. Он достал свой телефон и открыл электронную таблицу, в которой были перечислены все пациенты-кандидаты на сердце на данный момент. «У нас выходит ежедневный листок», — пояснил он. «Нам позвонят, или пришлют смс, или электронное письмо, в котором будет сказано: «У нас может быть пациент». На экране телефона прокручивались ряды пациентов с цветовой кодировкой.
компании, сказал мне. Он достал свой телефон и открыл электронную таблицу, в которой были перечислены все пациенты-кандидаты на сердце на данный момент. «У нас выходит ежедневный листок», — пояснил он. «Нам позвонят, или пришлют смс, или электронное письмо, в котором будет сказано: «У нас может быть пациент». На экране телефона прокручивались ряды пациентов с цветовой кодировкой.
«Я начинаю подозревать, что ему наплевать на нас».
Мультфильм Фрэнка Котэма
SynCardia сталкивается с той же проблемой, с которой столкнулся Кули в 1960-х: вы должны быть очень больны, чтобы подумать о том, чтобы вырезать себе сердце из груди, но если вы будете ждать слишком долго и заболеете, вас уже не спасти. «Есть дела, которые находятся там», — сказал Уэббер с тревогой в голосе. «Вы видите это в списке на этой неделе, вы видите это в списке в конце недели, вы видите это в списке на следующей неделе. Они просто ждут, и ждут, и ждут». Чем дольше пациент ждет, тем меньше у него шансов пережить имплантацию искусственного сердца и любую последующую трансплантацию. «Это не чистое решение, — сказал Уэббер. «У вас есть несколько человек в этой команде» — хирурги, кардиологи, госпиталисты, и все они должны согласиться.
«Это не чистое решение, — сказал Уэббер. «У вас есть несколько человек в этой команде» — хирурги, кардиологи, госпиталисты, и все они должны согласиться.
Бизнесмены используют множество различных метафор для описания изобретений и инноваций. Они говорят, что технологии могут развиваться непрерывно и прерывисто; что новые продукты должны подняться по «кривой принятия» или перепрыгнуть через пропасть юзабилити. Никому не нужны были мобильные телефоны, пока они не стали настолько маленькими, что всем захотелось иметь их. Электромобили казались непрактичными, но гибридные двигатели, дав водителям почувствовать вкус технологии, ускорили их внедрение.
Перед искусственным сердцем стоит уникальная задача. Только те, кто сталкивается с неминуемой смертью, готовы использовать сегодняшние модели. И все же почти шестьсот шестьдесят тысяч американцев ежегодно умирают от сердечных заболеваний — число погибших на уровне пандемии, в отношении которого мы не чувствуем особой опасности. Все большее число из нас живет с больным сердцем и страдает от последствий. Чтобы полностью реализовать свой потенциал, искусственные сердца должны быть достаточно хороши, чтобы люди действительно захотели их использовать; они должны быть предпочтительнее не смерти, а отказавшего сердца, как замена тазобедренного сустава предпочтительнее отказавших тазобедренных суставов. Между тем, пока они не получат более широкого распространения, они останутся нишевым продуктом и, следовательно, будут недоступны для многих людей, которые в них нуждаются. Еще мгновение Уэббер прокручивал свой список; Я задавался вопросом, должна ли Джесс быть на нем. Потом он убрал телефон.
Все большее число из нас живет с больным сердцем и страдает от последствий. Чтобы полностью реализовать свой потенциал, искусственные сердца должны быть достаточно хороши, чтобы люди действительно захотели их использовать; они должны быть предпочтительнее не смерти, а отказавшего сердца, как замена тазобедренного сустава предпочтительнее отказавших тазобедренных суставов. Между тем, пока они не получат более широкого распространения, они останутся нишевым продуктом и, следовательно, будут недоступны для многих людей, которые в них нуждаются. Еще мгновение Уэббер прокручивал свой список; Я задавался вопросом, должна ли Джесс быть на нем. Потом он убрал телефон.
Инженеры SynCardia отвечают за поддержание устаревшей технологии, но они также понимают, что ее необходимо развивать. Перед тем, как я уехал из Тусона, Виллазон рассказал мне о сердце нового поколения, которое разрабатывала компания SynCardia. В сердце будет использоваться новый насосный двигатель с батарейным питанием, который можно будет полностью разместить внутри пациента; как и AbioCor, он будет беспроводным, без внешнего драйвера. В то же время он будет перекачивать кровь, используя ранее существовавшие желудочки компании на основе SPUS , которые уже были одобрены FDA. Подключив этот новый двигатель к своему старому автомобилю — гибридной модели — SynCardia надеялась быстро разработать и продать сердце, а также привлечь существующих клиентов. По словам Виллазона, новое сердце может быть надежной постоянной имплантацией. Его могут использовать люди, находящиеся немного дальше от пропасти.
В то же время он будет перекачивать кровь, используя ранее существовавшие желудочки компании на основе SPUS , которые уже были одобрены FDA. Подключив этот новый двигатель к своему старому автомобилю — гибридной модели — SynCardia надеялась быстро разработать и продать сердце, а также привлечь существующих клиентов. По словам Виллазона, новое сердце может быть надежной постоянной имплантацией. Его могут использовать люди, находящиеся немного дальше от пропасти.
Я не Бад Фрейзер, но я видел много искусственных сердец, и дизайн Виллазона показался мне одновременно простым и гениальным. И все же инженеры SynCardia были заняты производством, продажей и обновлением существующего сердца, спасая более сотни жизней в год. Они изо всех сил пытались найти время, чтобы запустить новое сердце. Они напечатали на 3D-принтере несколько прототипов и присмотрелись к ним; они разговаривали с инвесторами.
Команда Bivacor в Серритосе счастливо не обременена технологическим прошлым. Когда я был там, все собирались на тайский — еженедельный обед для всей команды. Это была большая группа для ресторана, но маленькая для дизайна искусственного сердца. Тиммс сидел на одном конце стола рядом с Николасом Грейтрексом, инженером-электриком.
Когда я был там, все собирались на тайский — еженедельный обед для всей команды. Это была большая группа для ресторана, но маленькая для дизайна искусственного сердца. Тиммс сидел на одном конце стола рядом с Николасом Грейтрексом, инженером-электриком.
«Теперь, когда вы приближаетесь к тому, чтобы поместить устройство в человека, как вы себя чувствуете?» Я попросил. «Это захватывающе, или причудливо, или что?»
«Чем ближе вы подходите к тому, чтобы попасть в человека, тем больше вы думаете обо всем, что может пойти не так, и о том, что вы можете сделать», — сказал Матиас Кляйнхейер, бородатый инженер. «Даже если бы я не сомневался, что система работает так, как должна, это все равно было бы очень страшно». Кляйнхейер отвечает за резервные системы сердца; есть бэкапы на бэкапы на бэкапы.
Жить годами без сердца теперь возможно
Здоровье сердца
Автор
Кевин Джой
06 сентября 2016 г. 7:00
Устройство под названием «Тотальное искусственное сердце» помогает некоторым из самых тяжелых пациентов с сердечной недостаточностью восстановить функции — вне больницы — в ожидании трансплантации.
Звучит как побочный продукт научной фантастики: синтетическое устройство с батарейным питанием, предназначенное для замены работы самого важного органа тела.
БОЛЬШЕ ИЗ МИЧИГАНА: Подпишитесь на нашу еженедельную рассылку новостей
Но оборудование, известное как Тотальное искусственное сердце, предлагает спасательный круг для некоторых из самых тяжелых случаев сердечной недостаточности.
«Вот на что способна эволюция технологий, — говорит Джонатан Хафт, доктор медицинских наук, кардиохирург из системы здравоохранения Мичиганского университета. «На самом деле вы удаляете сердце и заменяете его».
Хафт указал на своего пациента Стэна Ларкина, изображенного выше, 25-летнего человека с редкой формой кардиомиопатии, который прожил 555 дней — вне больницы — с использованием тотального искусственного сердца, прежде чем ему сделали пересадку сердца в UMHS в мае. . «Сейчас он абсолютно процветает».
Внутренняя механика, которая заменяет оба желудочка и четыре сердечных клапана, регулируется двумя трубками, которые соединяются с портативным 13,5-фунтовым внешним воздушным насосом, который называется Freedom driver. (До одобрения водителя Freedom Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов два года назад большинству получателей приходилось полагаться на неуклюжего водителя весом 418 фунтов размером со стиральную машину, из-за чего они постоянно находились в больнице.)
(До одобрения водителя Freedom Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов два года назад большинству получателей приходилось полагаться на неуклюжего водителя весом 418 фунтов размером со стиральную машину, из-за чего они постоянно находились в больнице.)
Выпущен в 1969 году и развивающиеся с 1980-х годов, устройства не для всех.
Только левый желудочек поражается примерно у 85–90 процентов пациентов с далеко зашедшей терминальной стадией сердечной недостаточности, что дает им право на меньшую и менее инвазивную помпу, известную как вспомогательное устройство для левого желудочка (LVAD).
Однако для тех, кто столкнулся с бивентрикулярной недостаточностью, тотальное искусственное сердце является «единственным реальным вариантом», — говорит Хафт.
По сравнению с LVAD внедрение тотального искусственного сердца встречается гораздо реже.
Ежегодно в UMHS проводится от одной до семи таких операций для последнего, говорит Хафт, объясняя подробности своими словами.
Тотальное искусственное сердце SynCardia.
7 вещей, которые нужно знать о тотальных искусственных сердцах
Требуется хирургическое вмешательство: Операция мало чем отличается от пересадки сердца; где-то в районе четырех-пяти часов. Это может быть осложнено или оспорено предыдущими операциями. Если кто-то находился в больнице в течение длительного периода времени, восстановление может занять месяцы.
Они большие: Заметно больше, чем нормальное человеческое сердце. Пациенты должны пройти компьютерную томографию, чтобы определить, достаточно ли места. Это конкретное устройство имеет определенные требования к размеру в грудной полости. Для людей нормального телосложения с хронической сердечной недостаточностью обычно подходит.
СМОТРИТЕ ТАКЖЕ: Врожденное заболевание, которое приводит к «неожиданной» операции на сердце
Они обеспечивают мобильность: Водитель Freedom оснащен аккумулятором, поэтому пациенты могут быть относительно непривязанными в течение двух-трех часов. . Пациенты могут использовать резервные батареи, если им приходится покидать дом на более длительное время. Конечно, они могут подключаться к розетке, когда это необходимо.
. Пациенты могут использовать резервные батареи, если им приходится покидать дом на более длительное время. Конечно, они могут подключаться к розетке, когда это необходимо.
Они могут быть громоздкими: Внешний контроллер большой и тяжелый. Это бремя, которое люди должны нести все время. Это очень, очень шумно. Другое ограничение состоит в том, что два больших шланга, выходящих из корпуса, могут быть громоздкими и потенциально болезненными.
Они несут в себе риски: Проблема № 1 – заражение … (через) прокол кожи (для шлангов), через который могут попасть микробы. При огромном количестве поверхности раздела между кровью и инородной поверхностью существуют опасности образования тромбов внутри тела. А если пациент принимает препараты для разжижения крови, у него могут развиться геморрагические осложнения.
Они временные: Существуют проблемы с долгосрочной поддержкой, поэтому она предназначена для пациентов, имеющих право на трансплантацию, или тех, кого мы намерены провести трансплантацию, как только они получат право на трансплантацию. Для устройства нет конкретных ограничений по времени, а долговечность и риск осложнений с течением времени остаются неизвестными.
Для устройства нет конкретных ограничений по времени, а долговечность и риск осложнений с течением времени остаются неизвестными.
Они развиваются: Помпа объемом 70 мл (объем крови, заполняющий устройство) имеет ограничения по размеру. Вы не можете имплантировать его кому-то очень маленькому или людям с сердцем нормального размера. Исследуемая помпа объемом 50 куб. см, которая в настоящее время проходит клинические испытания, может повысить пригодность для маленьких людей и женщин.
Другие статьи о:
Операция по пересадке сердца
,
Новые технологии
,
Сердечно-сосудистые заболевания: лечение и хирургия
,
TweetSharePinShareEmailShare
Это сердце на маглеве может сохранить жизнь пациентам с сердечно-сосудистыми заболеваниями
..»> Элегантная простота: искусственное сердце Bivacor представляет собой центробежный насос с одной движущейся частью — вращающимся диском, который подвешен в корпусе с помощью магнитной левитации. Фото: Питер Адамс
Более 50 лет кардиохирурга и инженера-биомедика из Техасского института сердца (THI) искали искусственное сердце, которое могло бы полностью заменить естественные, которых катастрофически не хватает. для пересадки. Они видели свою долю металлических и пластиковых приспособлений, в которых использовались различные насосные механизмы, но ни одна из этих машин не могла сравниться с поразительной производительностью человеческого сердца.
Изобретатель: Дэниел Тиммс, основатель Bivacor, держит в руках 650-граммовую машину, которая может спасти жизни мужчин, женщин и детей с сердечной недостаточностью. ..»> Фото: Питер Адамс
В апреле 2019 года возможной кульминацией этого долгого квеста стала лохматая коричневая корова, мирно жующая жвачку в исследовательском центре THI в Хьюстоне. Животное участвовало в 90-дневном испытании, в ходе которого оно прожило свою жизнь с имплантированным искусственным сердцем, изготовленным нашей компанией Bivacor. На протяжении всего испытания теленок оставался здоровым и энергичным и набирал вес с нормальной скоростью. Он даже бегал на беговой дорожке по 30 минут.
В настоящее время наша компания работает над испытаниями нашего устройства на людях. Он основан на совершенно новом подходе: вместо механического насоса, который имитирует структуру и работу четырехкамерного человеческого сердца, используется вращающийся диск, подвешенный в магнитном поле. С помощью всего лишь одной подвижной части сердце Bivacor может отправлять богатую кислородом кровь в организм и возвращать обедненную кислородом кровь в легкие.
Нам пришлось преодолеть множество технических проблем, чтобы сделать искусственное сердце небольшим, биосовместимым, энергоэффективным и долговечным.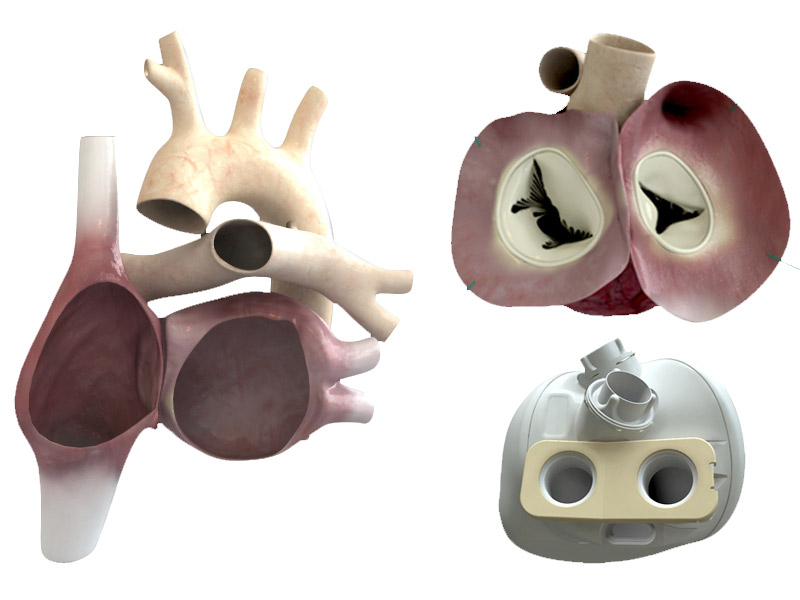 Учтите, что человеческое сердце бьется примерно 112 000 раз в день, что в сумме составляет 42 миллиона раз в год, и вы поймете масштаб проблемы.
Учтите, что человеческое сердце бьется примерно 112 000 раз в день, что в сумме составляет 42 миллиона раз в год, и вы поймете масштаб проблемы.
На данный момент мы протестировали сердце Бивакор на 15 коровах. Хотя необходимость испытаний на животных вызывает сожаление, это единственный способ доказать безопасность устройства и перейти к клиническим испытаниям на людях. Эти телята Corriente, которые относительно малы, имеют правильный размер, чтобы служить аналогами для взрослых пациентов. Мы также имплантировали сердце Бивакор нескольким овцам, которые больше подходят для пациентов с меньшими размерами тела, включая детей. Наши тесты показали, что сердце хорошо держится: поскольку его единственная движущаяся часть левитирует в магнитном поле, можно не беспокоиться о том, что трение и механический износ приведут к выходу машины из строя. Наши тесты также показали, что устройство может адаптироваться к потребностям сердечно-сосудистой системы пользователя.
Один из нас, основатель компании Bivacor Тиммс, начал работать над этим проектом 18 лет назад. [Для получения дополнительной информации о его личной истории см. «Изобретатель искусственного сердца был вдохновлен своим отцом-водопроводчиком».] На протяжении многих лет центральная концепция сердца на магнитной подвеске оставалась неизменной, хотя наша команда инженеров значительно усовершенствовала технологию. Мы очень рады, что устройство почти готово для испытаний на людях, потому что мы считаем, что сердце Бивакор — это решение, которого давно ждали тяжелобольные пациенты с сердечной недостаточностью.
[Для получения дополнительной информации о его личной истории см. «Изобретатель искусственного сердца был вдохновлен своим отцом-водопроводчиком».] На протяжении многих лет центральная концепция сердца на магнитной подвеске оставалась неизменной, хотя наша команда инженеров значительно усовершенствовала технологию. Мы очень рады, что устройство почти готово для испытаний на людях, потому что мы считаем, что сердце Бивакор — это решение, которого давно ждали тяжелобольные пациенты с сердечной недостаточностью.
При сердечной недостаточности сердце не может перекачивать достаточное количество крови, чтобы тело было здоровым и сильным. По крайней мере, 26 миллионов человек во всем мире живут с этой болезнью, и их число растет по мере старения населения. Пациенты с тяжелой сердечной недостаточностью имеют мрачные перспективы: лучший вариант для них — пересадка сердца, но ограниченное количество донорских сердец означает, что только около 5000 пациентов во всем мире получают трансплантацию каждый год. Еще тысячи пациентов имеют право на трансплантацию, и некоторые из них умирают в ожидании донорского органа.
Еще тысячи пациентов имеют право на трансплантацию, и некоторые из них умирают в ожидании донорского органа.
На рабочем месте: в инженерной лаборатории Бивакора Тиммс возится с частями последнего прототипа искусственного сердца. Фото: Питер Адамс
Кардиологи давно мечтают о механической замене. В 1969 году врач THI Дентон Кули имплантировал первое «полное искусственное сердце» пациенту, ожидавшему трансплантации, что позволило ему прожить в течение 64 часов, необходимых для доставки донорского органа. Однако этот пациент умер вскоре после операции по трансплантации от инфекции, и команда Кули отложила устройство на полку из-за опасений по поводу надежности и совместимости с человеческим телом.
Альтернативная анатомия: левая сторона помпы заменяет анатомический левый желудочек сердца, направляя обогащенную кислородом кровь (красного цвета) в самые отдаленные уголки тела.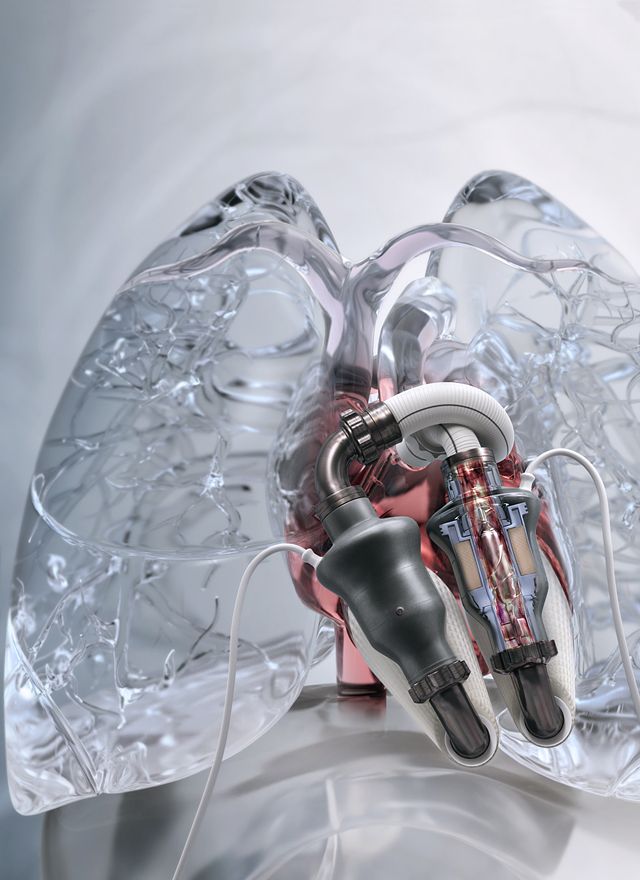 Правая сторона насоса заменяет правый желудочек сердца, возвращая деоксигенированную кровь (синего цвета) в легкие. Иллюстрация: Bivacor
Правая сторона насоса заменяет правый желудочек сердца, возвращая деоксигенированную кровь (синего цвета) в легкие. Иллюстрация: Bivacor
С тех пор было разработано несколько других тотальных искусственных сердец, и некоторые из них прошли испытания на людях. Но эти устройства были большими, тяжелыми и подверженными механическим повреждениям, и только два из них получили одобрение регулирующих органов в Соединенных Штатах. Искусственное сердце SynCardia Systems было одобрено в 2004 году как «мост к трансплантации» и в настоящее время проходит испытания в качестве постоянной замены. Тем не менее, пользователи должны носить с собой 6-килограммовый чемодан с громким воздушным компрессором, прикрепленным к трубкам, проходящим через брюшную полость, где воздух приводит в действие два пневматических насоса устройства. Второе искусственное сердце, AbioCor, получило одобрение в 2006 году, но почти сразу же было снято с производства, когда компания, разработавшая устройство, решила, что оно нецелесообразно с коммерческой точки зрения.
В настоящее время наиболее распространенной механической поддержкой является то, что называется вспомогательным устройством для левого желудочка (LVAD). Эта машина добавляет свою насосную мощность к больному сердцу, фокусируясь на левом желудочке, который перекачивает богатую кислородом кровь по разветвленным артериям, которые достигают головного мозга и спускаются к пальцам ног. LVAD в настоящее время используются как временные вспомогательные средства для пациентов, ожидающих трансплантации, и, в случаях, когда трансплантация невозможна, как постоянные дополнения к грудной полости пациентов. Тем не менее, LVADs может вызвать остановку правого желудочка, что требует интенсивного медикаментозного лечения, а иногда и имплантации вспомогательного устройства для правого желудочка.
В Bivacor нам нужна была настоящая механическая замена всего сердца с длительным сроком службы. В отличие от большинства предыдущих попыток, мы не стремились имитировать естественный пульсирующий насосный механизм сердца с клапанами, которые открываются и закрываются, когда левый желудочек выталкивает кровь в тело, а правый желудочек выталкивает кровь в легкие. В большинстве предыдущих искусственных сердец для достижения этого эффекта использовались поршневые насосы: их две искусственные камеры были раздвоены мембранами, которые изгибались вперед, чтобы выталкивать кровь через механические клапаны.
В большинстве предыдущих искусственных сердец для достижения этого эффекта использовались поршневые насосы: их две искусственные камеры были раздвоены мембранами, которые изгибались вперед, чтобы выталкивать кровь через механические клапаны.
Вместо этого мы выбрали центробежный насос, который направляет непрерывный поток крови в артерии. В таком насосе нет клапанов, поэтому у пациента, использующего сердце Бивакор в самом простом режиме, не будет пульса. Но недавно мы адаптировали наше устройство, чтобы дать ему возможность пульсирующего оттока, как мы объясним ниже. Мы хотим, чтобы клиницисты посмотрели на кардиомониторы пациентов с имплантированным сердцем Bivacor и увидели знакомые ритмические показания, которые они видели со времен медицинской школы.
Сердце Бивакор умещается на ладони — оно весит около 650 граммов, что немного тяжелее сердца взрослого человека. Его оболочка сделана из титана, устойчивого к коррозии материала, который почти никогда не вызывает иммунный ответ. Пациенты будут носить 4-килограммовый внешний блок управления, который содержит две перезаряжаемые батареи (обеспечивающие около 5 часов работы каждой), хотя они также могут подключаться непосредственно к розетке.
Пациенты будут носить 4-килограммовый внешний блок управления, который содержит две перезаряжаемые батареи (обеспечивающие около 5 часов работы каждой), хотя они также могут подключаться непосредственно к розетке.
Фото: Питер Адамс
Тиммс разрабатывает конструкцию искусственного сердца с 2001 года. Первая концептуальная модель проверяла гидравлическую осуществимость конструкции с одним ротором, перекачивающим жидкость в двух направлениях.
В процессе проектирования мы использовали 3D-принтеры для изготовления титановых и пластиковых деталей для наших прототипов, что позволило нам быстро экспериментировать с различной геометрией. Для тестирования мы построили аппаратную симуляцию системы кровообращения человека в нашем инженерном бюро в Лос-Анджелесе; этот макет позволяет нам тщательно и многократно проверять работу устройства в контролируемой среде и снижает потребность в тестировании на животных.
Основным конструктивным нововведением сердца Bivacor является его простая конструкция с одним мотором и одним вращающимся диском, которые одновременно поддерживают перекачку крови как в тело, так и в легкие. Вращающийся диск полностью подвешен в магнитном поле, работая по тому же принципу «маглев», который использовался в высокоскоростных поездах. Диск имеет открытые крыльчатки с обеих сторон, один большой набор, который перекачивает кровь под высоким давлением, необходимым для доставки крови по всему телу, и другой меньший набор, который перекачивает кровь при более низком давлении в легкие. Каждая сторона диска может перекачивать более 12 литров в минуту, что более чем достаточно для пациентов, занимающихся умеренными физическими нагрузками.
Вращающийся диск полностью подвешен в магнитном поле, работая по тому же принципу «маглев», который использовался в высокоскоростных поездах. Диск имеет открытые крыльчатки с обеих сторон, один большой набор, который перекачивает кровь под высоким давлением, необходимым для доставки крови по всему телу, и другой меньший набор, который перекачивает кровь при более низком давлении в легкие. Каждая сторона диска может перекачивать более 12 литров в минуту, что более чем достаточно для пациентов, занимающихся умеренными физическими нагрузками.
Хотя немного крови с двух сторон смешивается вокруг краев подвешенного диска, это не проблема из-за направления потока. Некоторое количество насыщенной кислородом крови просачивается со стороны высокого давления на сторону низкого давления, а это означает, что некоторое количество уже насыщенной кислородом крови возвращается в легкие. И эта утечка на самом деле является конструктивной особенностью, а не ошибкой. Смыв крови вокруг диска очищает кожух и гарантирует отсутствие областей, в которых застоявшаяся кровь может образовать опасные сгустки.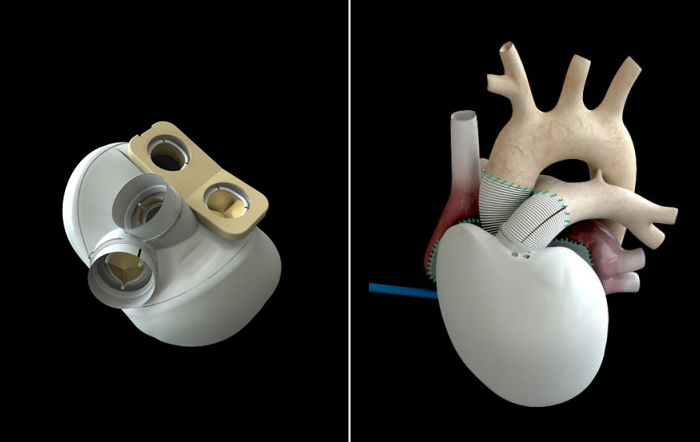
Статор двигателя обеспечивает крутящий момент за счет соединения с набором постоянных магнитов в диске ротора. При нормальной работе он вращает ротор со скоростью от 1600 до 2700 оборотов в минуту. Силам притяжения между двигателем и ротором противодействует магнитный подшипник на противоположной стороне ротора, который активно контролирует положение ротора внутри корпуса. Эта активная система управления необходима, поскольку ротор естественным образом перемещается, когда пациент ходит, поднимается по лестнице, прыгает и вообще занимается повседневными делами. Важно правильно подвешивать ротор и не допускать его ударов о стенки корпуса, которые могут повредить компоненты и разбить клетки крови.
Эта система управления положением работает следующим образом: крошечные бесконтактные датчики посылают магнитные поля, которые взаимодействуют с ротором, определяя его точное местоположение много раз в секунду. Если ротор движется в том или ином направлении, система управления подает электрическую энергию на электромагнитные катушки внутри нескольких приводов, заставляя их компенсировать это движение.
Конструкция приводов с магнитными подшипниками имела решающее значение, особенно потому, что они должны были быть небольшими, легкими и энергоэффективными, но при этом достаточно прочными, чтобы компенсировать все колебания и толчки, создаваемые человеком в движении. Мы использовали компьютерное моделирование магнитного поля для оптимизации конструкции, экспериментируя с различными материалами и геометрией, чтобы найти конфигурацию, обеспечивающую достаточную силу в небольшом пространстве. Сохранение нашего устройства небольшим и легким означает, что оно поместится внутри людей с небольшим телом, включая женщин и детей.
Чтобы повысить эффективность нашего искусственного сердца, мы также интегрировали контроллер «нулевой мощности» в систему подвески. Этот контроллер отслеживает дополнительную электромагнитную мощность, используемую подшипником, поскольку он реагирует на внешние силы, действующие на ротор, а затем перемещает ротор в положение, в котором постоянные магниты системы магнитных подшипников могут обеспечить уравновешивающую силу.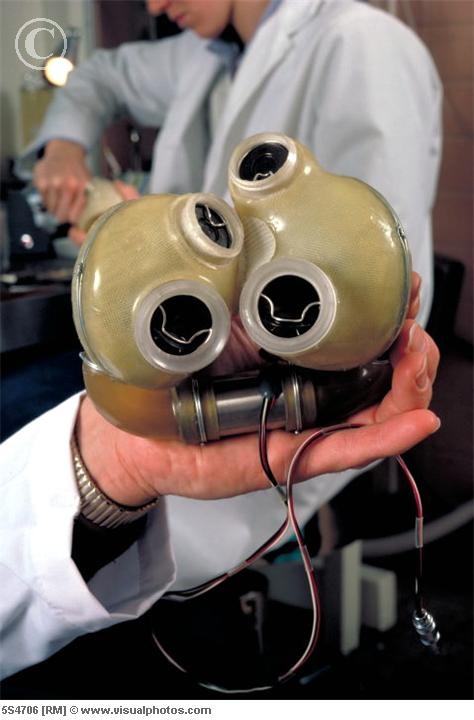 Эта система не производит мгновенных регулировок — это работа, выполняемая основным контроллером устойчивости, — но она снижает количество энергии, используемой магнитным подшипником при воздействии внешних сил.
Эта система не производит мгновенных регулировок — это работа, выполняемая основным контроллером устойчивости, — но она снижает количество энергии, используемой магнитным подшипником при воздействии внешних сил.
Фото: Питер Адамс
Чтобы быстро протестировать свои прототипы искусственного сердца и уменьшить потребность в испытаниях на животных, команда Бивакор создала аппарат, который воспроизводит систему кровообращения человека, имитируя поток крови через тело и легкие. .
Уникальной особенностью сердца Bivacor является то, что ротор может перемещаться вдоль своей оси вращения для изменения количества крови, перемещаемой левой и правой сторонами насоса. Когда ротор движется к левой стороне корпуса, он приближает лопасти рабочего колеса к стенке корпуса. В этом узком пространстве большая часть крови закручивается лопастями, а небольшое количество крови проходит через кончики лопастей, что увеличивает эффективность левого насоса и, следовательно, его подачу крови в тело. Эта функция полезна для быстрой корректировки, необходимой при переходах, например, когда пациент встает.
Эта функция полезна для быстрой корректировки, необходимой при переходах, например, когда пациент встает.
Наше устройство элегантно взаимодействует с человеческим телом, автоматически адаптируясь к уровню активности человека. Когда пациент тренируется, механическое сердце будет перекачивать больше крови к мышцам, как это делает биологическое сердце. Эта адаптация достигается за счет обратной связи тела: когда человек начинает бегать на беговой дорожке, усердно работающие мышцы ног и других частей тела быстрее расходуют насыщенную кислородом кровь и выталкивают кровь, лишенную кислорода, обратно в кровеносную систему. Этот увеличенный приток крови к сердцу Bivacor заставляет обе стороны насоса перемещать больше крови, не требуя увеличения скорости вращения ротора. Эта кажущаяся базовой функциональность на самом деле является результатом тщательной оптимизации гидравлической конструкции. Мы полагались на наш 3D-принтер, чтобы изготовить множество экспериментальных прототипов с корпусами и лопастями крыльчатки немного отличающейся формы.
Биосовместимость — одна из самых больших проблем в нашей области, потому что взаимодействие между механическим устройством и биологическими системами очень сложное. Например, хрупкие клетки крови и другие компоненты крови могут быть повреждены при грубом перемещении через устройство. В качестве ключевой конструктивной особенности сердца Bivacor мы обеспечили достаточный зазор между левитирующим ротором, корпусом и трубопроводами для крови. Все пути потока имеют зазоры не менее 240 микрометров при нормальной работе, что более чем в 20 раз превышает размер эритроцита. Такая конструкция уменьшает силы сдвига, которым подвергается кровь, а также гарантирует отсутствие застоя крови внутри корпуса.
Блокнот Начало: Тиммс впервые набросал основную идею искусственного сердца Bivacor в блокноте, когда он получал докторскую степень. в области биомедицинской инженерии — вскоре после того, как у его отца диагностировали сердечную недостаточность.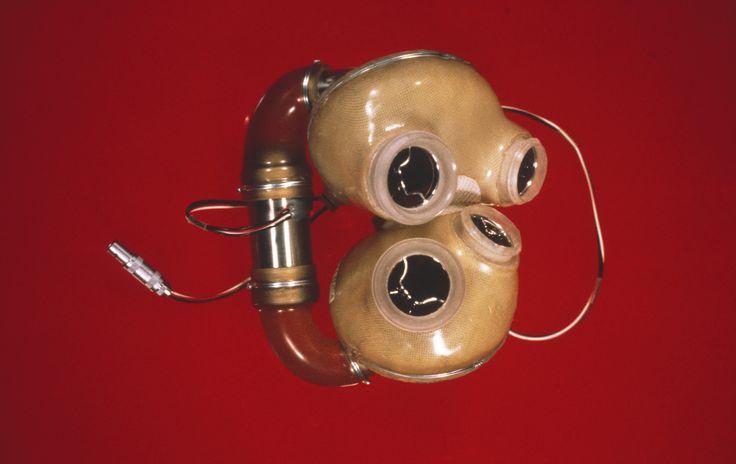 Фото: Питер Адамс
Фото: Питер Адамс
Помпа может работать с постоянной скоростью, создавая непрерывный поток крови при постоянном давлении, и в наших ранних экспериментах мы сосредоточились на тестировании этого «безпульсового» режима. Но его скорость легко изменить, и наши более поздние эксперименты показали, что контролируемое изменение скорости может привести к широкому диапазону характеристик потока и давления. Работа помпы сначала на высокой скорости (откачка большего количества крови), а затем на низкой скорости (откачка меньшего количества крови) создает нечто, напоминающее биологический пульс сердца; быстрое чередование этих двух скоростей создает нечто похожее на нормальное сердцебиение.
Сейчас мы работаем в основном в этом пульсирующем режиме. В кардиологии ведутся открытые дебаты о том, необходим ли пульс для хорошего здоровья. Некоторые пациенты с имплантированными LVAD, которые производят непрерывный (и, следовательно, без пульса) поток, испытывают медицинские проблемы, такие как желудочно-кишечное кровотечение, однако неясно, являются ли причиной их устройства. Мы надеемся, что наше устройство, которое можно использовать как в режиме непрерывного потока, так и в пульсирующем режиме, внесет свой вклад в научное исследование этой важной темы.
Мы надеемся, что наше устройство, которое можно использовать как в режиме непрерывного потока, так и в пульсирующем режиме, внесет свой вклад в научное исследование этой важной темы.
Основатель Bivacor Тиммс начал работу над оригинальной концепцией своего искусственного сердца 18 лет назад, и за эти годы она претерпела множество итераций. Тиммс начал проект в своей родной Австралии, и с тех пор команда разработчиков получила выгоду от сети увлеченных сотрудников в Германии, Японии, Тайване и США. На разных этапах проекта команда перемещалась в международные лаборатории, чтобы использовать опыт наших сотрудников. В настоящее время наша команда базируется в США (в Лос-Анджелесе и Хьюстоне) и Австралии (в Мельбурне и Брисбене), и мы сосредоточены на превращении нашего прототипа в коммерческий продукт.
Мы очень довольны дизайном нашего устройства. Теперь мы стандартизируем производственный процесс: наши методы 3D-печати хорошо подходили для этапа разработки, когда мы хотели тестировать прототипы и быстро выполнять итерации, но теперь мы переходим на прецизионную механическую обработку, которая придаст деталям устройства более гладкая полировка и более точные и последовательные размеры. Эти процедурные изменения сделают возможным крупномасштабное производство. Мы также документируем каждый этап процесса производства и имплантации, чтобы подготовиться к нашим первым клиническим испытаниям.
Эти процедурные изменения сделают возможным крупномасштабное производство. Мы также документируем каждый этап процесса производства и имплантации, чтобы подготовиться к нашим первым клиническим испытаниям.
К концу 2019 года у нас будет система клинического уровня. Затем мы отправим запрос в Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США на предварительное технико-экономическое обоснование на людях, которое, как мы надеемся, начнется в 2020 году.
Мы уже предвидим эти первые испытания на людях. Тяжелобольные пациенты будут поступать в операционную с отказавшим биологическим сердцем, слабо бьющимся в груди, и выходить из операционной с жужжащим безотказно функционирующим искусственным сердцем Bivacor. Поскольку устройства посылают мощные потоки богатой кислородом крови в их тела, мы надеемся, что к пациентам быстро вернутся силы. Если эти пациенты смогут подняться со своих больничных коек, обнять членов своей семьи и продолжить свою жизнь в течение многих лет, мы сделаем большой шаг вперед в долгом поиске полностью искусственного сердца.