Содержание
Овечья доля. Зачем клонируют животных и правда ли, что клоны рождаются старыми
22 февраля 1997 года мир узнал о существовании овечки Долли — первого млекопитающего, клонированного из клетки взрослого организма. Она была не первым и не последним клонированным животным, но осталась самым знаменитым и обсуждаемым, в частности благодаря тому, что ее ранняя смерть породила опасения о преждевременном старении клонированных животных.
Клоны рождаются старыми?
Овечка Долли появилась на свет 5 июля 1996 года. Ее назвали в честь певицы Долли Партон, чьи пышные формы часто становились предметом обсуждения в прессе. По словам Иэна Уилмута, одного из создателей Долли, эта идея пришла в голову двоим работникам, которые заботились о суррогатной матери знаменитой овцы при родах и задумались о том, что клетки для клонирования были взяты из молочной железы.
Долли прожила шесть с половиной лет, родив шестерых ягнят. Ее усыпили 14 февраля 2003 года, так как у овцы развилась опухоль легких. Ее болезни и преждевременная для овцы смерть зародили опасение, что животные, клонированные из клетки взрослого организма, «наследуют» его возраст, рождаются уже старыми и, соответственно, обречены на раннюю смерть.
Ее болезни и преждевременная для овцы смерть зародили опасение, что животные, клонированные из клетки взрослого организма, «наследуют» его возраст, рождаются уже старыми и, соответственно, обречены на раннюю смерть.
Долли со своим потомством. Фото: The Roslin Institute, The University of Edinburgh
Это предположение подтверждало и молекулярное исследование тканей овцы, проведенное, когда ей был год от роду. Ученые обнаружили, что уже в этом возрасте ее теломеры — участки ДНК, которые находятся на концах хромосом и укорачиваются на протяжении жизни при делении клеток — на 20% короче, чем должны быть у овцы ее возраста.
Однако у Долли были четыре сестры — овцы, клонированные из клеток той же овцы-донора, что и Долли. Они появились в 2005—2007 годах и пребывают в добром здравии, несмотря на солидный возраст, опровергая идею об обязательном раннем старении клонов.
Овцы, клонированные из тех же клеток, что и овечка Долли. Фото: The University of Nottingham
Что же касается Долли, то ученые не знают, почему ей так не повезло со здоровьем. Одно из предположений — методика клонирования в ее время была менее совершенной: Долли была единственной удачной из 277 попыток клонирования. Сейчас успех в подобных экспериментах может достигать 10%.
Одно из предположений — методика клонирования в ее время была менее совершенной: Долли была единственной удачной из 277 попыток клонирования. Сейчас успех в подобных экспериментах может достигать 10%.
Технология клонирования
История клонирования началась задолго до овечки Долли. В 1885 году немецкий биолог Ханс Дриш обнаружил, что, если разделить эмбрион морского ежа на стадии, когда он состоит из двух клеток, из каждой вырастет по целому ежу.
Долли не стала и первым животным, клонированным из взрослой клетки. Джон Гердон проделал это в 1962 году с лягушкой. Его эксперимент, как и клонирование Долли, основывался на технологии пересадки ядер соматических клеток: ядро, содержащее ДНК, выделяют из клетки взрослого животного и помещают в яйцеклетку другого животного (того же вида) с предварительно удаленным ядром. В новой обстановке ядро клеток «репрограммируется» — ДНК теряет эпигенетические модификации, которые она приобрела в процессе превращения эмбриональной клетки в клетку определенной ткани, и снова может быть использована для выращивания нового организма. Благо, каждая клетка в организме (кроме половых) содержит полный набор его генов вне зависимости от того, частью какой ткани она является. Затем собранную таким образом яйцеклетку подсаживают суррогатной матери.
Благо, каждая клетка в организме (кроме половых) содержит полный набор его генов вне зависимости от того, частью какой ткани она является. Затем собранную таким образом яйцеклетку подсаживают суррогатной матери.
Главное, что показал эксперимент Гердона, а затем и клонирование Долли, — клетка ткани взрослого организма может при определенных условиях вернуться в эмбриональное состояние. За это Гердон получил Нобелевскую премию вместе с японцем Синъей Яманакой, который придумал более простой способ перепрограммировать взрослые клетки в стволовые. Такие клетки могут использоваться для выращивания различных тканей или даже органов.
Зачем клонируют животных
После Долли из взрослых клеток клонировали мышей, коров, коз, свиней, лошадей, собак (афганских борзых), хорьков, мулов, буйволов и верблюдов — клонирование стало отработанной технологией.
Первый клонированный верблюд, 8 июня 2009 года. Фото: Nisar A. Wani et al., Biol Reprod. 2010;82(2):373−379. doi:10.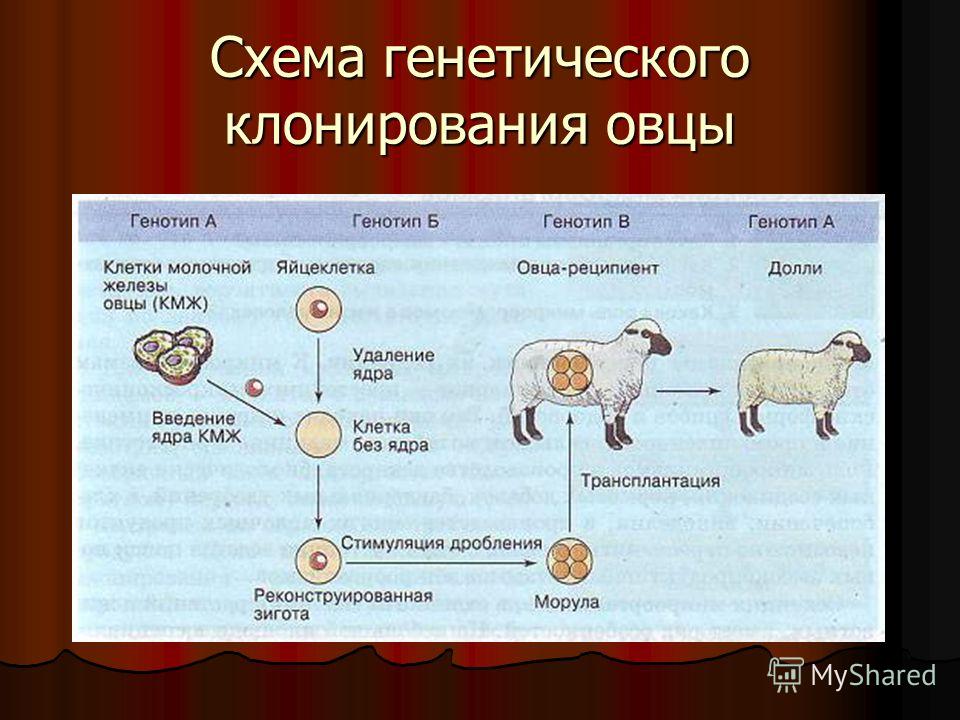 1095/biolreprod.109.81 083
1095/biolreprod.109.81 083
Разводить животных таким образом, конечно, не имеет смысла, разве что клонировать особо ценных быков или жеребцов-производителей. Однако комбинирование техники клонирования с методами генетического редактирования позволяет получать скот с новыми признаками. Например, недавно китайские ученые вывели коров, устойчивых к туберкулезу. Другие примеры — безрогий скот и коровы, которые не болеют бешенством, или свиньи, устойчивые к вирусу свиного репродуктивного и респираторного синдрома.
Бык по кличке Окончательный Ответ (Final Answer) был клонирован как особо ценный производитель
Екатерина Боровикова
Теги
Генетика
Почему о клонировании овечки Долли так быстро забыли
Впервые клонировать животное попробовали еще более чем 140 лет назад, но многие убеждены, что этот метод получил развитие с появлением на свет овцы Долли.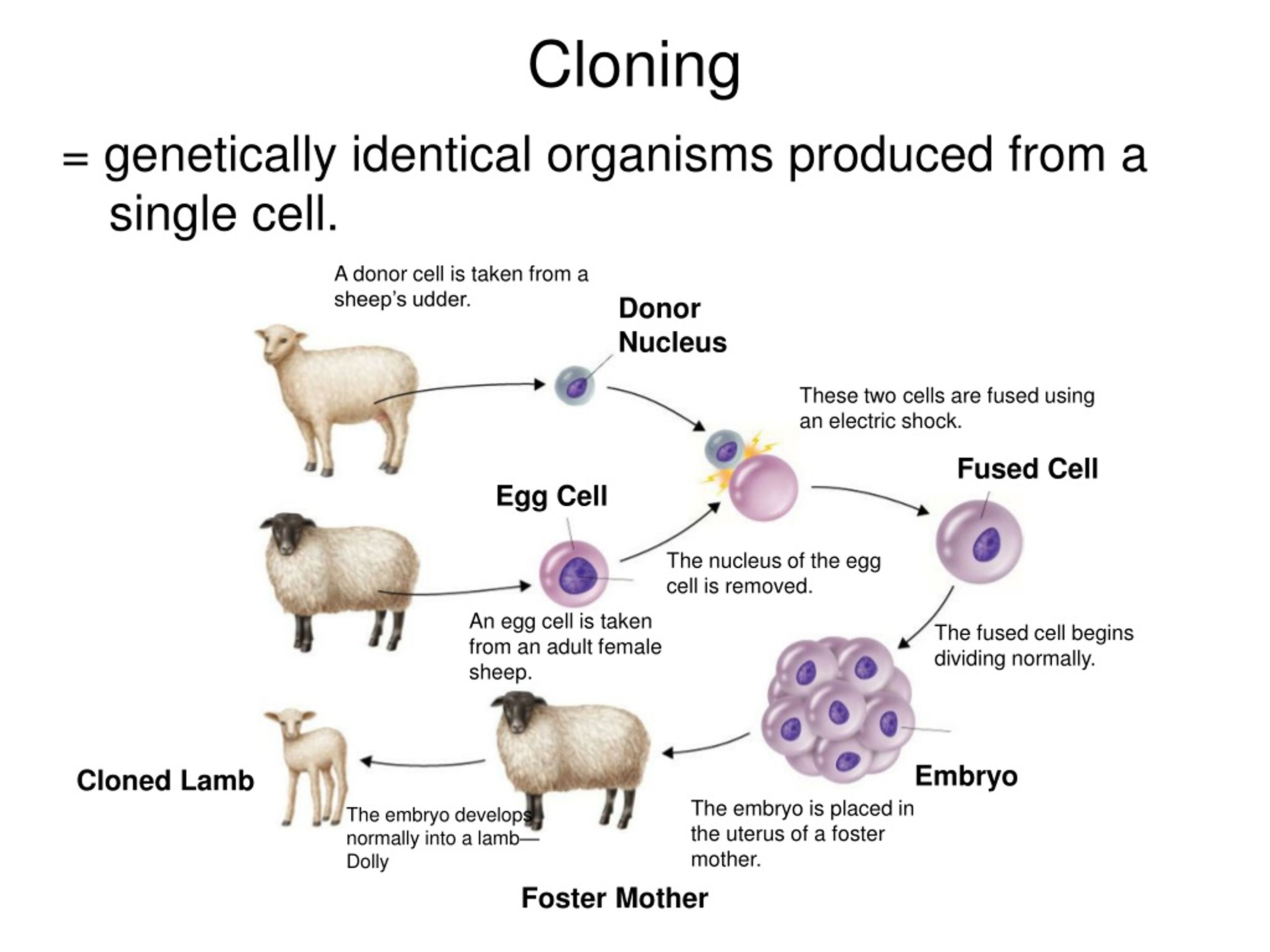 Однако это был не первый созданный клон млекопитающего животного — почему собственно об этом писалось в большинстве газет и журналов?
Однако это был не первый созданный клон млекопитающего животного — почему собственно об этом писалось в большинстве газет и журналов?
В чем уникальность овечки Долли
До 90-ых годов в процессе клонирования использовались 2 ооцита. С овцой Долли использовался другой метод: ядро, где сберегались персональные данные о ее “маме”, получили из вымени уже взрослого животного. Клеточный материал был заморожен. Путь к появлению Долли был длителен и сложен: в изысканиях использовали более 250 ооцитов, в которые переместили ядра из клеток вымени. Из них сформировалось 29 зародышей, а на свет появилась одна Долли. Оставшиеся двойники приостановились в развитии. Это был первый увенчавшийся успехом опыт по трансплантации ядра взрослой особи в яйцеклетку. С того времени ученые клонировали и других животных.
В США открылось несколько медлабораторий, которые специализируются на клонировании в коммерческих целях. Они предлагают возродить любимое животное после его смерти.
Каковы механизмы, управляющие формированием зародыша? Почему не все зародыши развиваются?
По всей видимости ответы на эти вопросы нашли в 2018 году ученые из Китая.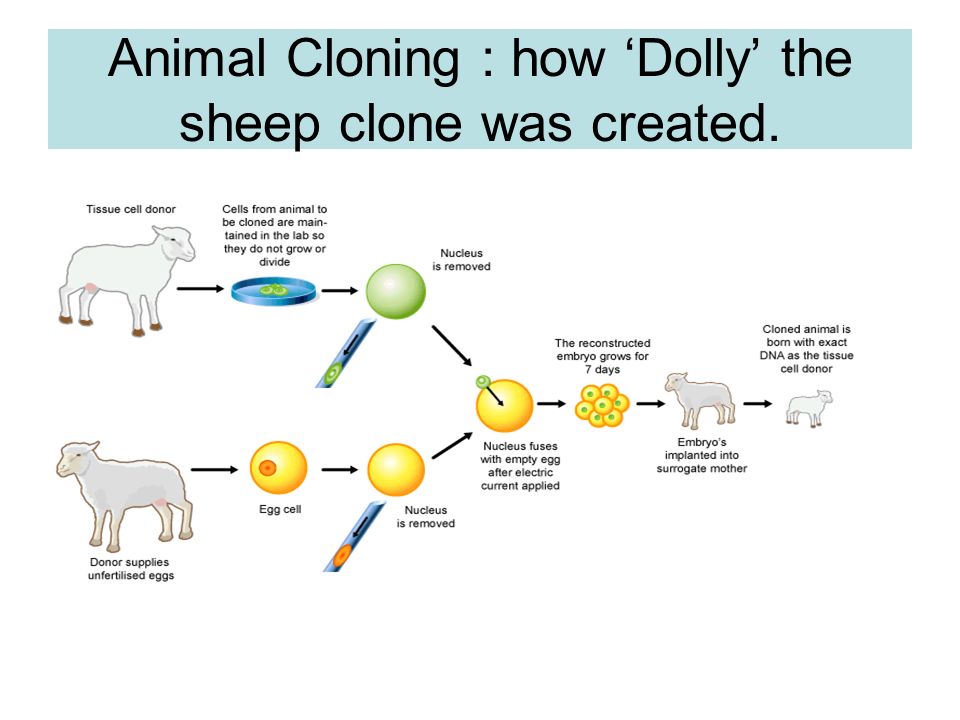 Несколько обезьянок родилось в ходе клонирования по “принципу Долли”. Раньше такие опыты срывались. Что же предприняли профессора из Китая? Они воспользовались закономерностями эпигенетического наследования. Иными словами вся наша жизнь обусловливается не только генетическими данными, но и зависит от белков, порядка выкладки ДНК, времени функционирования генов. Таким образом, даже точно скопировав нужные гены, нельзя быть уверенным в том, что они начнут работать. Необходимо учесть и другие факторы.
Несколько обезьянок родилось в ходе клонирования по “принципу Долли”. Раньше такие опыты срывались. Что же предприняли профессора из Китая? Они воспользовались закономерностями эпигенетического наследования. Иными словами вся наша жизнь обусловливается не только генетическими данными, но и зависит от белков, порядка выкладки ДНК, времени функционирования генов. Таким образом, даже точно скопировав нужные гены, нельзя быть уверенным в том, что они начнут работать. Необходимо учесть и другие факторы.
Применение клонирования для терапии пациентов
Создание клонов с целью лечения пациентов используется только в некоторых странах, к примеру, в Бельгии и Англии. В декабре 2006 года австралийским правительством впервые был снят запрет на клонирование людей — конечно это было предпринято только в целях развития науки. В РФ все исследования по клонированию остановлены: некоторые ученые утверждают, что нарушение структуры бластоцисты (а без этого нельзя получить нужный клеточный материал) подобно уничтожению эмбриона человека. Появляется дилемма, по которой ведутся вечные дискуссии: можно ли создать организм, чтобы в дальнейшем его разрушить, даже если таким образом можно спасти других людей? Еще более чем в 65 странах мира действует запрет на клонирование — не только из-за недостатков в технологиях, а и из-за морально-этических проблем.
Появляется дилемма, по которой ведутся вечные дискуссии: можно ли создать организм, чтобы в дальнейшем его разрушить, даже если таким образом можно спасти других людей? Еще более чем в 65 странах мира действует запрет на клонирование — не только из-за недостатков в технологиях, а и из-за морально-этических проблем.
Каков правовой статус вновь созданного организма — главная тема для дискуссий
В ходе терапевтического клонирования исследователи вправе растить человеческий эмбрион до 2 недель. Этого хватит для образования бластоцисты. К четырнадцатому дню возникает первичная полоска с которой формируется ЦНС. И вот тут начинаются споры. С позиции биологии зародыш — это не обособленный организм, он полностью зависит от благоприятных условий внешней среды и не может без них выжить. С другой стороны, из зародыша в дальнейшем вырастает человек. Религия утверждает, что с момента зарождения у эмбриона уже есть ум, поэтому испытания над ним — это преступление. Разрушение эмбрионов для извлечения стволовых клеток, которые потом можно использовать для создания органов и тканей, не разрешается и сравнивается со смертоубийством.
Кроме этого, представители различных религиозных конфессий критично настроены по отношению к ВРТ. Самый распространенный среди них — экстракорпоральное оплодотворение. Его применение категорично отрицает Российская Православная Церковь. Считается, что в данном случае уничтожается целостность человеческой личности. “Разрушая” в процессе манипуляции эмбрионы, мы наносим вред новой жизни. В прошлом году Государственной думой был принят закон, согласно которому категорически запрещается клонировать людей. Таким образом, создание человеческих двойников запрещено законом, да и с технологической точки зрения это сейчас невозможно. Но паника, связанная с вероятным возникновением армии клонов, с каждым годом все увеличивается. Вызвана она как элементарным страхом, что клоны будут более сильными и выносливыми чем обыкновенные люди, так и боязнью наказания свыше.
Бесспорен тот факт, что до возникновения двойника нужно будет решить много проблем эстетического характера, выработать позитивное расположение к людям, которые родились подобным образом и позаботиться об обеспечении их правами. Но все это нас ждет в далеком будущем. Пока ученые могут лишь выращивать нужные органы взамен многочасовых поисков доноров и заниматься разработкой методов терапии болезней с применением клонированного клеточного материала. Видимо, этот факт осознали даже журналисты и публицисты, которые не пугают теперь общественность новыми фактами о клонировании. Вместе с тем методика однозначно будет совершенствоваться. И если сегодня всем кажется редкостным феноменом рождение животных, то через несколько десятков лет, может быть, и возникновение двойников станет обыденностью.
Но все это нас ждет в далеком будущем. Пока ученые могут лишь выращивать нужные органы взамен многочасовых поисков доноров и заниматься разработкой методов терапии болезней с применением клонированного клеточного материала. Видимо, этот факт осознали даже журналисты и публицисты, которые не пугают теперь общественность новыми фактами о клонировании. Вместе с тем методика однозначно будет совершенствоваться. И если сегодня всем кажется редкостным феноменом рождение животных, то через несколько десятков лет, может быть, и возникновение двойников станет обыденностью.
Овцы, клонированные путем переноса ядра из культивируемой клеточной линии
. 1996 7 марта; 380 (6569): 64-6.
дои: 10.1038/380064a0.
К Х Кэмпбелл
1
, J McWhir, W A Ritchie, I Wilmut
принадлежность
- 1 Институт Рослина (Эдинбург), Великобритания.

PMID:
8598906
DOI:
10.1038/380064а0
KH Campbell et al.
Природа.
.
. 1996 7 марта; 380 (6569): 64-6.
дои: 10.1038/380064a0.
Авторы
К Х Кэмпбелл
1
, Дж. Маквир, В. А. Ричи, И. Уилмут
принадлежность
- 1 Институт Рослина (Эдинбург), Великобритания.
PMID:
8598906
DOI:
10.
 1038/380064а0
1038/380064а0
Абстрактный
Перенос ядер использовался у млекопитающих как ценный инструмент в эмбриологических исследованиях и как метод размножения «элитных» эмбрионов. Сообщалось о потомстве только тогда, когда ранние эмбрионы или клетки, полученные из эмбрионов во время первичной культуры, использовались в качестве доноров ядра. Здесь мы приводим первое, насколько нам известно, сообщение о живом потомстве млекопитающих после переноса ядра из установленной клеточной линии. Ягнята рождались после того, как клетки, полученные из эмбрионов овцы, которые культивировались в течение 6-13 пассажей, вызывали к остановке с помощью сывороточного голодания перед переносом их ядер в энуклеированные ооциты. Индукция покоя в донорских клетках может модифицировать структуру донорского хроматина, чтобы помочь ядерному перепрограммированию и обеспечить развитие. Этот подход предоставит те же мощные возможности для анализа и модификации функции генов у видов домашнего скота, которые доступны у мышей за счет использования эмбриональных стволовых клеток.
Похожие статьи
Ядерный перенос синхронизированных соматических клеток африканской дикой кошки в энуклеированные ооциты домашней кошки.
Гомес М.С., Дженкинс Дж.А., Хиральдо А., Харрис Р.Ф., Кинг А., Дрессер Б.Л., Папа К.Э.
Гомес М.С. и соавт.
Биол Репрод. 2003 г., сен; 69 (3): 1032-41. doi: 10.1095/biolreprod.102.014449. Epub 2003 28 мая.
Биол Репрод. 2003.PMID: 12773426
Влияние донорских ооцитов и условий культивирования на развитие клонированных эмбрионов мышей.
Гао С., МакГарри М., Приддл Х., Ферриер Т., Гаспаррини Б., Флетчер Дж., Харкнесс Л., Де Соуза П., МакВир Дж., Уилмут И.
Гао С. и др.
Мол Репрод Дев. 2003 г., октябрь; 66 (2): 126–33. doi: 10.1002/mrd. 10300.
10300.
Мол Репрод Дев. 2003.PMID: 12950099
Влияние различных донорских клеток и пассажей на развитие реконструированных эмбрионов.
Лей Л., Лю Чж., Ван Х., Коу Чж., Ву Ю. К., Сюй Ю., Ченг Ю., Чжу З.И., Ся Г.Л., Чен Д.Ю.
Лей Л. и др.
И Чуан Сюэ Бао. 2003 март; 30 (3): 215-20.
И Чуань Сюэ Бао. 2003.PMID: 12812086
Перенос ядер у кошек и его применение.
Гомес MC, Папа CE, Dresser BL.
Гомес М.С. и соавт.
Териогенология. 2006 г., 1 июля; 66 (1): 72–81. doi: 10.1016/j.theriogenology.2006.03.017. Epub 2006 18 апр.
Териогенология. 2006.PMID: 16620927
Рассмотрение.
Перенос ядер из соматических клеток: применение у сельскохозяйственных животных.

Eyestone WH, Кэмпбелл KH.
Eyestone WH и др.
J Reprod Fertil Suppl. 1999;54:489-97.
J Reprod Fertil Suppl. 1999.PMID: 10692878
Рассмотрение.
Посмотреть все похожие статьи
Цитируется
Комплементация бластоцист и межвидовые химеры у свиней с отредактированными генами.
Choe YH, Sorensen J, Garry DJ, Garry MG.
Choe YH и соавт.
Front Cell Dev Biol. 2022 8 декабря; 10:1065536. doi: 10.3389/fcell.2022.1065536. Электронная коллекция 2022.
Front Cell Dev Biol. 2022.PMID: 36568986
Бесплатная статья ЧВК.Рассмотрение.
Разрешение геропластичности на баланс омолаживающих и гериатринных веществ.
Табибзаде С.
Табибзаде С.
Старение Дис. 2022 1 декабря; 13 (6): 1664-1714. doi: 10.14336/AD.2022.0414. Электронная коллекция 2022 1 декабря.
Старение Дис. 2022.PMID: 36465174
Бесплатная статья ЧВК.Создание, характеристика и проверка новых свиных эмбриональных фибробластов как потенциального источника генетической модификации.
Park CH, Jeoung YH, Zhang L, Yeddula SGR, Park KE, Waters J, телугу BP.
Парк Ч. и др.
Front Cell Dev Biol. 2022 10 нояб.; 10:1059710. doi: 10.3389/fcell.2022.1059710. Электронная коллекция 2022.
Front Cell Dev Biol. 2022.PMID: 36438568
Бесплатная статья ЧВК.Эмбриональное клонирование с двойным цитопластом улучшает in vitro , но не in vivo развитие митотических плюрипотентных клеток крупного рогатого скота.

Appleby SJ, Misica-Turner P, Oback FC, Dhali A, McLean ZL, Oback B.
Appleby SJ и др.
Фронт Жене. 2022 сен 28;13:933534. doi: 10.3389/fgene.2022.933534. Электронная коллекция 2022.
Фронт Жене. 2022.PMID: 36246653
Бесплатная статья ЧВК.Эпигенетическая динамика модификации h5K20me3 во время созревания ооцитов и раннего репрограммирования эмбрионов коз с трансплантированным ядром соматических клеток.
Liu Z, Li M, Sun Y, Wang W, Wang Z, Presicce GA, An L, Du F.
Лю Зи и др.
Am J Transl Res. 2022 25 августа; 14 (8): 5941-5951. Электронная коллекция 2022.
Am J Transl Res. 2022.PMID: 36105059
Бесплатная статья ЧВК.
Просмотреть все статьи «Цитируется по»
Типы публикаций
термины MeSH
Фальшивые новости о клонированной овце Долли
Наука
Исследование костей известного животного показывает, что общепринятое мнение о том, как стареют клоны, вероятно, неверно.
Овечка Долли встречается с прессой в феврале 1997 года. (Джефф Дж. Митчелл / Reuters )
Поэтому, когда ученые заподозрили, что у нее короткие теломеры — участки ДНК, которые обычно укорачиваются с возрастом, — люди задались вопросом, не связано ли это с тем, что она была клонирована из взрослой клетки. Когда в возрасте пяти лет она начала хромать, заголовки писали, что ее артрит «подрывает веру в клонирование». А когда она умерла в возрасте шести лет — в результате распространенного легочного вируса, убившего и других овец в ее сарае, — ее короткая жизнь снова превратилась в притчу о клонировании. Определенный сюжет сложился.
Затем, в прошлом году, Кевин Синклер, биолог развития из Ноттингемского университета, опубликовал статью о нескольких клонах, включая четырех «сестер» Долли, которые были созданы из той же клеточной линии, что и Долли, и дожили до восьмилетнего возраста ( около 70 в человеческих годах). Для своего возраста они были вполне здоровы. Поэтому, конечно, он продолжал получать вопросы, например, если эти животные такие здоровые, то почему Долли была такой нездоровой? Всем была дорога Долли.
Для своего возраста они были вполне здоровы. Поэтому, конечно, он продолжал получать вопросы, например, если эти животные такие здоровые, то почему Долли была такой нездоровой? Всем была дорога Долли.
Синклер заметил бы, что Долли не так уж нездорова. Но вопросы вдохновили его команду на поиск медицинских карт Долли с начала 2000-х годов. Однако записи были утеряны. «Все сдвинулось. Люди уехали, и люди занимаются другими делами», — говорит Синклер. Но после ее смерти в 2003 году кости Долли были переданы Национальному музею Шотландии. Команда Синклера получила разрешение на их изучение — вместе с костями Меган и Мораг, двух овец, клонированных из незрелых клеток, которые были прототипами Долли, и дочери Долли, зачатой естественным путем, Бонни.
Группа ветеринаров сделала рентгеновские снимки костей на наличие признаков артрита. Меган и Бонни, умершие в преклонном возрасте 13 и 9 лет соответственно, действительно имели признаки артрита, что было нормальным для их возраста.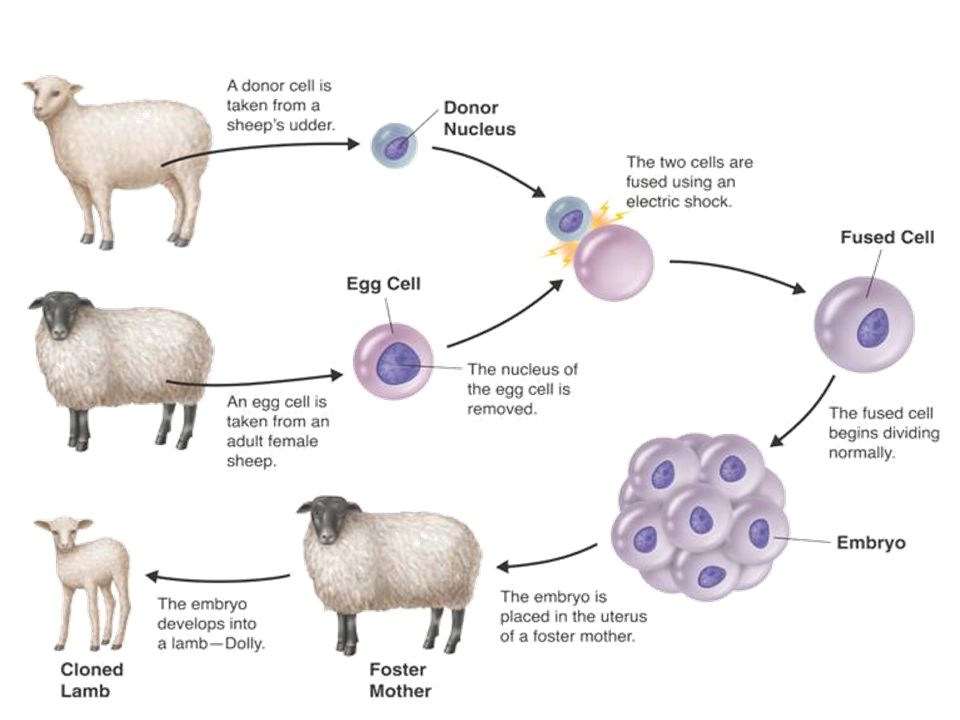 Меган, которая умерла в возрасте четырех лет от более ранней вспышки того же легочного вируса, который убил Долли, не умерла. Даже на колене Долли не было признаков артрита.
Меган, которая умерла в возрасте четырех лет от более ранней вспышки того же легочного вируса, который убил Долли, не умерла. Даже на колене Долли не было признаков артрита.
Установка рентгеновского снимка костей клонированной овцы (Ноттингемский университет)
Артрит также поражает мягкие ткани сустава, поэтому Синклер отмечает, что кости сами по себе не указывают на окончательный диагноз или его отсутствие. (И Долли действительно хромала.) Но общий набор данных, полученных от Меган, Мораг и Бонни, а также от клонов пожилых сестер Долли, позволяет предположить, что артрит встречается у клонов не чаще, чем у обычных овец. Опасения по поводу преждевременного старения клонов могут быть сильно преувеличены. «Мы чувствовали, что запись должна быть установлена прямо», — говорит Синклер.
Даже опасения по поводу слишком коротких теломер Долли не оправдались. Теломеры представляют собой повторяющиеся последовательности ДНК на концах хромосом, и они укорачиваются каждый раз, когда клетка делится. В 1999 году ученые опубликовали данные, свидетельствующие о том, что теломеры Долли были слишком короткими для ее возраста. С тех пор ученые клонировали целый зверинец животных: мышей, лошадей, крупный рогатый скот, свиней, собак и так далее. Исследования длины их теломер дали все возможные результаты: клоны имеют более короткие теломеры, клоны имеют более длинные теломеры и клоны имеют нормальные теломеры — в зависимости от вида или метода клонирования.
В 1999 году ученые опубликовали данные, свидетельствующие о том, что теломеры Долли были слишком короткими для ее возраста. С тех пор ученые клонировали целый зверинец животных: мышей, лошадей, крупный рогатый скот, свиней, собак и так далее. Исследования длины их теломер дали все возможные результаты: клоны имеют более короткие теломеры, клоны имеют более длинные теломеры и клоны имеют нормальные теломеры — в зависимости от вида или метода клонирования.
У клонов действительно есть уникальные проблемы со здоровьем, но не те, которые были в заголовках новостей о Долли. У клонов меньше шансов дожить до срока беременности, и когда они рождаются, они, скорее всего, будут немного неприспособленными. «Вы должны нянчиться с ними — давать им кислород, давать им глюкозу, пока они не нормализуются», — говорит Джордж Зайдель, изучающий технологии размножения животных в Университете штата Колорадо. Клоны, которые доживают до зрелого возраста, обычно вполне нормальны. Но это делает клонирование домашнего скота чрезвычайно дорогим, порядка 20 000 долларов за штуку. Несмотря на много шума вокруг клонированного мяса, клонирование не является экономичным способом выращивания крупного рогатого скота на мясо или молоко.
Несмотря на много шума вокруг клонированного мяса, клонирование не является экономичным способом выращивания крупного рогатого скота на мясо или молоко.
«Вы, наверное, ели сыр от потомства клона».
Однако у него есть нишевые применения в животноводстве, например, воссоздание быков за миллион долларов с чрезвычайно ценными генами. Зайдель, у которого также есть ранчо крупного рогатого скота, покупает сперму у Final Answer 2, клона знаменитого производителя Final Answer, умершего в 2014 году. Сперма правильного быка также невероятно ценна для молочной промышленности. «Вероятно, вы ели немного сыра от потомства клона», — говорит Зайдель. Но настоящие клоны не продаются в пищу в Соединенных Штатах.
Несмотря на все внимание, которое когда-то привлекла Долли, клонирование само по себе радикально не изменило мир. Исследование, которое создало ее, действительно многому научило ученых о том, как можно манипулировать эмбрионами, что вдохновило на новые направления исследований стволовых клеток.


 1038/380064а0
1038/380064а0 10300.
10300.

