Содержание
Ученые создали полусинтетическую кишечную палочку – DW – 26.06.2014
Фото: picture-alliance/dpa
Наука
Владимир Фрадкин
26 июня 2014 г.
Наследственная информация всех живых организмов закодирована в молекулах ДНК с помощью четырех букв генетического алфавита. Теперь ученые добавили к ним еще две буквы.
https://www.dw.com/ru/%D0%B3%D0%B5%D0%BD%D0%B5%D1%82%D0%B8%D1%87%D0%B5%D1%81%D0%BA%D0%B8%D0%B9-%D0%B0%D0%BB%D1%84%D0%B0%D0%B2%D0%B8%D1%82-%D0%BF%D0%BE%D0%BF%D0%BE%D0%BB%D0%BD%D0%B8%D0%BB%D1%81%D1%8F-%D0%B4%D0%B2%D1%83%D0%BC%D1%8F-%D0%B1%D1%83%D0%BA%D0%B2%D0%B0%D0%BC%D0%B8/a-17646569
Реклама
С тех пор, как ученые расшифровали структуру ДНК — носителя наследственной информации во всех живых организмах — прошло более 60 лет. Исследователи, в частности, выяснили, что с химической точки зрения ДНК является полимером, макромолекула которого состоит из повторяющихся звеньев — нуклеотидов, что каждый нуклеотид представляет собой комбинацию из азотистого основания, сахара-дезоксирибозы и фосфатной группы, и что в молекуле ДНК встречаются лишь четыре вида азотистых оснований — аденин, гуанин, тимин и цитозин.
Они обозначаются буквами А, Г, Т и Ц, которые принято именовать генетическим алфавитом, ведь именно последовательность азотистых оснований в молекуле ДНК и является тем кодом, что обеспечивает хранение, передачу из поколения в поколение и реализацию программы развития и функционирования всех живых организмов. В популярной литературе утвердился своего рода образ-штамп: алфавитом, состоящим из четырех букв А, Г, Т, и Ц, написана книга жизни.
Ученым четырех букв генетического алфавита недостаточно
Однако в последние годы исследователи, работающие в сфере так называемой синтетической биологии, почувствовали, что столь скудного алфавита им для реализации некоторых интересных идей уже не хватает. А потому взялись за создание искусственных, не существующих в природе нуклеотидных оснований. Теперь американским ученым удалось внедрить их в геном живой бактерии — кишечной палочки Escherichia coli. Результаты работы опубликованы в журнале Nature.
Тут важно иметь в виду, что молекула ДНК практически всегда состоит из двух цепочек (двойная спираль) и что азотистые основания одной цепочки соединены водородными связями с азотистыми основаниями другой цепочки, причем аденин образует пары только с тимином, а гуанин — только с цитозином. Теперь американские генетики обогатили геном энтеробактерии парой искусственных нуклеотидных оснований. Обозначения этих субстанций больше напоминают компьютерные пароли доступа повышенной надежности, чем пригодные в практике названия: одно вещество именуется d5SICSTP, другое dNaMTP. Но сами разработчики предпочитают называть их для простоты соответственно X и Y.
Теперь американские генетики обогатили геном энтеробактерии парой искусственных нуклеотидных оснований. Обозначения этих субстанций больше напоминают компьютерные пароли доступа повышенной надежности, чем пригодные в практике названия: одно вещество именуется d5SICSTP, другое dNaMTP. Но сами разработчики предпочитают называть их для простоты соответственно X и Y.
Природные нуклеотиды гидрофильны, искусственные — гидрофобны
Оба искусственных азотистых основания ученые синтезировали так, чтобы они по своим химическим свойствам существенно отличались от природных. Руководитель проекта Флойд Роумсберг (Floyd Romesberg), профессор химии в Исследовательском институте Скриппса в Ла-Холья, штат Калифорния, говорит: «Природные пары азотистых оснований характеризуются чрезвычайно высокой гидрофильностью, они образуют между собой водородные связи. Мы же хотели, чтобы наши искусственные основания с ними не смешивались — как жир и вода, — поэтому изначально конструировали их так, чтобы они были гидрофобными».
На поиск подходящих субстанций у профессора Роумсберга и его коллег ушло более десяти лет. С одной стороны, это должны были быть вещества, вообще не встречающиеся в природе. С другой стороны, имеющаяся в любой живой клетке ферментная система репарации, исправляющая повреждения ДНК, должна была не замечать данную аномалию, не воспринимать эти искусственные субстанции как чужеродные и подлежащие удалению. Все клеточные механизмы должны были работать как обычно, обрабатывать наследственную информацию так же, как если бы она была записана алфавитом из стандартных четырех букв, а не из шести. И в процессе деления клетки репликация этой необычной молекулы ДНК должна была, как положено, приводить к образованию двух дочерних копий, идентичных исходной родительской.
Многое пока неясно, но перспективы интересные
«Мы уже много лет занимаемся созданием неприродных нуклеотидов, — поясняет профессор Роумсберг. — Мы испробовали более 300 вариантов. Однако лишь теперь мы подобрали, наконец, такую пару нуклеотидных оснований, которую удалось интегрировать в живую бактерию. И добиться нормальной репликации этой необычной ДНК».
И добиться нормальной репликации этой необычной ДНК».
Пока, правда, неясно, выживет ли бактерия, если в ее геном внедрить не одну пару оснований X-Y, а множество таких пар. Неясно также, долго ли проживет такая полусинтетическая кишечная палочка и долго ли в ней будут сохраняться чужеродные буквы генетического алфавита. По крайней мере, в журнале Nature речь идет лишь о 24 репликациях в течение 15 часов. А самое главное, неясно, способны ли искусственные нуклеотиды участвовать в производстве белков.
Но профессор Роумсберг надеется, что генетический код из шести вместо четырех букв позволит придать бактерии целый ряд полезных биохимических свойств, которых она изначально не имела: «Если вы расширите генетический код за счет неприродных нуклеотидов, кодирующих дополнительные аминокислоты, то это даст возможность получать новые белки с необычными свойствами. Например, так можно производить лучшие лекарства — и быстрее».
Безопасность гарантированая самой природой
Никакой опасности для окружающей среды такие бактерии не представляют, подчеркивает ученый. Напротив, они гораздо легче поддаются контролю, чем генетически модифицированные микроорганизмы, полученные методами традиционной генной инженерии. «Мы должны снабжать наши бактерии неприродными компонентами ДНК, — поясняет профессор Роумсберг. — Бактерии не могут синтезировать эти нуклеотиды самостоятельно, нам приходится их кормить. С этой целью мы добавляем вещества Х и Y в питательную среду, а в геном кишечной палочки мы внедрили растительный ген, который придает водоросли — а теперь и нашей бактерии — способность поглощать нуклеотиды из окружающей среды. Если же прекратить подкормку бактерий искусственными нуклеотидами, все неприродное из ДНК кишечной палочки быстро исчезнет».
Напротив, они гораздо легче поддаются контролю, чем генетически модифицированные микроорганизмы, полученные методами традиционной генной инженерии. «Мы должны снабжать наши бактерии неприродными компонентами ДНК, — поясняет профессор Роумсберг. — Бактерии не могут синтезировать эти нуклеотиды самостоятельно, нам приходится их кормить. С этой целью мы добавляем вещества Х и Y в питательную среду, а в геном кишечной палочки мы внедрили растительный ген, который придает водоросли — а теперь и нашей бактерии — способность поглощать нуклеотиды из окружающей среды. Если же прекратить подкормку бактерий искусственными нуклеотидами, все неприродное из ДНК кишечной палочки быстро исчезнет».
Значит, если даже такой полусинтетический микроорганизм ускользнет из лаборатории, выжить ему не суждено. Или же он откажется от неприродных компонентов в своем геноме и превратится в самую обычную бактерию, какой и был изначально.
Написать в редакцию
Реклама
Пропустить раздел Топ-тема
1 стр. из 3
из 3
Пропустить раздел Другие публикации DW
На главную страницу
Химики создали транскрибируемую синтетическую ДНК с восьмибуквенным алфавитом
Химия
Биология
Генетика
Сложность
6.2
Shuichi Hoshika
Американские химики синтезировали новые четыре аналога
азотистых оснований, которые формируют пары по принципу комплементарности так
же, как это делают природные основания A,T,G,C в составе ДНК
живых организмов. Как показали ученые в статье в Science, полимер, содержащий все восемь букв
(«хатимодзи-ДНК»), напоминает по свойствам обычную ДНК и соответствует
критериям носителя информации. Более того, с восьмибуквенной матрицы при помощи
Более того, с восьмибуквенной матрицы при помощи
природного фермента удалось синтезировать молекулу РНК.
Информация в молекулах ДНК у всех живых организмов на Земле
кодируется с использованием всего четырех букв генетического алфавита — A,T,G,C, за
которыми скрываются азотистые основания пуринового и пиримидинового типа аденин,
тимин, гуанин и цитозин. Эти четыре основания формируют пары по принципу
комплементарности (A-T, G-C), которые удерживаются водородными связями. Любая
последовательность букв формирует двойную спираль ДНК, которая обладает
упорядоченной определенным образом структурой.
Эрвин Шредингер, рассуждая о природе носителя информации, предположил, что он представляет собой атипичный кристалл, мутации в котором не
приводят к утрате свойств кристалла. Авторы новой статьи в Science (где и цитируется Шредингер), химики из Firebird Biomolecular
Sciences во Флориде под руководством Стивена Беннера (Steven Benner),
одного из пионеров синтетической биологии, расширили генетический алфавит с
четырех букв до восьми. Ученые показали, что получившийся полимер в той же степени соответствует
Ученые показали, что получившийся полимер в той же степени соответствует
критериям Шредингера, что и природная ДНК. Такой полимер авторы назвали «хатимодзи-ДНК»,
что переводится как «восемь букв».
Пары оснований внутри хатимодзи ДНК и в дуплексе ДНК-РНК
Shuichi Hoshika et al / Science 2019
Поделиться
Ученые синтезировали две новых пары, Z-P и S-B, которые
тоже удерживаются водородными связями, и проанализировали свойства двойной
спирали с расширенным алфавитом. Они показали, что такие цепочки обладают
регулярной структурой и предсказуемыми термодинамическими свойствами вне
зависимости от последовательности. Кроме того, ученые показали, что с хатимодзи-матрицы
можно синтезировать цепочку РНК.
В этом эксперименте ученые использовали вирусную T7 РНК-полимеразу, которая
синтезировала на ДНК-матрице с использованием соответствующих рибонуклеотидов цепочку
хатимодзи-РНК, складывающуюся в определенную структуру (аптамер). Структура, в
Структура, в
свою очередь, связывала молекулу флуоресцентного красителя, которая при этом активировалась.
Таким образом, синтез РНК можно было детектировать по свечению раствора.
Структура синтезируемого хатимодзи-аптамера РНК и его свойства
Shuichi Hoshika et al / Science 2019
Поделиться
Оказалось, что полимераза дикого типа способна
использовать только три новых буквы из четырех, но перебрав все имеющиеся
варианты ученые обнаружили мутантную версию полимеразы с тремя аминокислотными
заменами, которая могла вставлять в РНК все четыре новых буквы.
Таким образом, ученые расширили генетический алфавит до
восьми букв, увеличили плотность кодируемой информации и показали потенциальную
возможность ее расшифровки в живых системах. Однако это не первый такой случай:
мы рассказывали о том, как группа Флойда Ромсберга успешно реплицировала ДНК с
шестибуквенным алфавитом в бактериях и даже закодировала с ее помощью новые аминокислоты.
В этой серии работ ученые использовали другую пару X-Y, которая удерживается при помощи гидрофобных взаимодействий.
Как пишут в новой статье создатели «хатимодзи-ДНК»,
гидрофобные взаимодействия накладывают ограничения на последовательность букв,
в которых можно использовать такую пару, потому что протяженные участки из
таких пар в конечном итоге нарушают структуру ДНК. Свою восьмибуквенную ДНК
авторы пока собираются использовать не для расширения генетического кода, а в
более прикладных целях, например, для бар-кодирования последовательностей при
секвенировании, создания наноструктур с заданными свойствами или для хранения
информации вне клетки (о том как используют ДНК в качестве внешнего носителя,
можно прочитать в нашем блоге).
Дарья Спасская
Генетический алфавит. Путешествие в страну микробов
Генетический алфавит. Путешествие в страну микробов
ВикиЧтение
Путешествие в страну микробов
Бетина Владимир
Содержание
Генетический алфавит
Авторы модели ДНК представляют систему «кодирования» следующим образом: различные свойства ДНК в разных организмах объясняются различием в составе нуклеотидов в ее молекуле. Нуклеотиды, по их мнению, являются своего рода генетическим алфавитом, при помощи которого в ДНК «химическим почерком» закодированы наследственные особенности организма. А поскольку ДНК содержит по меньшей мере несколько тысяч нуклеотидов, возникают неограниченные возможности комбинаций во взаимном чередовании и порядке пар А — Т, Г — Ц в ее молекуле. Каждая новая комбинация придает новые свойства ДНК.
Нуклеотиды, по их мнению, являются своего рода генетическим алфавитом, при помощи которого в ДНК «химическим почерком» закодированы наследственные особенности организма. А поскольку ДНК содержит по меньшей мере несколько тысяч нуклеотидов, возникают неограниченные возможности комбинаций во взаимном чередовании и порядке пар А — Т, Г — Ц в ее молекуле. Каждая новая комбинация придает новые свойства ДНК.
Молекулы ДНК в клетке, поясняют далее Дж. Уотсон и Ф. Крик, способны к «самовоспроизведению» (редупликации) с сохранением постоянного расположения нуклеотидов. Мы знаем, что внутренний «цилиндр» молекулы ДНК состоит из пар оснований А — Т и Г — Ц, соединенных между собой водородными связями. Редупликация молекул ДНК может идти следующим образом. Водородные связи между парными нуклеотидами на одном конце молекулы постепенно начинают прерываться и обе спиральные цепи ДНК «разматываются», освобождаясь друг от друга. Такая развернувшаяся цепь удерживается связями между остатками молекул дезоксирибозы и фосфорной кислоты, «выставив» перпендикулярно оси свои основания. В окружающей среде находятся синтезированные клеткой свободные нуклеотиды, которые могут входить в реакцию со свободными основаниями развернутой цепи ДНК. Но к каждому основанию может приблизиться и соединиться с ним только нуклеотид, имеющий парное, «дополняющее» основание. Это значит, что к развернутой цепи начнет присоединяться другая, недостающая цепь ДНК, причем точно такая, какая была в другой половине макромолекулы и отделилась, чтобы подобным же образом извлечь из среды то, чего ей недостает до полной молекулы ДНК. В результате этих процессов образуются две молекулы ДНК, каждая из которых имеет половину материнской молекулы, дополненную вновь синтезированной. Дочерние молекулы становятся, таким образом, точной копией материнской ДНК. При этом сохраняется и состав генетического материала.
В окружающей среде находятся синтезированные клеткой свободные нуклеотиды, которые могут входить в реакцию со свободными основаниями развернутой цепи ДНК. Но к каждому основанию может приблизиться и соединиться с ним только нуклеотид, имеющий парное, «дополняющее» основание. Это значит, что к развернутой цепи начнет присоединяться другая, недостающая цепь ДНК, причем точно такая, какая была в другой половине макромолекулы и отделилась, чтобы подобным же образом извлечь из среды то, чего ей недостает до полной молекулы ДНК. В результате этих процессов образуются две молекулы ДНК, каждая из которых имеет половину материнской молекулы, дополненную вновь синтезированной. Дочерние молекулы становятся, таким образом, точной копией материнской ДНК. При этом сохраняется и состав генетического материала.
Здесь мы должны, однако, предупредить читателя, что то, о чем он только что прочел, было всего-навсего гипотезой Уотсона и Крика о редупликации ДНК. Вы можете справедливо заметить, что правильность гипотез должна быть доказана экспериментально.
Описанную гипотезу подтвердил американский биохимик А. Корнберг, которому удалось открыть полимеразу ДНК — фермент, участвующий в процессе редупликации. Получив из клеток кишечных бактерий Escherichia coli ДНК и фермент, он соединил их в пробирке, добавив туда же смесь соответствующих нуклеотидов. Через некоторое время количество ДНК в пробирке значительно увеличилось, причем были использованы присутствующие в среде свободные Нуклеотиды. За свое открытие он получил в 1959 году Нобелевскую премию по физиологии и медицине. Эту премию разделил с ним профессор С. Очоа, открывший независимо от Корнберга фермент — полимеразу РНК, которая синтезирует рибонуклеиновую кислоту. Совсем недавно Корнберг обнаружил еще один фермент, участвующий в синтезе ДНК, и назвал его фосфатазой ДНК.
Модель редупликации молекулы ДНК. К развернутым цепочкам (вверху) присоединяются дополнительные цепочки того же состава, что и в материнской молекуле.
Гипотезу о редупликации ДНК подтвердили в 1958 году М. С. Месельсон и Ф. Сталь. Они культивировали бактерии Е. coli в жидкой питательной среде, содержащей вещества с радиоактивным азотом 15N. ДНК этих бактерий оказалась потом «меченной» радиоактивным элементом всюду, где в ее макромолекулах содержится атом азота. Затем ученые культивировали бактерии в жидкой питательной среде, содержащей нерадиоактивный азот 14N. При выращивании бактерии размножались, и можно было наблюдать, как радиоактивный азот ДНК равномерно распределялся по дочерним молекулам ДНК. В каждой последующей генерации бактерий отмечалась половинная радиоактивность ДНК по сравнению с предыдущей. Иначе говоря, при каждой редупликации ДНК радиоактивность материнской макромолекулы равномерно распределялась в двух дочерних макромолекулах, которые создавали недостающие им цепи, привлекая для этого нуклеотиды с нормальным азотом.
С. Месельсон и Ф. Сталь. Они культивировали бактерии Е. coli в жидкой питательной среде, содержащей вещества с радиоактивным азотом 15N. ДНК этих бактерий оказалась потом «меченной» радиоактивным элементом всюду, где в ее макромолекулах содержится атом азота. Затем ученые культивировали бактерии в жидкой питательной среде, содержащей нерадиоактивный азот 14N. При выращивании бактерии размножались, и можно было наблюдать, как радиоактивный азот ДНК равномерно распределялся по дочерним молекулам ДНК. В каждой последующей генерации бактерий отмечалась половинная радиоактивность ДНК по сравнению с предыдущей. Иначе говоря, при каждой редупликации ДНК радиоактивность материнской макромолекулы равномерно распределялась в двух дочерних макромолекулах, которые создавали недостающие им цепи, привлекая для этого нуклеотиды с нормальным азотом.
Жакоб и Моно обдумывают генетический код
Жакоб и Моно обдумывают генетический код
Итак, по мнению Крика и его коллег, ДНК можно считать химическим носителем наследственности, иначе говоря, ДНК — это определяющая составная часть генов.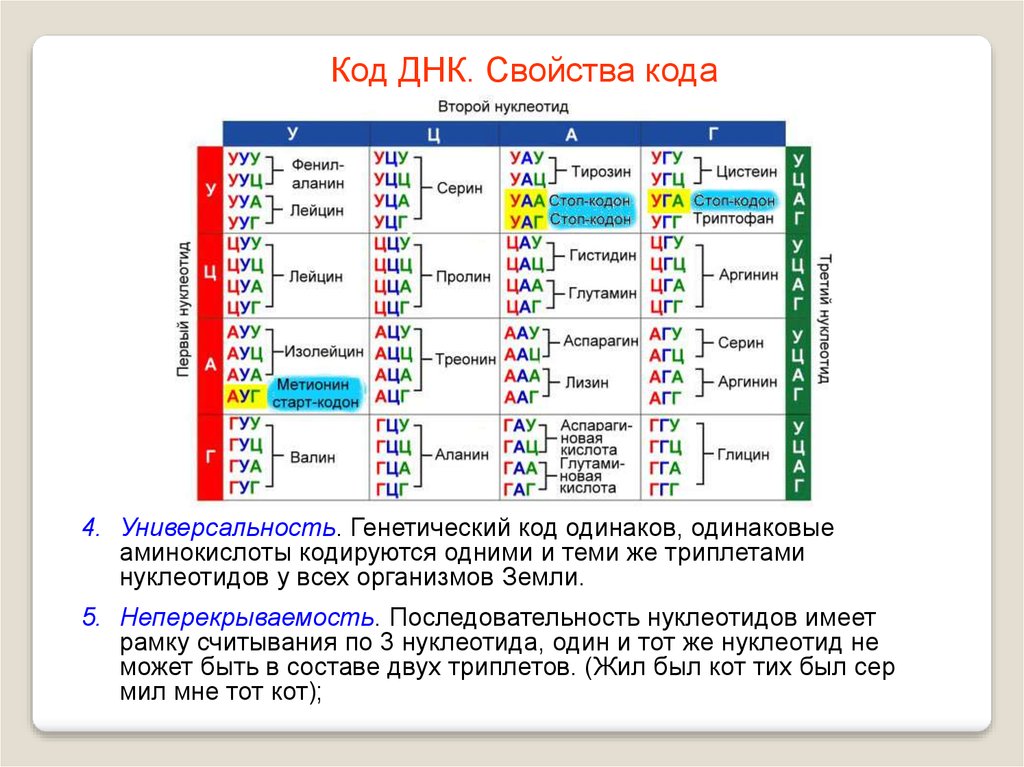 Бидл и Тейтем уже давно сформулировали положение «один ген — один фермент»,
Бидл и Тейтем уже давно сформулировали положение «один ген — один фермент»,
3.2. Генетический материал эукариот
3.2. Генетический материал эукариот
Генетический материал эукариот сконцентрирован в ядре и представлен хромосомами, в которых молекула ДНК образует сложный комплекс с различными белками.Каждая клетка любого организма содержит определенный набор хромосом.
4.2. Генетический анализ
4.2. Генетический анализ
Совокупность методов изучения наследственности получила название «генетический анализ». Его основа – гибридологический метод, разработанный Г. Менделем. С открытия законов наследования Г. Менделем и начинается история генетики. Не меньшая
6.2. Генетический код
6.2. Генетический код
Генетическая информация записывается последовательностями нуклеотидов в нуклеиновых кислотах с помощью 4 символов, как информация текста книги записывается с помощью букв, количество которых зависит от конкретного алфавита. В структуру белка эта
В структуру белка эта
ГЕНЕТИЧЕСКИЙ АНАЛИЗ
ГЕНЕТИЧЕСКИЙ АНАЛИЗ
В 1980 годах профессор Алек Джеффрис из Лестерского университета доказал наличие многочисленных участков ДНК, которые не следует считать кодом аминокислот. Эти участки назвали минисателлитные ДНК. Тысячи ДНК разбросаны по всем хромосомам; возможно,
Глава G@C. Генетический код явление «героя» (X)
Глава G@C. Генетический код ? явление «героя» (X)
События, связанные с эволюцией Вселенной и коротко описанные выше, привели, в конечном счете (а может быть, и «в том числе») к возникновению жизни, центральным феноменом которой стало объединение мира нуклеиновых кислот и мира
Генетический код
Генетический код
Поскольку информация о структуре белков в ДНК и и-РНК записана последовательностью нуклеотидов, для перезаписи в последовательность аминокислот должна существовать система кодировки, которая получила название «генетический код». Генетический код –
Генетический код –
Как взломать генетический замок
Как взломать генетический замок
Однако эволюционные черепахи перемешивают свои гены сильнее, чем эволюционные зайцы. Открытие Остина Берта о связи между длиной поколения и количеством рекомбинаций свидетельствует о том, что Черная Королева работает. Чем длительнее
Глава 4 Пол и генетический мятеж
Глава 4
Пол и генетический мятеж
Черепаха живет между двух пластин,
Она или он — вид один.
Черепаха, я думаю, очень умна,
Раз так, притом, плодовита она.
Огден Нэш (пер. О. Волковой).
В средневековых английских деревнях одно пастбище было общинным. Каждый имел право пасти
Приложение. Генетический код
Приложение. Генетический код
Генетический код — это небольшой словарь, который устанавливает связь между языком нуклеиновых кислот из четырех букв и языком белков из двадцати букв.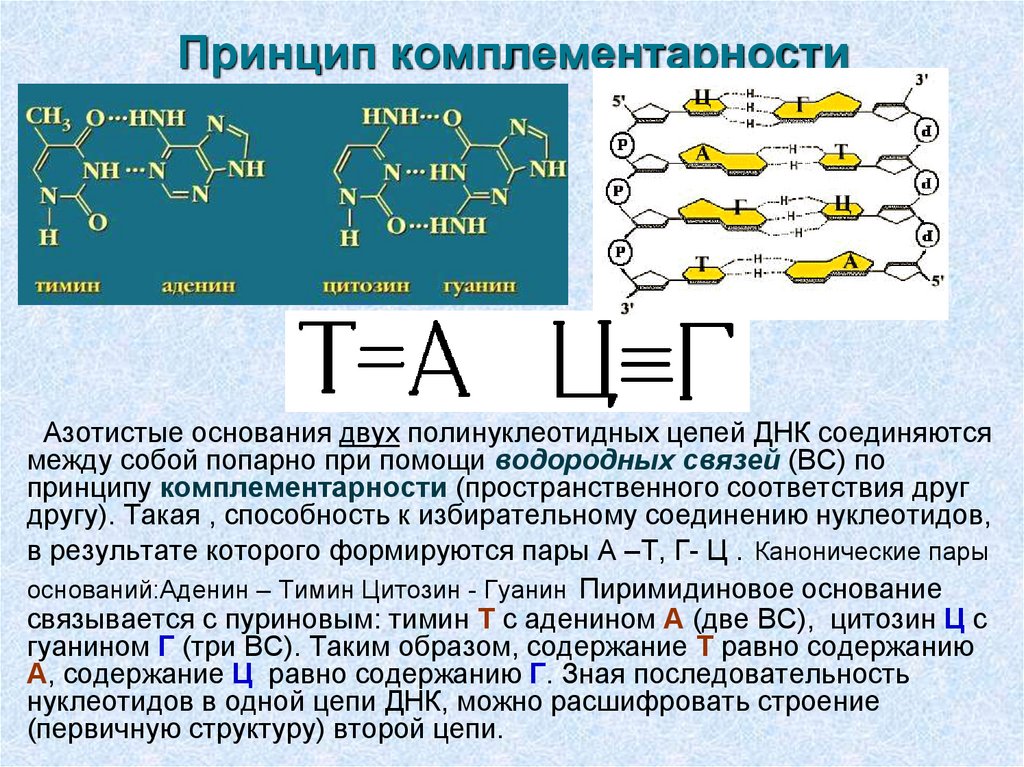 Каждый триплет оснований соответствует определенной аминокислоте, за исключением трех
Каждый триплет оснований соответствует определенной аминокислоте, за исключением трех
Генетический допинг
Генетический допинг
Генотерапия
Мы знаем, что человек страдает тяжелыми заболеваниями, если имеет дефектные варианты генов. Изменения в гене, из-за которых может возникнуть болезнь, называют патогенной мутацией. Сегодня известны примерно 1500 генов, несущих в себе
Генетический возраст
Генетический возраст
Итак, человек умирает. Ну хорошо – все мы рано или поздно умрем. Но как это происходит? Большинство людей, с которыми я обсуждал этот вопрос в винном ресторанчике Heuring, постоянно спрашивали: если человек никогда не болеет, он все равно умрет? Есть у
Генетический рецепт
Генетический рецепт
Для меня генетическое будущее человечества, однако, выглядит совершенно иначе. И то, о чем я хочу поговорить в заключение этой книги, не когда-нибудь появится, а уже есть. Я считаю, что будущее принадлежит не изменениям в генетике человека. Знание о его
И то, о чем я хочу поговорить в заключение этой книги, не когда-нибудь появится, а уже есть. Я считаю, что будущее принадлежит не изменениям в генетике человека. Знание о его
Генетический пол
Генетический пол
Первым в списке Мани значится хромосомный (или генетический) пол. Генетические различия между мужским и женским полом представляют собой фундаментальную основу феномена пола, отражающую важнейшую черту полового размножения. У подавляющего большинства
4 Новые буквы ДНК Double Life’s Alphabet
Share на Facebook
Share в Twitter
Share на Reddit
.
Кредит: Getty Images
ДНК жизни на Земле естественным образом хранит свою информацию всего в четырех ключевых химических веществах — гуанине, цитозине, аденине и тимине, обычно называемых G, C, A и T соответственно.
Теперь ученые удвоили это количество строительных блоков жизни, впервые создав синтетический генетический язык из восьми букв, который, кажется, хранит и расшифровывает информацию точно так же, как естественная ДНК.
В исследовании, опубликованном 22 февраля в Science , консорциум исследователей во главе со Стивеном Беннером, основателем Фонда прикладной молекулярной эволюции в Алачуа, Флорида, предполагает, что расширенный генетический алфавит теоретически может также поддерживать жизнь .
«Это настоящая достопримечательность, — говорит Флойд Ромесберг, химик-биолог из Научно-исследовательского института Скриппса в Ла-Хойя, Калифорния. По словам Ромесберга, исследование предполагает, что в этих четырех химических веществах, возникших на Земле, нет ничего особенно «волшебного» или особенного. «Это концептуальный прорыв», — добавляет он.
Обычно, когда пара нитей ДНК закручивается вокруг друг друга в виде двойной спирали, химические вещества каждой нити образуют пары: А связывается с Т, а С связывается с G.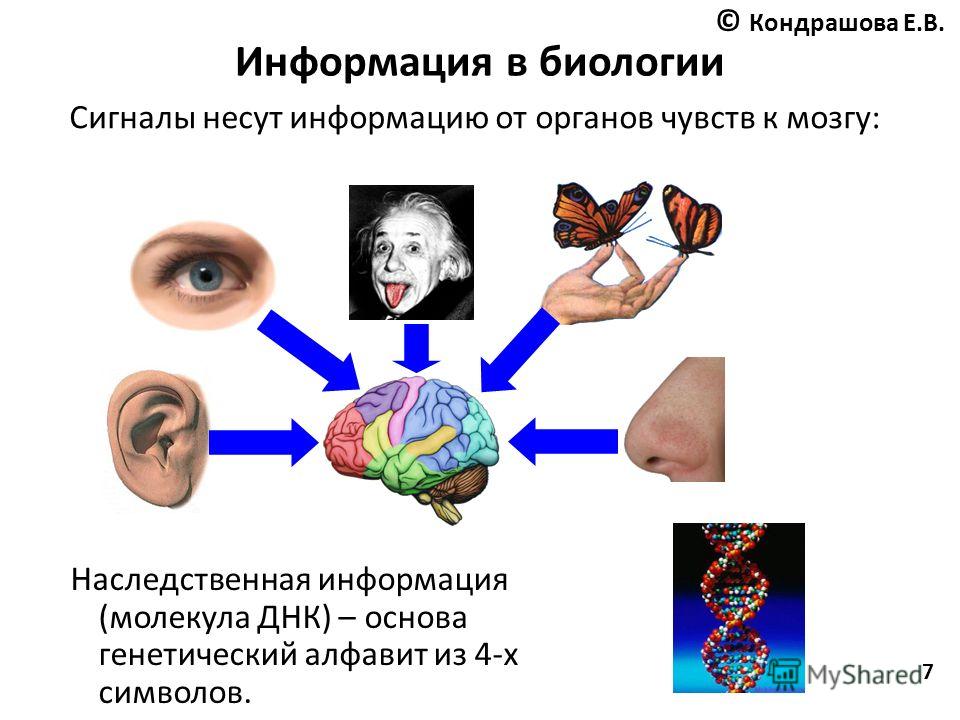
Долгое время ученые пытались добавить больше пар этих химических веществ, также известных как основания, к этому генетическому коду. Например, Беннер впервые создал «неестественные» базы в 19 веке.80-е годы. За ними последовали и другие группы: в 2014 году лаборатория Ромесберга попала в заголовки газет после того, как вставила пару неестественных оснований в живую клетку.
Но последнее исследование впервые систематически демонстрирует, что комплементарные неестественные основания распознают и связываются друг с другом, и что двойная спираль, которую они образуют, сохраняет свою структуру.
Команда Беннера, в которую входят исследователи из различных компаний и учреждений США, создала синтетические буквы, изменив молекулярную структуру обычных оснований. Буквы ДНК образуют пары, потому что они образуют водородные связи: каждая содержит атомы водорода, которые притягиваются к атомам азота или кислорода своего партнера. Беннер объясняет, что это немного похоже на кубики Lego, которые соединяются вместе, когда отверстия и зубцы совпадают.
Путем регулировки этих отверстий и штырей команда придумала несколько новых пар оснований, в том числе пару с именами S и B и еще одну, названную P и Z. В последнем документе они описывают, как они комбинируют эти четыре синтетических основания. с натуральными. Исследователи назвали получившийся восьмибуквенный язык «хатимодзи» в честь японских слов «восемь» и «буква». Каждое из дополнительных оснований похоже по форме на одно из четырех естественных, но имеет разные схемы связывания.
Затем исследователи провели серию экспериментов, которые показали, что их синтетические последовательности имеют общие свойства с природной ДНК, необходимые для поддержания жизни.
Поиск данных
Чтобы работать как система хранения информации, ДНК должна следовать предсказуемым правилам, поэтому команда впервые продемонстрировала, что, подобно обычным основаниям, синтетические основания надежно образуют пары. Они создали сотни молекул синтетической ДНК и обнаружили, что буквы предсказуемо связываются со своими партнерами.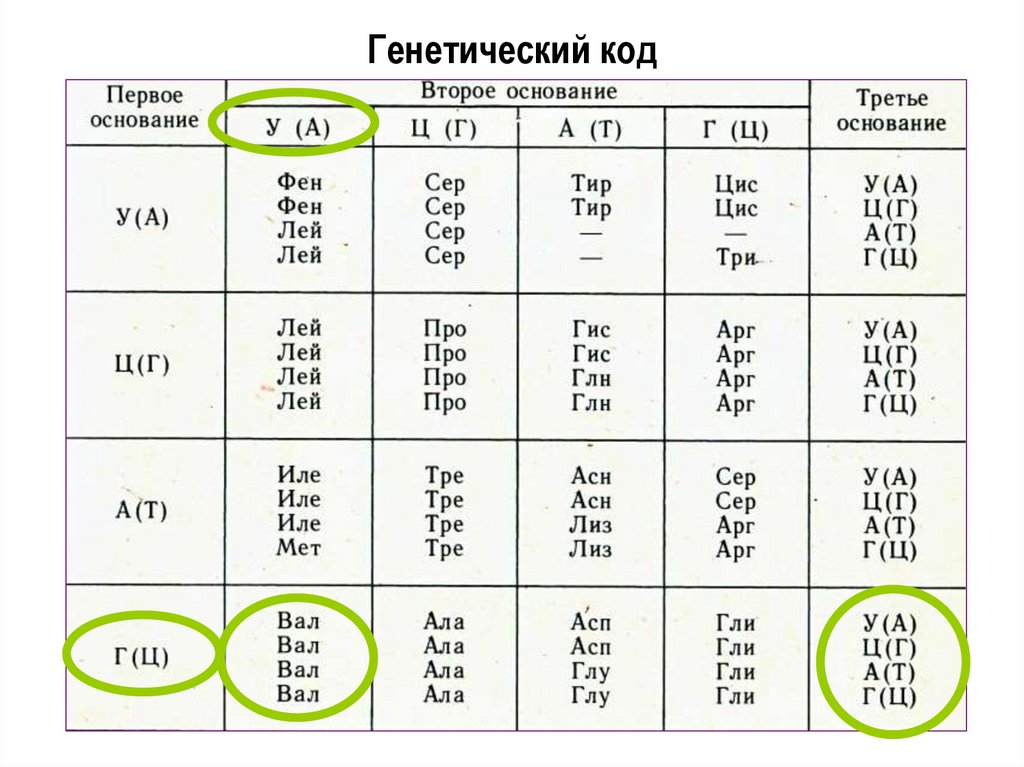
Затем они показали, что структура двойных спиралей остается стабильной независимо от порядка расположения синтетических оснований. Это важно, потому что для развития жизни последовательности ДНК должны иметь возможность изменяться без разрушения всей структуры. Используя рентгеновскую дифракцию, команда показала, что три разные последовательности синтетической ДНК сохраняют одинаковую структуру при кристаллизации.
Это значительный прогресс, говорит Филипп Холлигер, биолог-синтетик из Лаборатории молекулярной биологии MRC в Кембридже, Великобритания, потому что другие методы расширения генетического алфавита не являются столь структурно обоснованными. Вместо химических веществ, которые используют водородные связи для образования пар, в этих других подходах в качестве основы используются водоотталкивающие молекулы. Их можно размещать с промежутками между естественными буквами, но структура ДНК нарушается, если они расположены в ряд.
Наконец, команда показала, что синтетическая ДНК может быть точно транскрибирована в РНК. «Способность хранить информацию не очень интересна для эволюции», — говорит Беннер. «Вы должны быть в состоянии передать эту информацию в молекулу, которая что-то делает».
«Способность хранить информацию не очень интересна для эволюции», — говорит Беннер. «Вы должны быть в состоянии передать эту информацию в молекулу, которая что-то делает».
Преобразование ДНК в РНК является ключевым этапом преобразования генетической информации в белки, рабочие лошадки жизни. Но некоторые последовательности РНК, известные как аптамеры, сами могут связываться со специфическими молекулами.
Команда Беннера создала синтетическую ДНК, которая кодирует определенный аптамер, а затем подтвердила, что транскрипция произошла и последовательность РНК функционирует правильно.
Холлигер говорит, что работа является захватывающей отправной точкой, но до создания настоящей восьмибуквенной синтетической генетической системы еще далеко. Один из ключевых вопросов, например, будет заключаться в том, может ли синтетическая ДНК реплицироваться полимеразами, ферментами, ответственными за синтез ДНК внутри организмов во время клеточного деления. Это было продемонстрировано для других методов, таких как метод Ромесберга, в котором используются водоотталкивающие основы.
Разнообразие жизни
Тем не менее, Беннер говорит, что работа показывает, что жизнь потенциально может поддерживаться основаниями ДНК с отличной от четырех известных нам структурой, что может иметь значение при поиске признаков жизни в других местах во Вселенной.
Добавление букв к ДНК также может иметь более приземленное применение.
Благодаря большему разнообразию генетических строительных блоков ученые потенциально могут создавать последовательности РНК или ДНК, которые могут делать вещи лучше, чем стандартные четыре буквы, включая функции, выходящие за рамки генетического хранения.
Например, группа Беннера ранее показала, что нити ДНК, включающие Z и P, лучше связываются с раковыми клетками, чем последовательности только из четырех стандартных оснований. А Беннер создал компанию, которая занимается коммерциализацией синтетической ДНК для использования в медицинской диагностике.
Исследователи потенциально могут использовать свою синтетическую ДНК для создания новых белков, а также РНК. Команда Беннера также разработала дополнительные пары новых оснований, открыв возможность создания структур ДНК, содержащих 10 или даже 12 букв. Но тот факт, что исследователи уже расширили генетический алфавит до восьми, сам по себе примечателен, говорит Ромесберг. «Это уже удваивает то, что есть в природе».
Команда Беннера также разработала дополнительные пары новых оснований, открыв возможность создания структур ДНК, содержащих 10 или даже 12 букв. Но тот факт, что исследователи уже расширили генетический алфавит до восьми, сам по себе примечателен, говорит Ромесберг. «Это уже удваивает то, что есть в природе».
Эта статья воспроизведена с разрешения и впервые опубликована 21 февраля 2019 года.
ОБ АВТОРАХ
Читать дальше вирус под названием S-2L, поражающий цианобактерии, не имеет аденина в своем геноме. Вместо этого в S-2L используется нуклеотид, известный как диаминопурин или 2-аминоаденин, сокращенно до Z, который образует три водородные связи, а не две, которые образует аденин (А), в паре с тимином (Т). В трех статьях, опубликованных сегодня (29 апреля) в
Science, исследователи показывают, что использование Z фагами, теми вирусами, которые заражают бактерии, более широко распространены, чем считалось ранее, и они описывают пути, по которым альтернативный нуклеотид создается и включается в фаговые геномы.
«Известно, что есть фаг, в геноме которого нет аденина. . . и это было неразгаданной загадкой о том, как он это делает», — говорит Джеф Бёке, молекулярный биолог из Медицинской школы Гроссмана Нью-Йоркского университета, который не участвовал в работе. Эти статьи «излагают это в великолепных молекулярных деталях», — говорит он.0033 Ученый . Кроме того, авторы «проделали удивительно всеобъемлющую работу, показав, что это не один сумасшедший выброс, а целая группа бактериофагов, обладающих таким генетическим материалом».
В 1998 году Пьер Александр Камински из Института Пастера и его коллеги секвенировали геном цианофага S-2L в надежде расшифровать пути, позволяющие вирусу обходить канонический нуклеотидный код. Они нашли последовательность, связанную с purA — геном, кодирующим сукциноаденилатсинтазу, один из ферментов пути синтеза аденина, — которая казалась хорошей зацепкой, но затем отложили проект из-за проблем, связанных с работой с фагом и его цианобактериальный хозяин.
В последующие годы исследователи периодически проводили поиск в базах данных и сравнивали опубликованные последовательности с геном, подобным purA-. В конце 2015 года они обнаружили гомологичную последовательность в фаге Vibrio , который заражает Vibrio , род грамотрицательных бактерий, с которыми гораздо легче работать, чем с цианобактериями-хозяевами S-2L. Последовательности purA--подобных генов в фагах S-2L и Vibrio были более сходны друг с другом, чем с другими известными гены purA , что указывает на то, что фаг Vibrio также может использовать диаминопурин в своей ДНК.
С 1977 года цианофаг казался какой-то разовой проблемой и не очень интересной, но они действительно дали понять, что он существует, и в большем количестве мест, чем мы ожидаем.
— Дэвид Данлэп, Университет Эмори
Команда проанализировала состав ДНК фага Vibrio и обнаружила, что он действительно содержит диаминопурин вместо аденина.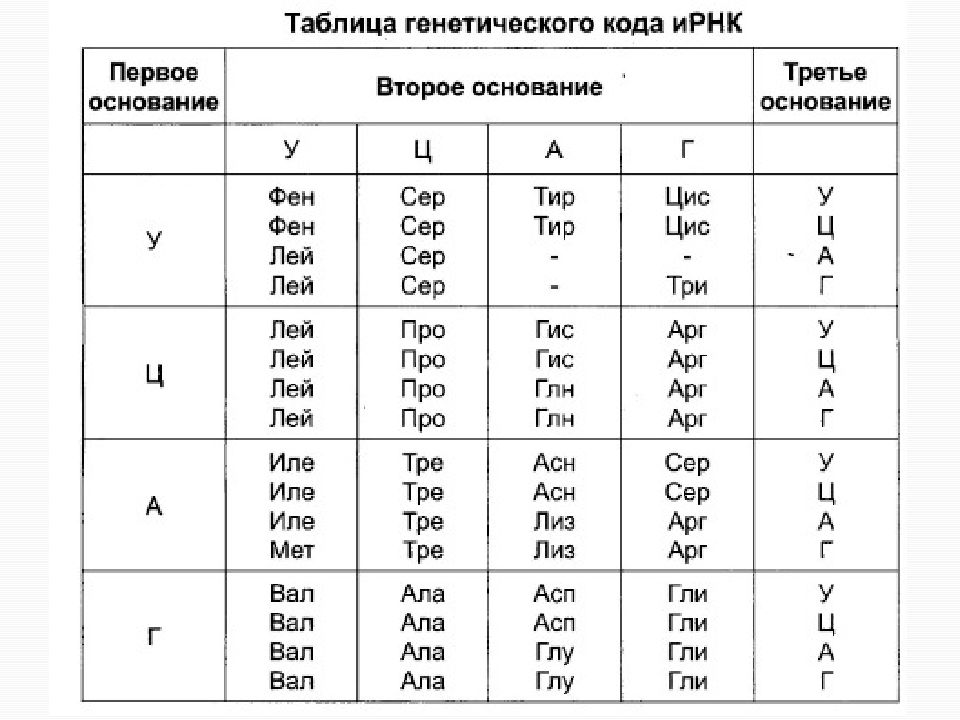 Они описывают эти результаты в одной из сегодняшних статей, а также структуру и функцию in vitro фермента, кодируемого purA -подобный ген, который они называют PurZ. Они показывают, что PurZ выполняет сходную функцию в пути биосинтеза Z с PurA в синтезе аденина, и что геномы бактериофагов также содержат другой фермент, участвующий в создании Z, известный как PurB.
Они описывают эти результаты в одной из сегодняшних статей, а также структуру и функцию in vitro фермента, кодируемого purA -подобный ген, который они называют PurZ. Они показывают, что PurZ выполняет сходную функцию в пути биосинтеза Z с PurA в синтезе аденина, и что геномы бактериофагов также содержат другой фермент, участвующий в создании Z, известный как PurB.
Они также идентифицировали 19 генов purZ у различных типов бактериофагов, которые филогенетически кластеризуются с генами purA , присутствующими у архей.
«Поразительно, как далеко это уходит. . . в филогении», — говорит Дэвид Данлэп, биофизик из Университета Эмори, не участвовавший в работе. «Эти вещи развивались параллельно в течение длительного времени. С 1977, цианофаг казался какой-то разовой проблемой и не очень интересной, но они действительно дали понять, что он есть, и в большем количестве мест, чем мы ожидаем».
См. «Являются ли фаги недооцененными медиаторами здоровья и болезней?»
Во втором исследовании та же команда определила фаговые гены, кодирующие ДНК-полимеразы, которые избирательно включают диаминопурин вместо аденина.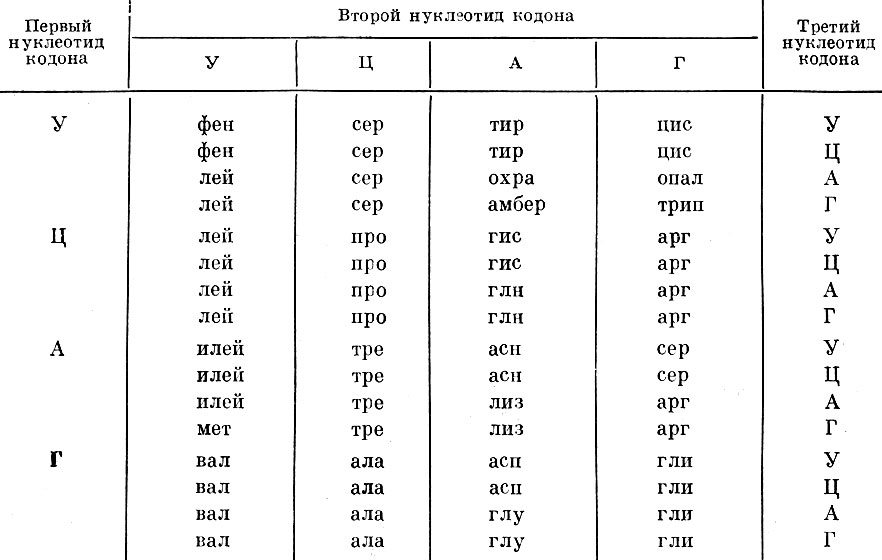 Исходный фаг S-2L, по-видимому, не содержит ни одного из этих генов, но содержит девять других фаговых геномов, в том числе Vibrio , действительно включают ген полимеразы, который авторы назвали dpoZ . В фаге Vibrio и других фаговых геномах этот ген ДНК-полимеразы был обнаружен рядом с геном purZ .
Исходный фаг S-2L, по-видимому, не содержит ни одного из этих генов, но содержит девять других фаговых геномов, в том числе Vibrio , действительно включают ген полимеразы, который авторы назвали dpoZ . В фаге Vibrio и других фаговых геномах этот ген ДНК-полимеразы был обнаружен рядом с геном purZ .
Независимая группа, возглавляемая Хуймином Чжао из Университета Иллинойса, подтверждает эти результаты в третьем опубликованном сегодня исследовании, в то же время описывая дополнительные характеристики ферментов, ответственных за синтез геномов, содержащих Z и Z, и идентифицируя десятки геномов фагов, распространенных по всему миру, которые содержат гены, кодирующие эти ферменты. Группа Чжао также обнаружила консервативный фермент, закодированный в нескольких геномах фагов, который поддерживает синтез Z-генома за счет истощения аденозинтрифосфата и его предшественника из пула нуклеотидов хозяина, тем самым предотвращая включение А фагами в их геномы.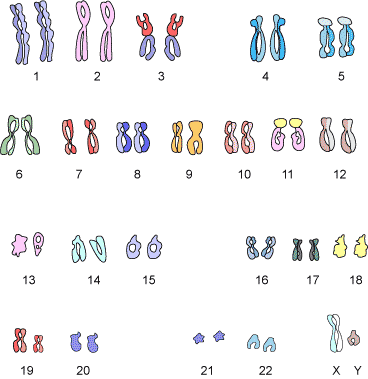
Помимо использования PurZ и PurB, эти фаги также захватывают ферменты хозяина, чтобы помочь синтезировать диаминопурин и включить его в геном фага. Наконец, исследователи показали, что Z-содержащие геномы устойчивы к деградации ферментами рестрикции хозяина.
«Если вы хотите иметь геном, содержащий диаминопурины, вам придется устранить конкурента», — объясняет Данлэп. «Фаг входит в адениновый мир и должен навязывать свою волю».
Чжао и его коллеги изучают, как использовать это проявление фаговой воли для таких приложений, как лечение бактериальных инфекций. По его словам, исследователи уже использовали фаги для лечения некоторых бактериальных инфекций, но включение этого пути в эти фаги может сделать их еще более эффективными, поскольку они будут устойчивы к деградации их бактериальными мишенями.
«Очень много вопросов остаются без ответа, — говорит Камински. В опубликованной ранее в этом месяце статье, соавтором которой он является, исследователи пролили свет на один из этих вопросов — как копируется геном S-2L — путем идентификации соответствующей полимеразы. Но Камински объясняет, что один из самых сложных вопросов, на который нужно ответить, — когда этот механизм развился. «Предполагается, что он древний, потому что глубоко уходит корнями в филогенетическое дерево и из-за сходства [ферментативных] структур», но неясно, какие геномы Z или A появились первыми.
Но Камински объясняет, что один из самых сложных вопросов, на который нужно ответить, — когда этот механизм развился. «Предполагается, что он древний, потому что глубоко уходит корнями в филогенетическое дерево и из-за сходства [ферментативных] структур», но неясно, какие геномы Z или A появились первыми.
D. Sleiman et al., “A third purine biosynthetic pathway encoded by aminoadenine-based viral DNA genomes,” Science , doi:10.1126/science.abe6494, 2021.
V. Pezo et al., «Неканоническая ДНК-полимеризация сипговирусами на основе аминоаденина», Science , DOI: 10.1126/Science.abe6542, 2021.
9015 9015 9015 9015 9015 9015 9015 9015 9015 9015 9015 9015 9015 9015 9015 9015 9015 9015 9015 9015 9015 9015 9015 9015 9. Широко распространенный путь замены аденина диаминопурином в фаговых геномах», Наука , doi:10.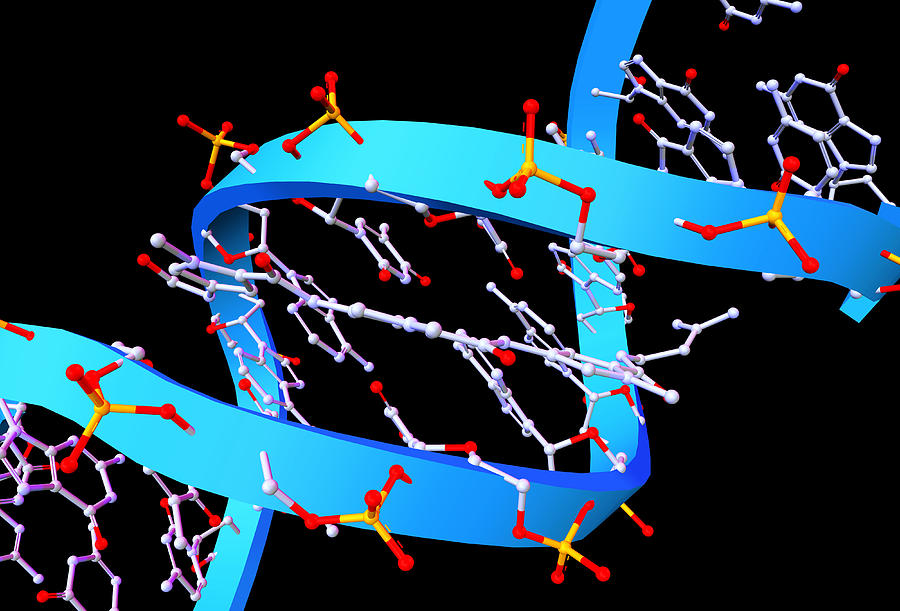 1126/science.abe4882, 2021.
1126/science.abe4882, 2021.
Генетический алфавит: расширенный или нет?
: 14 апр 2015 , Ворваться в десятку лучших , том 40,
N1
В первую десятку прорывов 2014 года входит исследование Флойда Ромесберга и его группы в Исследовательском институте Скриппса (Ла-Хойя, США), которые не только создали ДНК с двумя новыми буквами генетического кода, но и обманули ее, чтобы она реплицировалась в Escherichia coli, рабочая лошадка молекулярной биологии
Из школьных уроков биологии всем известно, что текст молекулы ДНК — хранилища генетической информации — записывается всего четырьмя буквами: А, Т, Г и Ц. Эти буквы обозначают четыре азотистых основания — аденин, тимин, гуанин и цитозин, которые присоединены к сахаро-фосфатному остову. Две получившиеся нити образуют хорошо известную двойную спираль ДНК, которая содержит схему построения и управления нашим телом.
Две цепи ДНК комплементарны: А в одной цепи всегда стоит напротив Т в другой цепи, а G всегда напротив С. «Противоположные» основания в парах соединены водородными связями, что обеспечивает согласование основания в паре. Например, между А и С не могут образовываться водородные связи; таким образом, дополнительные основания подходят как замок и ключ.
Когда в середине 20 века была открыта структура ДНК, ученые стали задаваться вопросом, почему Природа выбрала именно эти две пары оснований, а не другие, и можно ли так вмешаться в клетку, чтобы она использовала любые альтернативы? Этот вопрос до сих пор остается без ответа. Многие исследователи в области предбиотической эволюции считают, что этот выбор был сделан чисто случайно и закрепился позже, после прохождения сложнейшего этапа зарождения жизни на нашей планете — когда молекулы стали репликаторами, т. е. научились воспроизводить себя.
Вероятность этого события очень мала. Неудивительно, что даже если бы существовали комплементарные пары с другими основаниями, они прошли бы через это узкое место. Однако наиболее вероятно, что первой репликаторной молекулой была РНК, а не ДНК. В РНК вместо тимина используется другое азотистое основание — урацил, также образующий пары с аденином. При переходе в мир ДНК урацил был заменен тимином по причинам, связанным с надежностью хранения информации.
Однако наиболее вероятно, что первой репликаторной молекулой была РНК, а не ДНК. В РНК вместо тимина используется другое азотистое основание — урацил, также образующий пары с аденином. При переходе в мир ДНК урацил был заменен тимином по причинам, связанным с надежностью хранения информации.
Любопытно, что нам уже известны организмы, у которых Великая четверка отличается от описанной в учебниках. Например, ДНК многих бактериофагов (вирусов, поражающих бактерии) не содержит тимина, который заменен урацилом, гидроксиметилурацилом или другими производными урацила с дополнительным присоединением остатка сахара. Эта замена помогает вирусу защитить себя от бактериальных систем защиты, которые уничтожают чужеродную ДНК. Более того, в 19В 70-х годах ленинградские биологи нашли в самой обычной луже бактериофаг, у которого аденин был полностью заменен другим основанием — 2,6-диаминопурином.
Второй из поставленных выше вопросов послужил толчком к развитию новой области молекулярной биологии — созданию расширенного генетического кода. Исследователи, работающие в этой области, не только стремятся создать альтернативные пары оснований, но и ищут способы включения неприродных аминокислот в структуру белков (известно, что генетические системы всех известных в настоящее время живых организмов кодируют ровно 20 стандартных аминокислот). Ясно, что если мы научимся собирать ДНК из расширенного репертуара пар оснований и снабдим код способностью включать нестандартные аминокислоты в белки, мы откроем беспрецедентные новые возможности для синтетической биологии — области науки, изучающей создание живых систем и процессов, не существующих в природе.
Исследователи, работающие в этой области, не только стремятся создать альтернативные пары оснований, но и ищут способы включения неприродных аминокислот в структуру белков (известно, что генетические системы всех известных в настоящее время живых организмов кодируют ровно 20 стандартных аминокислот). Ясно, что если мы научимся собирать ДНК из расширенного репертуара пар оснований и снабдим код способностью включать нестандартные аминокислоты в белки, мы откроем беспрецедентные новые возможности для синтетической биологии — области науки, изучающей создание живых систем и процессов, не существующих в природе.
По сравнению с такой глобальной проблемой прорыв, о котором сообщает Science , выглядит не ошеломляющим открытием, а, скорее, очередной ступенькой (и не очень большой) на пути, который исследователи встали два десятилетия назад. Главный концептуальный прорыв на этом пути был сделан в конце 1990-х годов исследовательской группой под руководством Эрика Кула (Университет Рочестера, США), показавшей, что водородные связи вообще не нужны для создания стабильной пары оснований, хорошо вписывающейся в двойная спираль ДНК. Можно создать искусственные основания, не содержащие вообще атомов, способных к образованию этих связей, и они смогут не только устойчиво существовать в ДНК, но и встраиваться в ДНК обычными ДНК-полимеразными ферментами (по крайней мере, некоторыми из них).
Можно создать искусственные основания, не содержащие вообще атомов, способных к образованию этих связей, и они смогут не только устойчиво существовать в ДНК, но и встраиваться в ДНК обычными ДНК-полимеразными ферментами (по крайней мере, некоторыми из них).
Противоестественные основания также много лет изучались в лаборатории Флойда Ромесберга, результаты которых привлекли внимание Наука . Однако до недавнего времени все исследования проводились in vitro , а не в живой клетке. На этот раз команда Ромесберга взяла одну из этих неводородных пар оснований и попыталась заставить ее реплицироваться внутри бактерий E. coli , которые традиционно используются в экспериментах по молекулярной биологии.
Однако в живом организме основания не появляются по воле экспериментатора. За каждой из четырех букв ДНК стоит многоступенчатый путь их синтеза в клетке, и последние, конечно же, не могут составлять придуманные химиками противоестественные основания. Поэтому ученые схитрили: они выделили белок из клеточной стенки диатомовой водоросли Phaeodactylum tricornutum внутри бактерий, потому что этот белок может захватывать отдельные буквы ДНК непосредственно из окружающей среды. Следовательно, неприродные основания (точнее, не сами основания, а дезоксинуклеозидтрифосфаты, т. е. строительные блоки с частью сахаро-фосфатного остова, соединяющиеся в ДНК) просто добавлялись в культуральную среду, в которой росли эти бактерии. .
Следовательно, неприродные основания (точнее, не сами основания, а дезоксинуклеозидтрифосфаты, т. е. строительные блоки с частью сахаро-фосфатного остова, соединяющиеся в ДНК) просто добавлялись в культуральную среду, в которой росли эти бактерии. .
Однако оставалось решить еще одну проблему. Бактериальные клетки не могут использовать неестественные основания в больших количествах — бактерии не выживут, потому что существующий генетический аппарат не распознает их. Поэтому ученые поместили только одну неестественную пару, и даже не непосредственно в бактериальный геном, а в плазмиду, маленькую кольцевую молекулу ДНК, которая может независимо существовать и реплицироваться внутри бактериальной клетки. А поскольку фермент ДНК-полимераза III, отвечающая за массовую репликацию у бактерий, вообще не распознает нестандартные основания, ученым пришлось поместить неестественную пару оснований не просто в плазмиду, а в небольшой ее сегмент, который синтезируется другим ферментом, ДНК-полимеразой I.
После всех этих манипуляций бактерии выращивали в среде, содержащей нестандартные основания, в течение 15 часов; за это время клетки делились 24 раза. Затем исследователи проверили, что находится на том месте плазмиды, куда они поместили неестественную пару. Если бы клетка не смогла использовать совпадающие неестественные нуклеотиды для репликации и включила напротив них нормальные, то неестественная пара сохранилась бы после 24 делений только в одной плазмиде из 17 миллионов копий. Но ничего подобного не произошло: неестественная пара сохранилась в 86% копий плазмиды и в итоге была утеряна лишь через несколько дней дальнейшего роста.
Никто не может отрицать важность работы, проделанной командой Ромесберга: они первыми показали, что неестественная пара оснований может функционировать в живой клетке. Но говорить о том, что они создали организм с «расширенным генетическим алфавитом», пока рано. Якобы Nature несколько преувеличивает название статьи. Авторы статьи обошли стороной основные нерешенные проблемы искусственного генетического кода. Фактическое расширение алфавита ДНК требует, чтобы исследователи как минимум интегрировали синтез неестественных нуклеотидов в клетку, сделали эти нуклеотиды совместимыми с общей системой репликации и, самое главное, выяснили, как использовать новые буквы, чтобы сделать клетку производят новые белки.
Фактическое расширение алфавита ДНК требует, чтобы исследователи как минимум интегрировали синтез неестественных нуклеотидов в клетку, сделали эти нуклеотиды совместимыми с общей системой репликации и, самое главное, выяснили, как использовать новые буквы, чтобы сделать клетку производят новые белки.
Задача по-прежнему выглядит чрезвычайно сложной — как полет в космос на заре аэронавтики. В этом смысле работу, проделанную командой Ромесберга, можно сравнить с запуском монгольфьера братьями Монгольфье. Но в конечном итоге в космос полетели не воздушные шары. Таким образом, хотя прорыв, о котором сообщает Science , безусловно, является шагом в правильном направлении, неясно, приведет ли этот путь синтетическую биологию к ее конечному пункту назначения.
Литература
Власов В. В., Воробьев П. Е. Мир РНК: вчера и сейчас // Наука из первых рук. 2015. № 1 (40). С. 6—15.
Малышев Д. А., Дхами К., Лавернь Т. и др. Полусинтетический организм с расширенным генетическим алфавитом // Природа.
