Выращивание органов для трансплантации в лаборатории. Выращивание органов из стволовых клеток
Донор для самого себя: как вырастить стволовые клетки
Что такое стволовые клетки, как они влияют на жизнь человека и какие заболевания можно вылечить с их помощь? На эти и другие вопросы в интервью проекту "Социальный навигатор" рассказал профессор кафедр стволовых клеток и регенеративной биологии Гарвардской медицинской школы Деррик Росси накануне открытой лекции, организованной Московским физико-техническим институтом.
— Что такое стволовые клетки?
— Существует множество различных стволовых клеток. Например, эмбриональные: они отвечают за формирование тела человека. Такие клетки еще называют плюрипотентными стволовыми клетками — это означает, что они могут превращаться в любой вид тканей нашего организма.
Этот тип клеток существует только на очень ранних стадиях эмбрионального развития организма. Однако это не значит, что на этом история стволовых клеток заканчивается.
Для образования различных тканей организма в течение жизни человеку также необходимы стволовые клетки. Для этого существуют специальные стволовые клетки, которые создают замену старым или умершим клеткам в нашем теле.
Я работаю с теми стволовыми клетками, что образуют кровь, а точнее, те ее компоненты, которые перемещают кислород по нашему телу, борются с инфекциями и так далее. Существует порядка 200 различных клеток крови, которые отвечают за разные функции, и все они появляются всего лишь из стволовой клетки — гемоцитобласта, — которая живет в костном мозге. Их там не так много, но все же они есть.
У этих клеток огромный потенциал. Например, с их помощью можно вылечить лейкемию — рак крови. Возможно, вы слышали о трансплантации костного мозга. Однако на сегодняшний день она используется как средство последней надежды.
— Почему?
— Дело в том, что эта процедура довольно опасная сама по себе. В 10% случаев пересадка костного мозга оказывается летальной для пациента.
Ведь сначала человека подвергают жесткой химиотерапии или облучению радиоактивными или гамма-лучами, чтобы убить все клетки крови, а затем вводят новые, которые могут восстановить костный мозг и начать воспроизводство крови заново. При этом надо понимать, что если хоть одна клетка останется в организме человека, то болезнь вернется.
Новые стволовые клетки крови берутся у донора. Точнее, часть его костного мозга пересаживают больному. Донору даже не обязательно быть близким родственником: главное, чтобы у него и реципиента был высокий уровень совместимости. Точнее, так: чем выше, тем лучше.
Однако стоит понимать, что высокая совместимость — все равно не идеальная, поэтому будут элементы несовпадения. Из-за этого клетки донора могут начать атаковать организм реципиента, что приведет к такому заболеванию, как реакция "трансплантат против хозяина". Это очень страшная болезнь. Чем хуже совместимость, тем хуже заболевание. Именно поэтому изначально, более полувека назад, трансплантацию проводили лишь среди однояйцевых близнецов, у которых идеальная совместимость.
— Как определить степень совместимости?
— Она определяется с помощью генетического анализа системы тканевой совместимости, которая в организме представлена набором белков, находящихся на поверхности практически всех клеток организма. С их помощью последние определяют своих и чужих.
— Насколько сложно найти донора с высоким уровнем совместимости?
— По-разному, для кого-то сложно, для кого-то нет. Какие-то типы чаще встречаются, какие-то реже.
Русфонд и Казанский университет создадут регистр доноров костного мозгаПри исследовании системы тканевой совместимости человека проверяют по десяти параметрам. А вообще все просто: чем больше доноров, тем больше шанс найти высокий уровень совместимости.
— Как берут костный мозг у донора и сколько его нужно для успешной операции?
— В этой процедуре важно не количество костного мозга, а количество стволовых клеток. В костном мозге, как я уже говорил, их не так много: примерно одна клетка из 20 тысяч будет стволовой. Но, например, в бедренной кости около 10 миллиардов клеток, так что стволовых клеток там достаточно.
Что касается необходимого для операции количества, одной истинной гемопоэтической стволовой клетки достаточно, чтобы восстановить процесс образования крови, но пока стволовая клетка разгонится и даст всех предшественников, могут пройти месяцы! Поэтому нужно переносить не только стволовые клетки, но и дифференцирующиеся из них предшественники, которые могут на короткий срок восстановить систему кроветворения, но очень быстро. Это как выпечка: вы можете купить готовый продукт, полуфабрикат, исходный продукт или построить ферму. Гемопоэтические клетки — это ферма, и пока она заработает в полную силу, вы умрете с голода.
Нужные стволовые клетки также есть в пуповинной крови, но их там слишком мало: не хватит даже для крупного ребенка, а что уж говорить о взрослом.
Врач-анестезиолог: Я защитник пациентов от хирургической агрессииПоэтому для данной операции клетки берут из костного мозга. Существует два способа получить их. Первый — когда у человека под общей анестезией с помощью специальной огромной иглы из подвздошной кости, точнее, из ее гребня, высасывают часть костного мозга.
Второй — когда с помощью определенных белков, которые дают донору, выводят стволовые клетки из костей в кровь. Далее с помощью специального аппарата их оттуда забирают. Но чтобы таким образом получить достаточное количество стволовых клеток, нужно проводить процедуру на протяжении пяти дней подряд.
— Может ли это как-то навредить донору?
— Нет. Во время процедуры с белками возможна небольшая кратковременная боль в костях.
Если же говорить о процедуре с иглой, то будет немного больно и дискомфортно после процедуры. Однако что такое немного дискомфорта и боли в сравнении с тем, что вы можете подарить кому-то жизнь?
— В июле новостные агентства писали об эксперименте, когда мышам, если не ошибаюсь, вводили стволовые клетки в гипоталамус, что увеличило скорость регенерации всех клеток в организме и, соответственно, замедлило старение. Вы слышали об этом?
— Честно говоря, нет.
Подконтрольная эволюция: какие перспективы открывает генная инженерияОднако иногда в науке какие-то, казалось бы, фантастические вещи оказываются правдой. Да и в целом наука — это открытие неизведанного, а природа удивляет нас постоянно. Никогда не говори никогда. Это особенно актуально для биологии и науки в целом. Если кому-то что-то удалось, кто-то обязательно попытается повторить эксперимент. Так работает наука. В этом и состоит ее прелесть: она всегда проверяет себя.
Вот, например, японский ученый Синья Йаманака обнаружил, что можно взять любую клетку в организме и превратить ее в стволовую. Он взял маленький кусочек кожи мыши, получил из него отдельную клетку, фибробласт. Затем Йаманака понял, что если провести ряд генетических манипуляций, то можно перепрограммировать ее в стволовую клетку, которая может превратиться в любой вид ткани. По факту он получил плюрипотентные стволовые клетки, однако назвал их индуцированными стволовыми клетками.
Благодаря этому открытию ученые научились превращать любую клетку организма в плюрипотентную, которая в свою очередь может трансформироваться в любую другую.
До этого открытия любой ученый сказал бы, что клетка кожи — это клетка кожи и ничем другим никогда не будет. Своеобразная догма. Но Йаманака опровергнул это.
Свой доклад он опубликовал в 2006 году, а в 2012-м получил за это открытие Нобелевскую премию.
— Если можно превратить любую клетку в любую, то почему эта технология не используется при лечении той же лейкемии?
— Мы можем взять любую клетку и спокойно превратить в плюрипотентную стволовую клетку, да. Однако вот сделать из нее стволовую клетку крови — куда более сложная задача. Многие лаборатории в мире сейчас работают над тем, как "уговорить" плюрипотентную стволовую клетку превратиться в нужную. Мы просто не знаем пока тех правил, которые позволят это делать.
— Что вы можете сказать о применении стволовых клеток в косметологии?
— Единственная клинически доказанная процедура со стволовыми клетками — это пересадка костного мозга. Все!
В мире очень много псевдонаучных клиник, который обещают вернуть молодость, красоту и много всего с помощью стволовых клеток. Клинически ничего подобного доказано не было. Это полная чушь! Вас просто хотят развести на деньги.
Единственное, на что можно надеяться, идя на такую процедуру, — это что вам не навредят. Повезет, если они дадут вам солевой раствор. Поверьте, вы не хотите, чтобы они давали вам стволовые клетки, ведь эти горе-врачи не знают, что делают.
Не верьте тому, что вы читаете в интернете.
— Как вы думаете, какие перспективы существуют у стволовых клеток в медицине?
— Да кто ж его знает-то, настоящий потенциал? До 2006-го все думали, что невозможно из одной клетки другую получить.
Российские ученые синтезировали молекулу, предотвращающую заражение ВИЧКак скоро стволовые клетки начнут применять на повседневной основе в медицине? На сегодняшний момент проводится около 40 тысяч операций по пересадке костного мозга в год. Мы пытаемся увеличить этот показатель. Если сделать операцию более безопасной, то в перспективе можно будет лечить и другие заболевания, например ВИЧ.
Слышали про "берлинского пациента"? Это единственный на земле человек, которого смогли вылечить от ВИЧ-инфекции. Зовут его Тимоти Браун. Дважды ему очень крупно не повезло, а один раз невероятно повезло. В 1995 году у мужчины нашли ВИЧ, в 2006-м — лейкемию. Для него нашли донора с мутацией гена CCR5, который делает человека невосприимчивым к ВИЧ. Данная мутация встречается у небольшого числа европейцев (примерно у 10% есть вариант гена delta32, и только у 1% он присутствует в двойном наборе, что делает таких людей резистентными к ВИЧ-1). В 2007 году Тимоти Брауну провели пересадку костного мозга, благодаря чему он победил лейкемию, а затем и ВИЧ. Этот факт неоднократно был подтвержден.
Беседовал Константин Ермолаев
ria.ru
Выращивание органов человека для пересадки: достижения и перспектива
Постиндустриальные темпы развития человечества, а именно науки и техники, велики настолько, что их невозможно было представить еще 100 лет назад. То, о чем раньше можно было прочитать только в научно-популярной фантастике, теперь появилось и в реальном мире.
Уровень развития медицины 21-го века выше, чем когда-либо. Заболевания, считавшиеся смертельно опасными раньше, в наши дни успешно лечатся. Однако еще не решены проблемы онкологии, СПИДа и множества других заболеваний. К счастью, в ближайшем будущем для этих проблем найдется решение, одним из которых послужит выращивание органов человека.
Основы биоинженерии
Наука, использующая информационный базис биологии и пользующаяся аналитическим и синтетическим методами для решения своих задач, зародилась не так давно. В отличие от обычной инженерии, которая для своей деятельности применяет технические науки, по большей части математику и физику, биоинженерия идет дальше и пускает в ход инновационные методы в виде молекулярной биологии.

Одной из главных задач новоиспеченной научно-технической сферы является выращивание искусственных органов в лабораторных условиях с целью их дальнейшей пересадки в тело пациента, у которого отказал из-за повреждения или в силу изношенности тот или иной орган. Опираясь на трехмерные клеточные структуры, ученые смогли продвинуться в изучении влияния различных болезней и вирусов на деятельность человеческих органов.
К сожалению, пока это не полноценные органы, а лишь органоиды – зачатки, незаконченная совокупность клеток и тканей, которые можно использовать только в качестве экспериментальных образцов. Их работоспособность и уживчивость проверяются на подопытных животных, в основном, на разных грызунах.
Историческая справка. Трансплантология
Росту биоинженерии как науки предшествовал долгий период развития биологии и других наук, целью которых было изучение человеческого тела. Еще в начале 20-го века толчок своему развитию получила трансплантология, задачей которой было изучение возможности пересадки органа донора другому человеку. Создание методик, способных консервировать на некоторое время донорские органы, а также наличие опыта и детальных планов по трансплантации позволили хирургам со всего мира в конце 60-х годов успешно пересадить такие органы, как сердце, легкие, почки.
На данный момент принцип трансплантации является наиболее действенным в случае, если пациенту угрожает смертельная опасность. Основная проблема заключается в остром дефиците донорских органов. Больные могут годами ждать своей очереди, так ее и не дождавшись. Кроме того, существует высокий риск того, что пересаженный донорский орган может не прижиться в теле реципиента, так как иммунной системой пациента он будет рассматриваться в качестве инородного предмета. В противоборство данному явлению были изобретены иммунодепрессанты, которые, однако, скорее калечат, чем лечат – иммунитет человека катастрофически ослабевает.
Преимущества искусственного создания над трансплантацией
Одно из главных конкурентных отличий метода выращивания органов от их пересадки от донора заключается в том, что в лабораторных условиях органы могут производиться на основе тканей и клеток будущего реципиента. В основном, используются стволовые клетки, обладающие способностью дифференцироваться в клетки определенных тканей. Данный процесс ученый способен контролировать извне, что существенно снижает риск будущего отторжения органа иммунной системой человека.

Более того, с помощью метода искусственного выращивания органов можно производить их неограниченное количество, тем самым удовлетворяя жизненно важные потребности миллионов людей. Принцип массового производства значительно снизит цены на органы, спасая миллионы жизней и значительно увеличивая выживаемость человека и отодвигая дату его биологической смерти.
Достижения биоинженерии
На сегодняшний день ученые в состоянии выращивать зачатки будущих органов – органоиды, на которых испытывают различные болезни, вирусы и инфекции с целью проследить процесс заражения и разработать тактику противодействия. Успешность функционирования органоидов проверяют посредством их трансплантации в тела животных: кроликов, мышей.

Стоит также отметить, что биоинженерия достигла определенных успехов в создании полноценных тканей и даже в выращивании органов из стволовых клеток, которые, к сожалению, пока невозможно пересадить человеку в силу их неработоспособности. Однако на данный момент ученые научились создавать искусственным путем хрящи, сосуды и другие соединительные элементы.
Кожа да кости
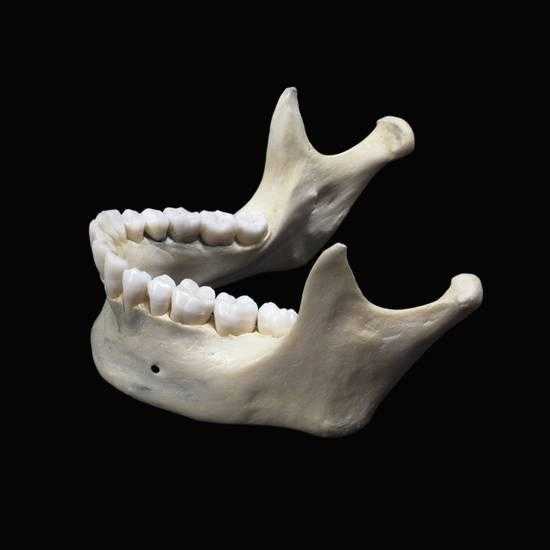
Не так давно у ученых Колумбийского университета получилось создать фрагмент кости, по структуре схожий с суставом нижней челюсти, соединяющим ее с основанием черепа. Фрагмент был получен посредством использования стволовых клеток, как и при выращивании органов. Чуть позже израильской компании Bonus BioGroup удалось изобрести новый метод воссоздания человеческой кости, который был с успехом испробован на грызуне – искусственно выращенная кость была пересажена в одну из его лап. В данном случае опять же были использованы стволовые клетки, только получены они были из жировой ткани пациента и в последующем помещены на гелеобразный каркас кости.
Начиная с 2000-х годов, для лечения ожогов доктора применяют специализированные гидрогели и методы естественной регенерации поврежденных участков кожи. Современные же экспериментальные методики позволяют вылечивать сильнейшие ожоги за несколько дней. Так называемый Skin Gun распыляет особую смесь со стволовыми клетками пациента на поврежденную поверхность. Также наблюдаются крупные успехи в создании стабильно функционирующей кожи с кровеносными и лимфатическими сосудами.
Выращивание органов из клеток
Недавно ученым из Мичигана удалось вырастить в лабораторных условиях часть мышечной ткани, которая, правда, вдвое слабее оригинальной. Точно так же ученые в Огайо создали трехмерные ткани желудка, которые были в состоянии производить все необходимые для пищеварения ферменты.
Японские же ученые совершили почти невозможное – вырастили полностью функционирующий человеческий глаз. Проблема трансплантации заключается в том, что присоединить зрительный нерв глаза к головному мозгу пока не представляется возможным. В Техасе искусственным путем в биореакторе удалось также вырастить легкие, но без кровеносных сосудов, что ставит под сомнение их работоспособность.
Перспективы развития
Совсем недолго осталось до того момента в истории, когда человеку можно будет пересадить большинство органов и тканей, созданных в искусственных условиях. Уже сейчас ученые со всего мира располагают разработками проектов, экспериментальными образцами, некоторые из которых не уступают оригиналам. Кожу, зубы, кости, все внутренние органы по прошествии некоторого времени можно будет создавать в лабораториях и продавать нуждающимся людям.

Новые технологии также ускоряют развитие биоинженерии. 3D-печать, получившая распространение во многих сферах человеческой жизни, будет полезной и в рамках выращивания новых органов. 3D-биопринтеры уже экспериментально используются с 2006 года, а в будущем они смогут создавать трехмерные работоспособные модели биологических органов, перенося культуры клеток на биосовместимую основу.
Общий вывод
Биоинженерия как наука, целью которой является выращивание тканей и органов для их дальнейшей трансплантации, зародилась не так давно. Семимильный темп, в котором она шагает по пути прогресса, характеризуется существенными достижениями, которые в будущем спасут миллионы жизней.
Выращенные из стволовых клеток кости и внутренние органы сведут на нет нужду в донорских органах, количество которых и так находится в состоянии дефицита. Уже сейчас ученые располагают множеством разработок, результаты которых пока не слишком продуктивны, но имеют огромный потенциал.
fb.ru
Органы из пробирки: что уже умеют выращивать - МедНовости
6 сентября 2017 года, 15:48
Возможность вырастить человеческий орган в пробирке и пересадить его человеку, нуждающемуся в пересадке — мечта трансплантологов. Ученые по всему миру работают над этим и уже научились делать ткани, небольшие работающие копии органов, и до полноценных запасных глаз, легких и почек нам на самом деле осталось совсем немного. Пока что органеллы используются в основном в научных целях, их выращивают, чтобы понять, как работают органы, как развиваются болезни. Но от этого до трансплантации всего несколько шагов. МедНовости собрали сведения о самых перспективных проектах.
Легкие. Ученые из Техасского университета вырастили легкие человека в биореакторе. Правда, без кровеносных сосудов такие легкие не функциональны. Однако команда ученых из Медицинского центра Колумбийского университета (Columbia University Medical Center, New York) недавно впервые в мире получили функциональное легкое с перфузируемой и здоровой сосудистой системой у грызунов ex vivo.
Ткани сердечной мышцы. Биоинженерам из университета Мичигана удалось вырастить в пробирке кусок мышечной ткани. Правда, полноценно сердце из такой ткани пока работать не сможет, она вдвое слабее оригинала. Тем не менее пока это самый сильный образец сердечной ткани.
Кости. Израильская биотехнологическая компания Bonus BioGroup использовалат трехмерные сканы для создания гелеобразного каркаса кости перед посевом стволовыми клетками, взятыми из жира. Кости, получившиеся в результате, они успешно пересадили грызунам. Уже планируются эксперименты по выращиванию человеческих костей по этой же технологии.
Ткани желудка. Ученым под руководством Джеймса Уэллса из Детского медицинского клинического центра в Цинциннати (Огайо) удалось вырастить «в пробирке» трехмерные структуры человеческого желудка при помощи эмбриональных стволовых клеток и из плюрипотентных клеток взрослого человека, перепрограммированных в стволовые. Эти структуры оказались способны вырабатывать все необходимые человеку кислоты и пищеварительные ферменты.
Японские ученые вырастили глаз в чашке Петри. Искусственно выращенный глаз содержал основные слои сетчатки: пигментный эпителий, фоторецепторы, ганглионарные клетки и другие. Трансплантировать его целиком пока возможности нет, а вот пересадка тканей — весьма перспективное направление. В качестве исходного материала были использованы эмбриональные стволовые клетки.
Ученые из корпорации Genentech вырастили простату из одной клетки. Молекулярным биологам из Калифорнии удалось вырастить целый орган из единственной клетки. Ученым удалось найти единственную мощную стволовую клетку в простатической ткани, которая способна вырасти в целый орган. Таких клеток оказалось чуть меньше 1% от общего числа. В исследовании 97 мышам трансплантировали такую клетку под почку и у 14 из них выросла полноценная простата, способная нормально функционировать. Точно такую же популяцию клеток биологи нашли и в простате человека, правда, в концентрации всего 0,2%.
Сердечные клапаны. Швейцарские ученые доктор Саймон Хоерстрап (Simon Hoerstrup) и Дорта Шмидт (Dorthe Schmidt) из университета Цюриха (University of Zurich) смогли вырастить человеческие сердечные клапаны, воспользовавшись стволовыми клетками, взятыми из околоплодной жидкости. Теперь медики смогут выращивать клапаны сердца специально для неродившегося еще ребенка, если у него еще в зародышевом состоянии обнаружатся дефекты сердца.
Ушная раковина. Используя стволовые клетки, ученые вырастили ухо человека на спине крысы. Эксперимент был проведен исследователями из Университета Токио (University of Tokyo) И Университета Киото (Kyoto University) под руководством Томаса Сервантеса (Thomas Cervantes).
Кожа. Ученые из Цюрихского университета (Швейцария) и университетской детской больницы этого города впервые сумели вырастить в лаборатории человеческую кожу, пронизанную кровеносными и лимфатическими сосудами. Полученный кожный лоскут способен почти полностью выполнять функцию здоровой кожи при ожогах, хирургических дефектах или кожных болезнях.
Поджелудочная железа. Ученые впервые создали васкуляризованные островки поджелудочной железы, способные вырабатывать инсулин. Еще одна попытка вылечить диабет I типа.
Почки. Ученые из австралийского университета Квинсленда научились выращивать искусственные почки из стволовых клеток кожи. Пока это лишь маленькие органоиды размером 1 см, но по устройству и функционированию они практически идентичны почкам взрослого человека.
Печень. Биологи сразу нескольких стран заявили о том, что смогли вырастить полноценный аналог печени, способный очищать кровь от токсинов и выполнять другие функции этого органа. Для этого ученые использовали стволовые клетки и «заготовки» из стволовых клеток. Эти разработки параллельно велись в Японии, Америке и России.
Мочевой пузырь. Группа американских ученых под руководством Энтони Аталы (Anthony Atala) вырастила в лаборатории человеческие мочевые пузыри, полностью готовые к пересадке, из образцов собственных тканей пациентов. Те же ученые вырастили мочеиспускательные каналы для пациентов, у которых они были повреждены.
Кроме того, ученые уже научились выращивать хрящевые ткани, ткани скелетных мышц и костей, ткани гипофиза, тимуса, а также ткани, функционирующие аналогично тканям человеческого мозга.
medportal.ru
Роботы помогут выращивать органы из стволовых клеток
Исследователи из Школы медицины Университета Вашингтона в Сиэтле, США, разработали новую роботизированную систему автоматизации производства человеческих мини-органов из стволовых клеток. Способность к быстрому массовому производству органоидов обещает расширить их использование в фундаментальных исследованиях и открытии лекарств. Результаты опубликованы 17 мая 2018 года в Cell Stem Cell.
«Это новое «секретное оружие» в борьбе с болезнями», - сказал руководитель исследования Бенджамин Фридман (Benjamin Freedman), доцент медицины отдела нефрологии в Школе медицины Университета Вашингтона (University of Washington Health Sciences/UW Medicine)
Фридман объяснил, что традиционный способ выращивания клеток для биомедицинских исследований представляет собой простое культивирование на плоских двумерных поверхностях. В последние годы исследователи всё более успешно применяют методику формирования из стволовых клеток трёхмерных структур, называемых мини-органами или органоидами. По внешним признакам и своим свойствам они во многом напоминают органы на их зачаточной стадии развития.
И хотя это делает органоиды идеальными для биомедицинских исследований, их массовое производство пока проблематично. По словам авторов исследования, новая роботизированная технология наиболее перспективна в решении именно этой проблемы.
Несмотря на то, что подобные подходы были успешными со взрослыми стволовыми клетками, в настоящей работе учёные впервые использовали плюрипотентные стволовые клетки, обладающие универсальными свойствами и способные создавать любой тип органов.
В процессе исследования роботизированные дозаторы засевали планшеты с 384 миниатюрными лунками стволовыми клетками, а затем их развитие направлялось в органоиды почек в течение 21 дня. Каждая микролунка обычно содержала 10 и более органоидов, т. е. на каждом планшете их было несколько тысяч. Со скоростью, которая впечатлила бы Генри Форда, создавшего конвейерную линию сборки автомобилей, роботизированная система могла обслуживать множество планшетов за считанные минуты.
«Обычно простой эксперимент такого масштаба занимает у исследователей весь день, а робот может это сделать за 20 минут», - говорит Фридман. «Кроме того, робот не устаёт и не совершает ошибок. Без сомненья, повторяющиеся утомительные задачи, подобные этим, роботы выполняют лучше людей».
Исследователи дополнительно обучили роботов обработке и анализу производимых органоидов. Учёные использовали автоматизированную современную технологию, известную как секвенирование РНК одиночных клеток, чтобы идентифицировать все типы клеток в органоидах.
«Мы установили, что данные органоиды действительно напоминают развивающиеся почки, однако мы также обнаружили клетки, не имеющие отношение к почкам, которые ранее не наблюдались в таких культурах», - сказала доктор Дженнифер Хардер (Jennifer Harder), специалист по заболеваниям почек.
«Эти результаты дают лучшее представление о природе данных органоидов и предоставляют нам основание, от которого мы можем отталкиваться», - сказал Фридман.
«Значение этой высокопроизводительной платформы заключается в том, что теперь мы можем всячески изменять процедуру в любой момент и сразу увидеть, какие из изменений дают лучший результат».
Чтобы продемонстрировать это, исследователи открыли способ значительно увеличить количество клеток кровеносных сосудов в органоидах, чтобы сделать их более похожими на настоящие почки.
Учёные также использовали новую технологию для поиска лекарственных препаратов. В одном из таких экспериментов они создавали органоиды с мутациями, вызывающими поликистоз почек – наследственное заболевание, которое часто приводит к почечной недостаточности и встречающееся у 1 человека из 600 во всём мире.
При данном заболевании канальцы в почках расширяются, образуя кисты, вытесняющие здоровую ткань.
В своём эксперименте исследователи воздействовали на органоиды с поликистозом рядом соединений. Они обнаружили, что один из факторов, известный как блеббистатин (blebbistatin), блокирующий белок миозин, провоцировал значительное увеличение количества и размеров кист.
«Это оказалось неожиданностью, поскольку миозин, как известно, не участвует в поликистозе почек», - сказал Фридман.
Миозин, который более известен своей ролью в сокращении мышц, принимает участие в расширении и сокращении канальцев. Фридман пояснил, что сбои в его функциях могут привести к образованию кист.
«Это именно тот путь, который мы будем исследовать», - сказал он.
biopro-st.com
Роботы помогут выращивать органы из стволовых клеток
Исследователи из Школы медицины Университета Вашингтона в Сиэтле, США, разработали новую роботизированную систему автоматизации производства человеческих мини-органов из стволовых клеток. Способность к быстрому массовому производству органоидов обещает расширить их использование в фундаментальных исследованиях и открытии лекарств. Результаты опубликованы 17 мая 2018 года в Cell Stem Cell.
«Это новое «секретное оружие» в борьбе с болезнями», - сказал руководитель исследования Бенджамин Фридман (Benjamin Freedman), доцент медицины отдела нефрологии в Школе медицины Университета Вашингтона (University of Washington Health Sciences/UW Medicine)
Фридман объяснил, что традиционный способ выращивания клеток для биомедицинских исследований представляет собой простое культивирование на плоских двумерных поверхностях. В последние годы исследователи всё более успешно применяют методику формирования из стволовых клеток трёхмерных структур, называемых мини-органами или органоидами. По внешним признакам и своим свойствам они во многом напоминают органы на их зачаточной стадии развития.
И хотя это делает органоиды идеальными для биомедицинских исследований, их массовое производство пока проблематично. По словам авторов исследования, новая роботизированная технология наиболее перспективна в решении именно этой проблемы.
Несмотря на то, что подобные подходы были успешными со взрослыми стволовыми клетками, в настоящей работе учёные впервые использовали плюрипотентные стволовые клетки, обладающие универсальными свойствами и способные создавать любой тип органов.
В процессе исследования роботизированные дозаторы засевали планшеты с 384 миниатюрными лунками стволовыми клетками, а затем их развитие направлялось в органоиды почек в течение 21 дня. Каждая микролунка обычно содержала 10 и более органоидов, т. е. на каждом планшете их было несколько тысяч. Со скоростью, которая впечатлила бы Генри Форда, создавшего конвейерную линию сборки автомобилей, роботизированная система могла обслуживать множество планшетов за считанные минуты.
«Обычно простой эксперимент такого масштаба занимает у исследователей весь день, а робот может это сделать за 20 минут», - говорит Фридман. «Кроме того, робот не устаёт и не совершает ошибок. Без сомненья, повторяющиеся утомительные задачи, подобные этим, роботы выполняют лучше людей».
Исследователи дополнительно обучили роботов обработке и анализу производимых органоидов. Учёные использовали автоматизированную современную технологию, известную как секвенирование РНК одиночных клеток, чтобы идентифицировать все типы клеток в органоидах.
«Мы установили, что данные органоиды действительно напоминают развивающиеся почки, однако мы также обнаружили клетки, не имеющие отношение к почкам, которые ранее не наблюдались в таких культурах», - сказала доктор Дженнифер Хардер (Jennifer Harder), специалист по заболеваниям почек.
«Эти результаты дают лучшее представление о природе данных органоидов и предоставляют нам основание, от которого мы можем отталкиваться», - сказал Фридман.
«Значение этой высокопроизводительной платформы заключается в том, что теперь мы можем всячески изменять процедуру в любой момент и сразу увидеть, какие из изменений дают лучший результат».
Чтобы продемонстрировать это, исследователи открыли способ значительно увеличить количество клеток кровеносных сосудов в органоидах, чтобы сделать их более похожими на настоящие почки.
Учёные также использовали новую технологию для поиска лекарственных препаратов. В одном из таких экспериментов они создавали органоиды с мутациями, вызывающими поликистоз почек – наследственное заболевание, которое часто приводит к почечной недостаточности и встречающееся у 1 человека из 600 во всём мире.
При данном заболевании канальцы в почках расширяются, образуя кисты, вытесняющие здоровую ткань.
В своём эксперименте исследователи воздействовали на органоиды с поликистозом рядом соединений. Они обнаружили, что один из факторов, известный как блеббистатин (blebbistatin), блокирующий белок миозин, провоцировал значительное увеличение количества и размеров кист.
«Это оказалось неожиданностью, поскольку миозин, как известно, не участвует в поликистозе почек», - сказал Фридман.
Миозин, который более известен своей ролью в сокращении мышц, принимает участие в расширении и сокращении канальцев. Фридман пояснил, что сбои в его функциях могут привести к образованию кист.
«Это именно тот путь, который мы будем исследовать», - сказал он.
biopro-st.com
Роботы помогут выращивать органы из стволовых клеток
Исследователи из Школы медицины Университета Вашингтона в Сиэтле, США, разработали новую роботизированную систему автоматизации производства человеческих мини-органов из стволовых клеток. Способность к быстрому массовому производству органоидов обещает расширить их использование в фундаментальных исследованиях и открытии лекарств. Результаты опубликованы 17 мая 2018 года в Cell Stem Cell.
«Это новое «секретное оружие» в борьбе с болезнями», - сказал руководитель исследования Бенджамин Фридман (Benjamin Freedman), доцент медицины отдела нефрологии в Школе медицины Университета Вашингтона (University of Washington Health Sciences/UW Medicine)
Фридман объяснил, что традиционный способ выращивания клеток для биомедицинских исследований представляет собой простое культивирование на плоских двумерных поверхностях. В последние годы исследователи всё более успешно применяют методику формирования из стволовых клеток трёхмерных структур, называемых мини-органами или органоидами. По внешним признакам и своим свойствам они во многом напоминают органы на их зачаточной стадии развития.
И хотя это делает органоиды идеальными для биомедицинских исследований, их массовое производство пока проблематично. По словам авторов исследования, новая роботизированная технология наиболее перспективна в решении именно этой проблемы.
Несмотря на то, что подобные подходы были успешными со взрослыми стволовыми клетками, в настоящей работе учёные впервые использовали плюрипотентные стволовые клетки, обладающие универсальными свойствами и способные создавать любой тип органов.
В процессе исследования роботизированные дозаторы засевали планшеты с 384 миниатюрными лунками стволовыми клетками, а затем их развитие направлялось в органоиды почек в течение 21 дня. Каждая микролунка обычно содержала 10 и более органоидов, т. е. на каждом планшете их было несколько тысяч. Со скоростью, которая впечатлила бы Генри Форда, создавшего конвейерную линию сборки автомобилей, роботизированная система могла обслуживать множество планшетов за считанные минуты.
«Обычно простой эксперимент такого масштаба занимает у исследователей весь день, а робот может это сделать за 20 минут», - говорит Фридман. «Кроме того, робот не устаёт и не совершает ошибок. Без сомненья, повторяющиеся утомительные задачи, подобные этим, роботы выполняют лучше людей».
Исследователи дополнительно обучили роботов обработке и анализу производимых органоидов. Учёные использовали автоматизированную современную технологию, известную как секвенирование РНК одиночных клеток, чтобы идентифицировать все типы клеток в органоидах.
«Мы установили, что данные органоиды действительно напоминают развивающиеся почки, однако мы также обнаружили клетки, не имеющие отношение к почкам, которые ранее не наблюдались в таких культурах», - сказала доктор Дженнифер Хардер (Jennifer Harder), специалист по заболеваниям почек.
«Эти результаты дают лучшее представление о природе данных органоидов и предоставляют нам основание, от которого мы можем отталкиваться», - сказал Фридман.
«Значение этой высокопроизводительной платформы заключается в том, что теперь мы можем всячески изменять процедуру в любой момент и сразу увидеть, какие из изменений дают лучший результат».
Чтобы продемонстрировать это, исследователи открыли способ значительно увеличить количество клеток кровеносных сосудов в органоидах, чтобы сделать их более похожими на настоящие почки.
Учёные также использовали новую технологию для поиска лекарственных препаратов. В одном из таких экспериментов они создавали органоиды с мутациями, вызывающими поликистоз почек – наследственное заболевание, которое часто приводит к почечной недостаточности и встречающееся у 1 человека из 600 во всём мире.
При данном заболевании канальцы в почках расширяются, образуя кисты, вытесняющие здоровую ткань.
В своём эксперименте исследователи воздействовали на органоиды с поликистозом рядом соединений. Они обнаружили, что один из факторов, известный как блеббистатин (blebbistatin), блокирующий белок миозин, провоцировал значительное увеличение количества и размеров кист.
«Это оказалось неожиданностью, поскольку миозин, как известно, не участвует в поликистозе почек», - сказал Фридман.
Миозин, который более известен своей ролью в сокращении мышц, принимает участие в расширении и сокращении канальцев. Фридман пояснил, что сбои в его функциях могут привести к образованию кист.
«Это именно тот путь, который мы будем исследовать», - сказал он.
biopro-st.com
Выращивание органов для трансплантации в лаборатории
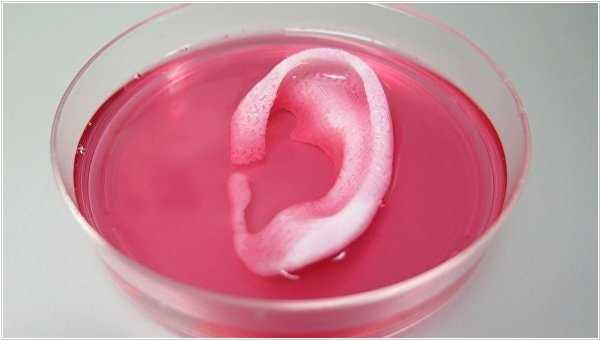 Биоинженеры из Института регенеративной медицины в Уэйк-Форесте (США) разработали необычную технологию трехмерной печати, которая позволяет создавать полноценные копии отдельных костей, мышц и хрящей из стволовых клеток. До сих пор ученым удавалось распечатывать только очень тонкие слои живой ткани (до 200 мкм) - иначе ткань начинала гибнуть, так как питательные вещества и кислород не могут проникнуть на такую глубину без наличия кровеносных сосудов. В данном случае биоинженеры использовали особый полимер, позволявший укладывать клетки слоями и при этом сохранять небольшой просвет между ними. А после печати, ученые помещают органоид в организм мыши, где он постепенно "зарастает" кровеносными сосудами, а полимер постепенно разлагается, уступая им место. В конечном итоге на месте заготовки возникает полноценный орган, обладающий нужной трехмерной формой и всеми необходимыми видами ткани.
Биоинженеры из Института регенеративной медицины в Уэйк-Форесте (США) разработали необычную технологию трехмерной печати, которая позволяет создавать полноценные копии отдельных костей, мышц и хрящей из стволовых клеток. До сих пор ученым удавалось распечатывать только очень тонкие слои живой ткани (до 200 мкм) - иначе ткань начинала гибнуть, так как питательные вещества и кислород не могут проникнуть на такую глубину без наличия кровеносных сосудов. В данном случае биоинженеры использовали особый полимер, позволявший укладывать клетки слоями и при этом сохранять небольшой просвет между ними. А после печати, ученые помещают органоид в организм мыши, где он постепенно "зарастает" кровеносными сосудами, а полимер постепенно разлагается, уступая им место. В конечном итоге на месте заготовки возникает полноценный орган, обладающий нужной трехмерной формой и всеми необходимыми видами ткани.
2014. В Японии хотят выращивать в свиньях органы для людей
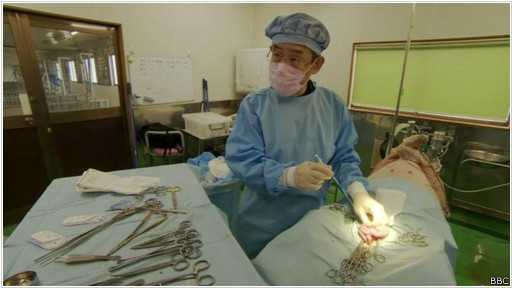 Ученые из Университета Токио проводят невероятный эксперимент, главная цель которого - научиться выращивать свиней с человеческой поджелудочной железой и другими человеческими органами. Все начинается с того, что в зародыше белой свиньи выключается ген, ответственный за развитие поджелудочной железы. Затем исследователи вводят в эмбрион стволовые клетки из другого организма (в экспериментах используются клетки черной свиньи). При развитии такой эмбрион превратится в обычную свинью, за исключением того, что ее поджелудочная железа в генетическом отношении будет органом черной свиньи. В перспективе можно получать эмбрионы (химеры), в которых имеется человеческая поджелудочная, или почка, или печень, а может быть, даже и сердце. При этом такой орган будет генетически идентичен тому человеческому организму, из которого получены исходные клетки кожи. А это полностью снимет проблему отторжения пересаживаемых органов, с которой сталкивается сейчас трансплантология.
Ученые из Университета Токио проводят невероятный эксперимент, главная цель которого - научиться выращивать свиней с человеческой поджелудочной железой и другими человеческими органами. Все начинается с того, что в зародыше белой свиньи выключается ген, ответственный за развитие поджелудочной железы. Затем исследователи вводят в эмбрион стволовые клетки из другого организма (в экспериментах используются клетки черной свиньи). При развитии такой эмбрион превратится в обычную свинью, за исключением того, что ее поджелудочная железа в генетическом отношении будет органом черной свиньи. В перспективе можно получать эмбрионы (химеры), в которых имеется человеческая поджелудочная, или почка, или печень, а может быть, даже и сердце. При этом такой орган будет генетически идентичен тому человеческому организму, из которого получены исходные клетки кожи. А это полностью снимет проблему отторжения пересаживаемых органов, с которой сталкивается сейчас трансплантология.
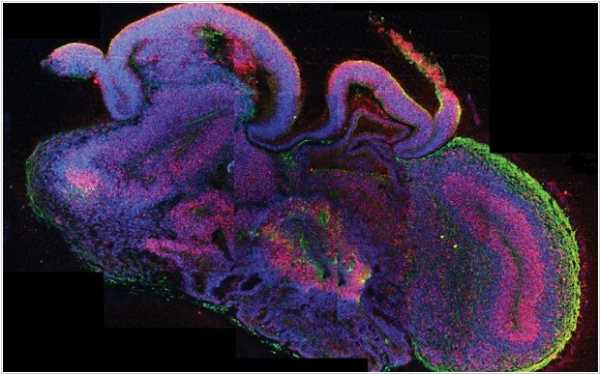 Выращивание различных органов для трансплантации - это очень полезная и понятная затея. Но зачем выращивать головной мозг? Ведь в мозге находится сознание человека, запрограммированное нейронными связями и его нельзя заменить стандартным мозгом, выращенным в лаборатории... Однако, ученые из австрийского Института Молекулярной Биологии говорят, что искусственно выращенный мозг - неоценим для испытания лекарств и методов лечения нейродегенеративных заболеваний. Им удалось вырастить мозговую ткань (органоид) из стволовых клеток. Для этого они поместили стволовые клетки в специальную среду, стимулирующую их трансформацию в нейроны. За 30 дней удается вырастить мозг-органоид размеров в несколько миллиметров. Дальнейший рост пока невозможен из-за того, что в органоиде нет сосудов для снабжения и очищения клеток.
Выращивание различных органов для трансплантации - это очень полезная и понятная затея. Но зачем выращивать головной мозг? Ведь в мозге находится сознание человека, запрограммированное нейронными связями и его нельзя заменить стандартным мозгом, выращенным в лаборатории... Однако, ученые из австрийского Института Молекулярной Биологии говорят, что искусственно выращенный мозг - неоценим для испытания лекарств и методов лечения нейродегенеративных заболеваний. Им удалось вырастить мозговую ткань (органоид) из стволовых клеток. Для этого они поместили стволовые клетки в специальную среду, стимулирующую их трансформацию в нейроны. За 30 дней удается вырастить мозг-органоид размеров в несколько миллиметров. Дальнейший рост пока невозможен из-за того, что в органоиде нет сосудов для снабжения и очищения клеток.
2009. Как клонируют человеческие органы
Клонирование органов и тканей для трансплантации (воссоздание органов и тканей в лаборатории) - это одно из самых многообещающих направлений в медицине. И многие достижения этой технологии родились в стенах Американского института регенеративной медицины Wake Forest Institute. На видео - впечатляющая презентация директора этого института, Энтони Аталы. Он начал свое выступление с того, что каждые 30 секунд в мире умирает пациент, которого можно было бы спасти с помощью замены органа или ткани. Пересаживать органы научились еще 55 лет назад, но с тех пор никакого особого прогресса в этом направлении нет. Основная проблема (с которой медики пока ничего не могут поделать) - дефицит донорских органов. Вот было бы здорово, если б органы для трансплантации можно было выращивать за несколько недель в лаборатории. Как это делают в институте Wake Forest? ***
www.livemd.ru
















